Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "БРОНХИАЛЬНАЯ АСТМА У ДЕТЕЙ: ЛЕЧЕНИЕ, ПРОФИЛАКТИКА Часть 2"
Автор: Пшеничная Е.В.
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Педиатрия/Неонатология, Пульмонология, Семейная медицина/Терапия
Просмотров: 3 280
Дата проведения: с 18.12.2014 по 18.12.2015
Актуальность проблемы. Бронхиальная астма (БА) является глобальной проблемой здравоохранения. Люди всех возрастов во всем мире страдают этим хроническим заболеванием дыхательных путей, которое при недостаточно эффективном лечении может значительно ограничивать повседневную жизнь пациентов и даже приводить к смерти.
Целью лечения БА является достижение и поддержание контроля над клиническими проявлениями заболевания. Многие больные БА получают (или получали) те или иные противоастматические препараты. Задачей врача является определение у каждого отдельного пациента текущего уровня терапии и уровня контроля над БА, последующая коррекция лечения с целью достижения и поддержания контроля над БА. Контроль над БА означает, что у пациентов отсутствуют симптомы заболевания (в том числе ночные) или они минимальны, нет ограничений повседневной активности (включая физические упражнения), отсутствует потребность в препаратах неотложной помощи (или она минимальна), функция легких близка к норме, частота обострений крайне низкая.
Общая цель: уметь определить тактику ведения ребенка с бронхиальной астмой.
Конкретные цели: определить план лечебно-профилактических мероприятий ребенка с бронхиальной астмой.
Содержание обучения
Теоретические вопросы
- Задачи, которые необходимо решать при лечении бронхиальной астмы.
- Требования к диетическому режиму ребенка, страдающего бронхиальной астмой.
- Контроль окружающей среды.
- Доставочные устройства ингаляционных препаратов.
- Лекарственные препараты, используемые для лечения бронхиальной астмы.
- Ступенчатый подход к лечению бронхиальной астмы.
- Лечение приступа бронхиальной астмы.
- Лечение тяжелого приступа бронхиальной астмы у детей раннего возраста.
- Терапия астматического состояния.
- Показатели эффективной терапии бронхиальной астмы.
- Качество жизни детей, больных бронхиальной астмой.
- Прогноз клинического течения БА у детей.
- Меры профилактики обострений БА у детей.
Ориентировочная основа деятельности
Во время подготовки к занятию необходимо ознакомиться с основными теоретическими вопросами с помощью источников литературы.
ЗАДАЧИ, РЕШАЕМЫЕ ПРИ ЛЕЧЕНИИ БРОНХИАЛЬНОЙ АСТМЫ
Основные задачи при ведении ребенка с бронхиальной астмой.
- Купирование обострений.
- Достижение ремиссии со снижением дозы требуемых медикаментов.
- Закрепление ремиссии.
- Перевод бронхиальной астмы в более легкую форму.
- Обеспечение действенного контроля заболевания до возможного выздоровления ребенка.
ДИЕТИЧЕСКИЙ РЕЖИМ
У детей с бронхиальной астмой должна быть элиминационная гипоаллергенная диета с полным исключением из пищи больного ребенка продуктов, способствующих выбросу биологически активных веществ и, прежде всего гистамина в кровь. К ним относятся явные (любой продукт питания) и облигатные аллергены (фрукты и овощи, содержащие каротин, орехи, яйца, шоколад, мед, рыба и др.), под влиянием которых происходит либерация гистамина в кровь, приводящая к запуску аллергической реакции в шоковом органе, т.е. в бронхиальной системе, не сопровождаясь появлением дерматоаллергии. Отсутствие последней позволяет родителям, а иногда и медикам считать, что данные нутриенты непричастны к возникновению и сохранению бронхиальной астмы у детей. Между тем продолжающееся поступление в организм больного этих продуктов способствует неблагоприятному течению бронхиальной астмы и снижает эффективность терапии и вторичной профилактики.
Определяя диетический режим ребенку, страдающему бронхиальной астмой, следует также иметь ввиду возможность перекрестного реагирования. Так, установлено перекрестное реагирование на пыльцу подсолнечника и такие продукты как халва, семечки, подсолнечное масло, на продукты, содержащие грибок или полученные на его основе – сыр, сметана, кефир, выпечка и др.
Длительность периода элиминации при бронхиальной астме исчисляется годами, а также может быть пожизненной.
ТРЕБОВАНИЯ К СРЕДЕ, ОКРУЖАЮЩЕЙ РЕБЕНКА
Ребенок, страдающий бронхиальной астмой должен иметь отдельную комнату, оборудование которой исключает предметы «собирающие» домашнюю пыль (мягкая мебель, ковры, тяжелые портьеры, подушки, набитые пухом, пером, шерстью, стеганые одеяла, мягкие игрушки, открытые стеллажи с книгами и т.п.). Лучшим материалом для занавесок, постельного белья является хлопок. В связи с высокой сенсибилизирующей способностью сухого корма для рыб, не рекомендуется держать в комнате ребенка аквариум.
Ежедневно должна проводиться влажная уборка. Следует избегать использования пылесоса. Последним можно пользоваться для уборки других помещений при закрытой комнате ребенка и в период его отсутствия. Вообще комнату ребенка следует постоянно держать закрытой.
МЕДИКАМЕНТОЗНАЯ ТЕРАПИЯ
Ингаляционная терапия – краеугольный камень лечения БА. Практически все дети могут научиться правильно пользоваться ингаляторами. Для эффективного лечения пациентов разного возраста требуются разные ингаляторы; выбор типа ингалятора должен быть индивидуальным.
При лечении детей информация о дозе препарата, которая попадает в легкие, для конкретной лекарственной формы обычно отсутствует; к тому же между разными ингаляторами существуют выраженные различия в величине легочной фракции. Это следует учитывать в случае замены одного ингалятора на другой. Кроме того, при выборе типа ингалятора необходимо принимать во внимание эффективность доставки препарата, стоимость, безопасность, простоту использования, удобство и наличие данных о применении этого типа ингалятора в данной возрастной группе пациентов.
Ингаляционные препараты для лечения БА представлены в виде дозирующих аэрозольных ингаляторов (ДАИ), активируемых дыханием ДАИ, дозирующих порошковых ингаляторов (ДПИ), ингаляторов типа «soft mist» (новое устройство без пропеллентов, создающее медленно перемещающееся и долго сохраняющееся «облачко» мелкодисперсных частиц (менее 5,8 мкм) препарата), растворов для небулайзерной терапии (так называемых «влажных» аэрозолей). Разные ингаляторы различаются по эффективности доставки лекарственного препарата в нижние дыхательные пути, зависящей от типа ингалятора и формы лекарственного средства, размера частиц, скорости аэрозольного облачка или струи (не у всех ингаляторов) и простоты применения ингалятора у большинства пациентов. Предпочтения отдельных больных, удобство и простота применения ингалятора могут повлиять не только на эффективность доставки препарата, но и на то, насколько аккуратно больной будет выполнять назначения врача, а также на контроль над заболеванием при длительной терапии (см. таблицу 1).
Таблица 1
Выбор типа ингалятора для детей разного возраста
Для пользования ДАИ необходимо предварительное обучение пациентов и умение координировать вдох с активацией ингалятора. При нажатии на баллончик ДАИ открывается клапан и выбрасывается струя газа, содержащая одну дозу препарата (рис. 1). ДАИ могут использоваться при БА разной степени тяжести, в том числе при обострении.
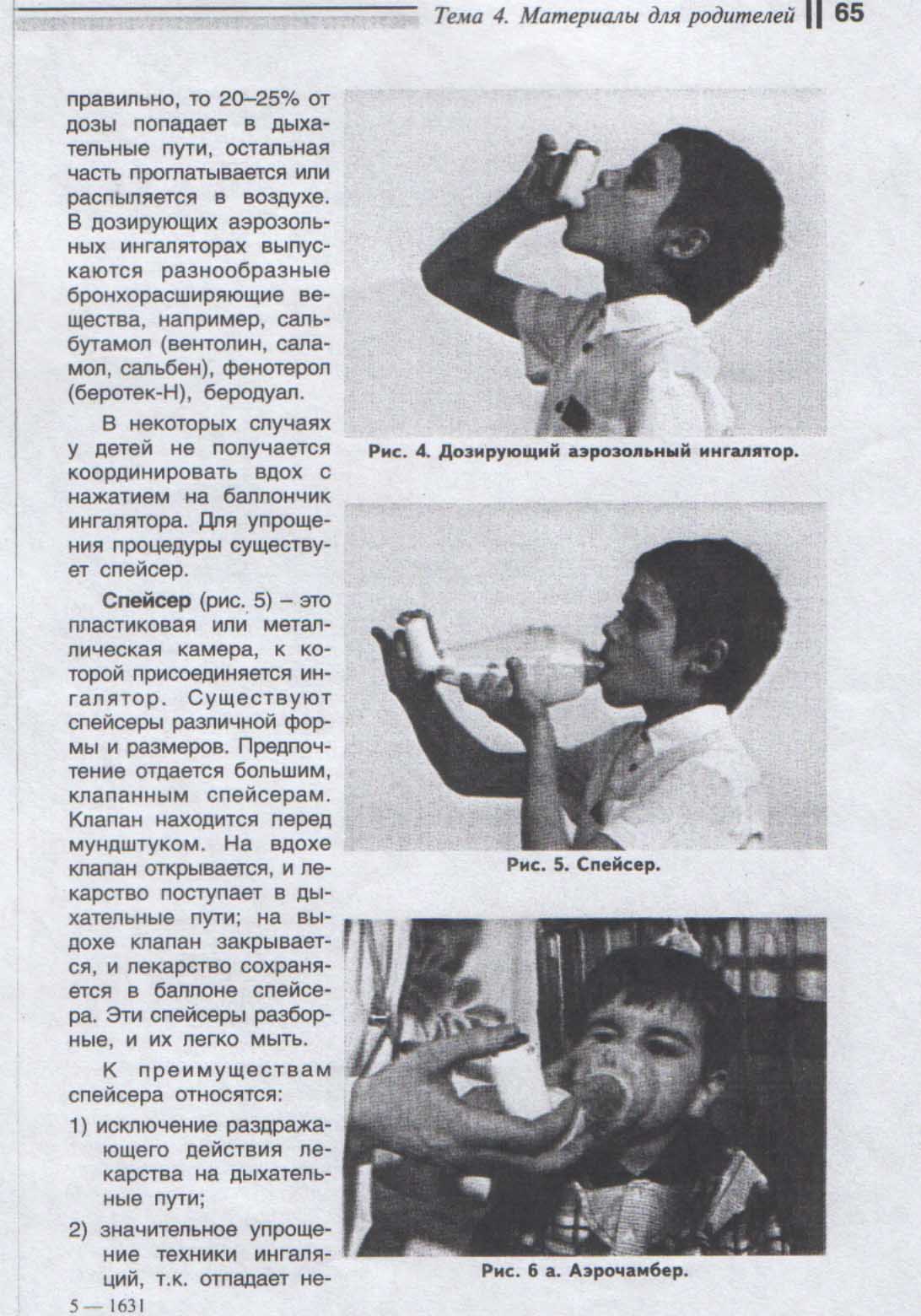
Рис. 1. Дозирующий аэрозольный ингалятор.
Активируемые дыханием ДАИ могут быть полезны больным, которые испытывают трудности при пользовании обычными ДАИ, требующими координации вдоха и нажатия на распылитель.
При применении ингаляторов типа «soft mist» четкая координация вдоха и нажатия на распылитель не является таким же критичным условием правильности ингаляции, как при использовании ДАИ.
Дозирующие порошковые ингаляторы обычно проще использовать, однако они требуют определенного усилия вдоха (достижения минимальной скорости вдоха), которое может оказаться слишком большим для некоторых больных. ДПИ различаются по тому, какой процент от дозы, вышедшей из распылителя, поступает в легкие.
При терапии некоторыми препаратами переход с ДАИ на ДПИ может потребовать коррекции дозы лекарственного средства.
В целом использование ДАИ со спейсерами следует предпочесть небулайзерной терапии, так как ДАИ более удобны, обеспечивают более эффективную доставку препарата в легкие при меньшем риске побочных эффектов и меньшей стоимости. В спейсерах задерживаются крупные частицы взвеси препарата, которые без спейсера оседали бы в ротоглотке. В результате снижается всасывание препарата во рту и желудочно-кишечном тракте и, следовательно, системная биодоступность ингалируемого препарата (рис. 2).

Рис. 2. Спейсеры.
Использование спейсера также уменьшает частоту побочных эффектов со стороны ротоглотки. В случае острого приступа БА необходимо применять ДАИ только со спейсером, так как в такой ситуации ребенок может не суметь правильно скоординировать вдох с активацией ДАИ. Предпочтительно использовать имеющиеся в продаже спейсеры с хорошо изученными характеристиками доставки препарата. В случае их недоступности возможно применение самодельного спейсера (например, сделанного из пластиковой бутылки от газированной воды емкостью 500 мл).
Небулайзеры не обеспечивают точную дозировку препаратов, являются дорогостоящими и требуют затрат времени на использование и обслуживание, а также нуждаются в техническом обслуживании. Они в основном предназначены для детей, не способных пользоваться другими типами ингаляторов. Небулайзеры часто применяются при тяжелых обострениях БА, хотя в этой ситуации ДАИ со спейсером не менее эффективны (рис. 3, 4).

Лекарственные вещества, применяемые для лечения бронхиальной астмы, разделяются на две группы: препараты для длительного контроля (ингаляционные и системные глюкокортикостероиды, кромоны, β2-агонисты длительного действия, антилейкотриеновые препараты, теофиллин) и препараты для оказания неотложной помощи (β2-агонисты короткого действия, системные глюкокортикостероиды, теофиллин короткого действия). Выбор лекарственных веществ проводится с учетом тяжести состояния больного и степени тяжести течения заболевания.
ПРЕПАРАТЫ, КОНТРОЛИРУЮЩИЕ ТЕЧЕНИЕ ЗАБОЛЕВАНИЯ
ИНГАЛЯЦИОННЫЕ ГЛЮКОКОРТИКОСТЕРОИДЫ
Ингаляционные глюкокортикостероиды (ИГКС) обладают выраженным противовоспалительным действием, в основе которого лежит стабилизация биологических мембран и ограничение выхода биологически активных веществ в межклеточное пространство, тем самым предупреждая деструктивные процессы в бронхиальном дереве. Ингаляционные глюкокортикостероиды угнетают образование антител, иммунных комплексов, а также пролиферацию фибробластов и синтез ими коллагена, что снижает интенсивность развития склеротического процесса в стенке бронхов. ИГКС уменьшают гиперреактивность бронхов и способствуют восстановлению поврежденного эпителия бронхов, не оказывая отрицательного влияния на мукоцилиарный клиренс.
Использование ингаляционных глюкокортикостероидов приводит к достаточно быстрому созданию высокой концентрации лекарственного препарата непосредственно в трахеобронхиальном дереве и позволяет избежать развития системных побочных явлений. Наряду с этим отмечено, что использование значительных доз ингаляционных глюкокортикостероидов в течение длительного периода времени может вызывать обратимую супрессию гипоталамо-гипофизарно-надпочечниковой системы, замедление роста и развитие остеопороза, а также у детей с иммунодефицитным состоянием повышение риска возникновения оппортунистической инфекции.
К местным осложнениям ингаляционной глюкокортикостероидной терапии относят кандидоз и дисфонию, что также может возникать при высокой дозе препарата и длительном применении.
В настоящее время ИГКС являются единственными препаратами базисной терапии у детей младше 3 лет, эффективность которых доказана исследованиями, проведенными в течение длительного периода времени. При прекращении ИГКС симптомы БА могут возобновляться. У детей применяют беклометазон, флутиказон, будесонид в дозах, представленных в таблице 2.
Таблица 2
Суточные дозы ИГКС для детей старше 5 лет
|
Препарат |
Низкие суточные дозы (мкг) |
Средние суточные дозы (мкг) |
Высокие суточные дозы (мкг) |
|
Беклометазона дипропионат Будесонид Будесонид Неб Циклесонид Флунизолид Флутиказона пропионат Мометазона фуроат Триамцинолона ацетонид |
100-200
100-200 250-500 80-160 500-750 100-200
100
400-800 |
≥200
|
≥400
|
Ингаляционные глюкокортикостероиды используются при ведении детей со среднетяжелой и тяжелой бронхиальной астмой. Установлено, что они не эффективны при астматическом статусе, при котором следует назначать системные глюкокортикостероиды.
АНТИЛЕЙКОТРИЕНОВЫЕ ПРЕПАРАТЫ
Лейкотриены обладают выраженным провоспалительным и бронхоконстрикторным действием. Так, активность лейкотриенов С4 и Д4 превышает действие гистамина более, чем в 1000 раз. Кроме того, они индуцируют секрецию слизи в бронхиальном дереве, замедляя ее эвакуацию путем снижения активности реснитчатого эпителия. Лейкотриены также повышают сосудистую проницаемость, способствуют поступлению эозинофилов и нейтрофилов в дыхательные пути. Под влиянием лейкотриенов изменяется возбудимость нервных волокон, повышается освобождение тахикининов из пресинаптических окончаний.
Указанные обстоятельства явились побудительным моментом для разработки антилейкотриеновых препаратов и их использования в комплексе терапии бронхиальной астмы.
Антилейкотриеновые препараты (монтелукаст, зафирлукаст) блокируют рецепторы лейкотриенов, ингибируют фермент 5-липооксигеназу и снижают синтез лейкотриенов. Монтелукаст разрешен к применению у детей старше 6 лет по 5мг. один раз в вечернее время. Зафирлукаст назначается детям старше 12 лет. Длительность применения антагонистов лейкотриенов определяется особенностями течения бронхиальной астмы и в среднем составляет 2-3 недели.
Результаты клинических наблюдений показали, что упомянутые препараты уменьшают выраженность аллергического воспаления как в ранние, так и в поздние фазы, снижают гиперреактивность бронхов и тем самым оказывают положительное терапевтическое действие. При средне- и тяжелой формах бронхиальной астмы, а также аспириновой астме следует использовать совместное применение антилейкотриеновых и глюкокортикоидных препаратов. Указанная комбинация позволяет достигнуть взаимоусиливающего положительного терапевтического эффекта.
β2-АГОНИСТЫ ДЛИТЕЛЬНОГО ДЕЙСТВИЯ
β2-агонисты длительного действия (салметерол, формотерол) в основном используются в качестве дополнительной терапии у детей в возрасте старше 5 лет в случае недостаточного контроля над БА на фоне применения средних доз ИГКС, а также в виде отдельных ингаляций перед интенсивной физической нагрузкой. Следует избегать монотерапии ингаляционными β2-агонистами длительного действия. Их следует использовать только в комбинации с адекватной дозой ИГКС предпочтительно в виде фиксированной комбинации.
Ингаляционные β2-агонисты длительного действия хорошо переносятся у детей даже при длительном применении, однако вследствие противоречивых данных об их влиянии на обострения БА эти препараты не рекомендуются в тех случаях, когда требуется более одного лекарства для контроля течения заболевания.
Что же касается пероральных β2-агонистов длительного действия, то они могут быть использованы для предупреждения ночных приступов бронхиальной астмы, в том числе и в качестве дополнения к ингаляционным глюкокортикостероидам в тех случаях, когда последние в стандартных дозах не обеспечивают достаточного контроля ночных симптомов.
К возможным нежелательным эффектам β2-агонистов длительного действия относят стимуляцию сердечно-сосудистой системы, повышение возбудимости скелетной мускулатуры, гипокалиемию, повышение тревожности, что ограничивает их применение. Терапия пероральными β2_агонистами длительного действия практически не обеспечивает защиты от бронхоспазма, вызванного физической нагрузкой.
Развитие указанных явлений чаще наблюдается при использовании пероральных β2-агонистов.
ТЕОФИЛЛИН
Теофиллин, относящийся к метилксантинам, обладает бронходилатирующим, противовоспалительным и иммуномодулирующим действием.
Теофиллин эффективен в качестве монотерапии и терапии, назначаемой в дополнение к ингаляционным или пероральным ГКС у детей в возрасте старше 5 лет. Он устраняет дневные и ночные симптомы, улучшает функцию легких. Поддерживающая терапия обеспечивает пограничный защитный эффект от бронхоспазма, вызванного физической нагрузкой. Добавление теофиллина у детей с тяжелой БА, получающих ингаляционные или пероральные ГКС, позволяет улучшить контроль над БА и снизить поддерживающую дозу ГКС. Для поддерживающей терапии предпочтительно использование препаратов с замедленным высвобождением, так как их можно принимать два раза в сутки.
Самыми частыми побочными эффектами теофиллина являются анорексия, тошнота, рвота и головная боль. Также возможны легкая стимуляция центральной нервной системы, дрожь, тахикардия, аритмии, боли в животе, диарея и редко желудочное кровотечение. Эти побочные эффекты преимущественно встречаются при использовании доз >10 мг/кг/сут. Риск нежелательных эффектов снижается, если терапию начинают с доз 5 мг/кг/сут и дозу постепенно увеличивают до 10 мг/кг/сут. Тяжелая передозировка теофиллина может приводить к смерти.
АНТИТЕЛА К ИММУНОГЛОБУЛИНУ E
Эффективность применения анти-IgE (омализумаб) доказана у детей в возрасте от 6 до 12 лет с аллергической (IgE-опосредованной) персистирующей БА средней тяжести и тяжелой персистирующей БА.
Уровень IgE у многих детей с БА, которая трудно поддается лечению, выше, чем верхняя граница, рекомендуемая для терапии анти-IgE (1300 МЕ). Эффективность омализумаба у данной категории пациентов неизвестна. В настоящее время не существует тестов, которые позволяли бы спрогнозировать, будет ли пациент отвечать на терапию.
Терапия анти-IgE является дорогостоящей, требует регулярного введения препарата и наблюдения за пациентом после каждой инъекции. Согласно данным анализа стоимости и эффективности, для того чтобы сократить расходы, терапию анти-IgE следует назначать детям, у которых было не менее 5 госпитализаций с общейпродолжительностью пребывания в стационаре не менее 20 дней.
При терапии анти-IgE наблюдаются нежелательные явления легкой и средней степени тяжести; к ним относятся: крапивница, сыпь, гиперемия, зуд.
КРОМОНЫ
Противовоспалительные препараты – кромоны (кромогликат натрия и недокромил натрия) обладают широким спектром действия. Точкой их приложения являются многие клетки (тучные, эозинофилы, эпителиальные, а также клетки сенсорных нервов). Одним из основных их действий является ингибиция выхода биологически активных веществ из тучных клеток, эпителиальных клеток слизистой дыхательных путей и тем самым – предупреждение развития приступа бронхиальной астмы. Показано, что их применение предупреждает формирование аллергических реакций, уменьшает частоту обострений бронхиальной астмы и потребность в симпатомиметиках и глюкокортикоидах, способствует предупреждению бронхоконстрикции, в том числе в связи с физической нагрузкой, а в случае возникновения – уменьшает ее тяжесть и продолжительность.
Недокромил натрия обладает эффекторным действием в отношении снижения гиперреактивности кашлевых рецепторов. Кромоны являются действенными препаратами для длительного проведения базисной терапии больным детям дошкольного и школьного возраста, а также при выведении из послеприступного периода детей с гормонозависимой бронхиальной астмой. Назначаются при легком, а также среднетяжелом течении БА, а также с целью профилактики обострений бронхиальной астмы в связи с возможным предстоящим контактом с аллергенами (периоды цветения и др.). Кромоны не должны отменяться в периоды года, неблагоприятные для больных бронхиальной астмой. Основным регулятором дозы указанных препаратов является состояние больного. По мере его улучшения доза снижается. Привыкания к данным препаратам не наблюдается. Побочные эффекты (кашель, бронхоспазм, раздражение глотки) редки. Самыми частыми побочными эффектами недокромила являются неприятный вкус, головная боль и тошнота.
СИСТЕМНЫЕ ГЛЮКОКОРТИКОСТЕРОИДЫ
Системные глюкокортикостероиды вводятся перорально и парэнтерально. Механизм их терапевтического действия аналогичен ингаляционным глюкокортикостероидам, однако при длительном применении они обладают выраженными нежелательными действиями, к которым относятся минералокортикоидный эффект, ожирение, подавление функциональной активности гипоталамо-гипофизарно-надпочечниковой системы, артериальная гипертензия, стероидный диабет, остеопороз, снижение иммунного статуса и ряд других. Указанные обстоятельства обуславливают необходимость их кратковременного использования при острой тяжелой астме. В частности они показаны при:
- астматическом статусе;
- тяжелом приступе бронхиальной астмы, если предыдущие снимались с помощью системных глюкокортикоидов;
- частых повторных тяжелых приступах бронхиальной астмы в случае отсутствия эффекта от ингаляционных глюкокортикостероидов;
- приступе, возникшем у ребенка с аспириновой астмой;
- возникновении признаков надпочечниковой недостаточности.
В ряде случаев возникает необходимость совместного использования ингаляционных и системных глюкокортикостероидов. При этом следует стремиться к более короткому применению последних.
К препаратам выбора системных глюкокортикостероидов относятся преднизолон, преднизон, метилпреднизолон, как обладающие менее выраженными нежелательными эффектами.
СРЕДСТВА НЕОТЛОЖНОЙ ПОМОЩИ
ИНГАЛЯЦИОННЫЕ Β2-АГОНИСТЫ БЫСТРОГО ДЕЙСТВИЯ И ПЕРОРАЛЬНЫЕ Β2-АГОНИСТЫ КОРОТКОГО ДЕЙСТВИЯ
Симпатомиметики β2-агонисты оказывают релаксирующее действие на гладкую мускулатуру бронхов, вызывая бронходилатирующий эффект, предотвращают выход из клеток биологически активных веществ (гистамина, кининов, лейкотриенов и др.), повышают мукоцилиарный клиренс, снижают сосудистую проницаемость.
β2-агонисты быстрого короткого действия (сальбутамол, тербуталин, фенотерол) применяются в приступный период заболевания для купирования бронхоспазма, а также с целью профилактики обструктивных явлений, индуцируемых физической нагрузкой. По сравнению с пероральным или внутривенным применением ингаляционный путь введения обеспечивает более быструю бронходилатацию при более низкой дозе и меньших побочных эффектах. Кроме того, ингаляционная терапия обеспечивает выраженную защиту от бронхоспазма, вызванного физической нагрузкой и другими провоцирующими факторами, в течение 0,5-2 ч (применение β2-агонистов длительного действия сопровождается более продолжительным защитным эффектом).
Потребность в пероральных препаратах возникает редко, обычно у маленьких детей, не способных получать ингаляционную терапию.
Возникновение необходимости частого или ежедневного применения β2-агонистов быстрого действия или снижение их эффективности (отсутствие быстрого и стойкого ответа) при обострении бронхиальной астмы свидетельствует об ухудшении ее течения и необходимости назначения или усиления противовоспалительной терапии.
Побочные эффекты: тремор скелетных мышц, головная боль, сердцебиение и небольшое возбуждение являются самыми частыми жалобами, связанными с назначением детям высоких доз β2-агонистов. Эти жалобы чаще отмечаются при системном применении препаратов и обычно исчезают при продолжении терапии.
АНТИХОЛИНЕРГИЧЕСКИЕ ПРЕПАРАТЫ
Холинолитики (ипратропиума бромид и окситропиума бромид) оказывают бронхолитическое действие путем блокирования ацетилхолина, поступающего из холинергических нервных окончаний дыхательных путей. Оказывают блокирующее действие на рефлекторную бронхоконстрикцию, индуцированную вдыханием различных раздражающих веществ, а также снижают выраженность триггерного воздействия вирусной инфекции – индукция обострения бронхиальной астмы. Применяются ингаляционно. Ингаляционные антихоленэргические вещества более медленно вызывают терапевтический эффект.
К нежелательным эффектам ингаляционных антихоленэргических препаратов относится появление у некоторых больных сухости в полости рта и ощущения горького вкуса. Ингаляционные антихолинергические средства не рекомендованы для длительного лечения БА у детей.
Препараты неотложной помощи
|
Препарат |
Доза |
Побочные эффекты |
Комментарии |
|
Β2-адреномиметики:Сальбутамол (ДАИ)
Сальбутамол (небулайзер)
Фенотерол (ДАИ)
Фенотерол (раствор для небулайзерной терапии) |
1 доза – 100 мкг по 1 -2 ингаляции до 4 раз в день 2,5 мг/2,5 мл: < 6 лет – 1,25 мл, – 2,5 мл 1 доза – 100 мкг по 1 -2 ингаляции до 4 раз в день 1 мг/мл: < 6 лет – 10 капель, – 20 капель |
Тахикардия, тремор, головная боль, раздражитель-ность |
При ингаляционном применении более быстрое начало действия по сравнению с пероральными формами. При использовании 1 баллончика за 1 мес. можно предположить плохой контроль БА, при использовании 2 баллончиков – тяжелый, угрожающий жизни характер течения |
|
Антихолинергические препараты: Ипратропия бромид (ДАИ)
Ипратропия бромид (раствор для небулайзерной терапии) |
1 доза – 20 мкг по 2-3 ингаляции до 4 раз в день 250 мкг/мл: < 3 лет – 30 капель |
Минимальная сухость и неприятный вкус во рту |
Более медленное начало действия, применяют при непереносимостиΒ2-адреномиметиков |
|
Комбинированные препараты: Фенотерол Ипратропия бромид (ДАИ) Фенотерол ипратропия бромид (раствор для небулайзерной терапии) |
по 2 ингаляции до 4 раз в день
1-2 мл: < 6 лет – 10 капель, – 20 капель |
Тахикардия, тремор скелетных мышц, головная боль, раздражитель-ность. Минимальная сухость и неприятный вкус во рту |
|
|
Теофиллины короткого действия:Аминофиллин |
150 мг – по 12-24 мг/кг/сут |
Тошнота, рвота, головная боль, тахикардия, нарушения ритма |
Необходим мониторинг концентрации теофиллина в сыворотке крови |
СТУПЕНЧАТЫЙ ПОДХОД К ЛЕЧЕНИЮ
Ступенчатый подход лечения БА подразумевает увеличение уровня терапии при возрастании степени тяжести заболевания. Если пациент уже получает лечение, классификация тяжести БА должна основываться на имеющихся клинических признаках и дозах ежедневно принимаемых лекарственных средств. Например, пациенты с сохраняющимися (несмотря на проведение терапии, соответствующей данной ступени) симптомами легкой персистирующей БА должны рассматриваться как имеющие персистирующую БА средней тяжести. То есть при ступенчатом подходе к терапии переход на более высокую ступень показан в том случае, если контроля не удается достичь или он теряется на фоне проводимой терапии, причем необходимо быть уверенным, что пациент правильно принимает препараты. Целью лечения является достижение контроля над болезнью с применением наименьшего количества препаратов.
Ступень 1, легкая интермиттирующая БА.
Симптомы болезни появляются только при контакте с аллергеном или триггером. Если такового нет, симптомы болезни отсутствуют, а показатели функции легких находятся в пределах нормы. Интермиттирующую форму БА также диагностируют у больных с эпизодами БА физического усилия. Нечастые симптомы и не нарушенная функция легких являются основанием для того, чтобы не рекомендовать при этой форме БА длительную терапию противовоспалительными препаратами. Больные нуждаются в лекарственной терапии в периоды обострения болезни.
В качестве средств неотложной помощи используют ингаляционные формы сальбутамола.
Ступень 2, легкая персистирующая БА.
Если у пациента необходимость в приеме лекарственных средств появляется чаще 1 раза в неделю на протяжении более 3 месяцев, его следует расценивать как больного с легкой персистирующей БА.
Препараты выбора у детей любого возраста – ИГКС в низких дозах (беклометазон, флутиказон, будесонид). В качестве альтернативных препаратов для контроля БА рассматривают теофиллины замедленного высвобождения и кромоны. В случае сохранения симптомов болезни у пациента, начавшего лечение БА с использования теофиллина медленного высвобождения или кромонов, следует спустя 4 недели назначить ИГКС.
Монотерапия другими препаратами (кроме ГКС) менее эффективна для контроля воспаления при БА.
Исследование монотерапии β2-адреномиметиками длительного действия у детей выявило некоторую эффективность этих препаратов, однако результаты исследований противоречивы. Применение антилейкотриеновых препаратов у детей с легкой персистирующей БА не изучалось. У больных с более тяжелыми формами заболевания препараты этой группы обладают умеренной эффективностью, поэтому их можно использовать у некоторых пациентов для контроля БА.
У детей старше 12 лет в качестве стартовой терапии может быть выбрана комбинация ИГКС и длительно действующего β2-адреномиметика.
Помимо регулярного применения препаратов для контроля БА, пациенту должен быть доступен ингаляционный β2-адреномиметик быстрого действия для купирования симптомов при необходимости, однако частота его применения не должна превышать 3-4 раз в сутки. Применение симптоматических препаратов более 4 раз в сутки указывает на плохой контроль БА на данной схеме терапии, в таких случаях следует считать, что пациент имеет более тяжелую степень БА.
Ступень 3, среднетяжелая персистирующая БА.
Дети с интермиттирующей БА, но с тяжелыми обострениями должны расцениваться как имеющие персистирующую БА средней степени тяжести. При среднетяжелой персистирующей БА симптомы возникают ежедневно в течение длительного времени или ночью, чаще 1 раза в неделю. Диагноз персистирующей БА средней тяжести ставят пациенту с исходным значением ПСВ до приема лекарственных средств более 60%, но менее 80% от должного или индивидуального лучшего значения и вариабельностью ПСВ от 20 до 30%. Если течение БА не удается контролировать низкими дозами ИГКС (ступень 2), то такую БА следует расценивать как персистирующую средней степени тяжести.
Больные со среднетяжелой персистирующей БА должны ежедневно принимать противовоспалительные препараты, контролирующие течение заболевания. Препаратами выбора у детей старше 5 лет являются ИГКС в низких/средних дозах и β2-адреномиметики длительного действия, а у детей младше 5 лет – ИГКС в средних дозах. Лучше всего в качестве средств усиливающей терапии изучены ингаляционные β2-адреномиметики длительного действия. Кроме того, можно также применять теофиллин медленного высвобождения и антилейкотриеновые препараты (монтелукаст, зафирлукаст). Эффективность этих препаратов варьирует у отдельных пациентов, поэтому дополнительную терапию следует выбирать индивидуально.
Помимо регулярного применения препаратов для контроля БА, у пациента должен быть ингаляционный β2-адреномиметик быстрого действия, который он должен использовать при необходимости для купирования симптомов, но не чаще 3-4 раз в сутки.
Если контроля БА достичь не удается, следует начать лечение, соответствующее ступени 4.
Ступень 4, тяжелая персистирующая БА.
Терапией первого ряда при тяжелой персистирующей БА у детей является комбинация ИГКС (флутиказон, будесонид) в высоких дозах и ингаляционных длительно действующих β2-адреномиметиков (салметерол, формотерол). С этой целью рекомендованы также препараты комбинированной терапии, так называемые фиксированные комбинации (флутиказон салметерол, будесонид формотерол). Дополнительное назначение β2-адреномиметика длительного действия к базисной терапии ИГКС при неконтролируемом течении болезни дает больший клинический эффект, чем увеличение дозы ИГКС в 2 раза и более. Хотя ингаляционные β2-адреномиметики длительного действия лучше всего изучены и наиболее предпочтительны в качестве дополнительной терапии, однако можно использовать теофиллин медленного высвобождения, антилейкотриеновые препараты. В некоторых случаях на 2-4-й ступенях терапии может потребоваться применение короткого курса системных ГКС для быстрого достижения контроля заболевания. Рекомендуемая доза пероральных ГКС для короткого курса составляет 1-2 мг/кг/сут (по преднизолону) и не должна превышать 60 мг/сут. Длительное лечение пероральными ГКС следует начинать в минимально возможных дозах, лучше всего в виде однократного приема утром для сведения к минимуму возможных побочных эффектов. При переводе больных с пероральных ГКС на ИГКС необходимо наблюдать их на предмет развития симптомов надпочечниковой недостаточности. У больных, получающих комбинированную терапию, начать снижение объема лечения следует с уменьшения дозы ИГКС примерно на 25% каждые 3 месяца. После того как доза ГКС составит менее 800 мкг будесонида в сутки (для детей младше 12 лет) или эквивалента, следует отменить дополнительную терапию. На этапе уменьшения интенсивности терапии рекомендуется наблюдать пациента не реже 1 раза в 3 месяца.
При тяжелой БА контроль над симптомами достигается далеко не всегда, в таком случае цель лечения заключается в получении наилучших возможных результатов.
В дополнение к базисной терапии используется β2-адреномиметик быстрого действия по потребности для облегчения симптомов, но желательно не чаще 3-4 раз в сутки.
Таким образом, комбинация текущего уровня симптомов и текущей ступени лечения дает возможность установить тяжесть БА для пациента и назначить соответствующее лечение. После того как контроль над заболеванием установлен и поддерживается в течение не менее 3 месяцев, следует провести попытку уменьшения объема терапии (ступень вниз) и определить минимальное лечение, необходимое для сохранения контроля. Если контроль поддерживается не менее 3 месяцев, степень тяжести должна быть пересмотрена в соответствии с новым лечением.
АЛГОРИТМ ЛЕЧЕНИЯ ТЯЖЕЛОГО ПРИСТУПА БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ РАННЕГО ВОЗРАСТА
(О.И. Ласица)
|
|
|
|
НЕОТЛОЖНАЯ ПОМОЩЬ ПРИ АСТМАТИЧЕСКОМ СОСТОЯНИИ
Основными задачами неотложной терапии при астматическом состоянии является снятие блокады β2-адренорецепторов, бронхообструкции, нормализация метаболизма.
Комплекс неотложных мероприятий для выведения из астматического состояния включает:
- оксигенотерапию, проводимую с помощью кислородной палатки или маски, доводя и поддерживая уровень насыщения крови кислородом выше 90%;
- кортикостероиды. Преднизолон в дозе 2-3 мг на 1 кг массы тела при первой стадии астматического состояния, 4-5 мг при второй и 6-7 мг при третьей. Вся доза преднизолона вводится внутривенно, причем половина ее вводится струйно и остальная часть капельно. Указанная доза повторяется каждые 3,5-4 часа, до выведения ребенка из астматического статуса;
- 2,4% раствор эуфиллина по 1 мл на год жизни, но не боле 10 мл. указанная доза вводится внутривенно каждые 8-12 часов (½ дозы струйно и ½ капельно);
- при наличии метаболического ацидоза вводится внутривенно капельно 4% раствор гидрокарбоната натрия (исходная доза 3-4 мл/кг) под контролем щелочно-кислотного равновесия;
- с целью регидратации вводится внутривенно капельно жидкость, вначале из расчета 20 мл на 1 кг массы тела, а затем вводимое количество определяется клиническим состоянием и диурезом. Для внутривенного капельного введения используется физиологический раствор, 5% раствор глюкозы, реополиглюкин. Ни в коем случае нельзя вводить плазму, альбумин и другие белковые растворы.
Противопоказано введение симпатомиметиков, β2-агонистов, седативных средств, фитопрепаратов, муколитиков, витаминов, проведение физиотерапевтических процедур.
При возникновении третьей стадии астматического состояния (гипоксической комы) – перевод в реанимационное отделение.
После выведения из астматического статуса с целью стабилизации состояния β2-адренорецепторов показано в течение недели один раз в день капельное введение 2,4% раствора эуфиллина из расчета 1мл на год жизни, но не более 10 мл. Снижение дозы преднизолона проводится постепенно в течение 12-14 дней. В период снижения дозы преднизолона может обнаружиться гормонозависимость бронхиальной астмы, свидетельством чего является появление реакции отмены (рикошета), признаками которой является нарастание или появление обструктивных явлений после очередного снижения дозы кортикостероида. В этих случаях возникает необходимость длительной глюкокортикоидной терапии в сочетании с кромонами.
ГОРМОНОЗАВИСИМАЯ БРОНХИАЛЬНАЯ АСТМА
Гормонозависимая бронхиальная астма относится к ее наиболее тяжелой форме, встречаясь у 10-15% детей. Для ее течения характерны частые приступы удушья, резистентные к обычной бронхолитической терапии, возникновение астматических состояний различной степени выраженности, в том числе и третьей (асфиксического синдрома). Достижение положительного клинического эффекта возможно только при использовании кортикостероидной терапии.
К факторам, способствующим формированию гормонозависимой формы, относят двустороннюю наследственную отягощенность, поливалентную сенсибилизацию, наличие других проявлений аллергии, перинатальное повреждение центральной нервной системы, нерациональное лечение, неадекватное применение кортикостероидов, выраженность морфологических (воспалительных и структурных – склерозирование) изменений в бронхиальном дереве, надпочечниковая недостаточность.
Имеются сведения, что у детей с гормонозависимой формой бронхиальной астмы наряду со снижением Т-лимфоцитов и повышением общего IgE наблюдается повышенный уровень циркулирующих иммунных комплексов. К гормонозависимой форме с полным правом может быть отнесена аспириновая астма. Гормонозависимая форма бронхиальной астмы требует длительной кортикостероидной терапии с использованием системных и ингаляционных кортикостероидных препаратов, как в остром периоде заболевания, так и в качестве базисного лечения.
Прогноз при гормонозависимой форме бронхиальной астмы серьезен. Именно при этой форме чаще возможен летальный исход, чему способствует несвоевременное назначение кортикостероидов и неправильное их использование (неадекватность доз, нерациональность выбора пути введения). Возможность полного выздоровления минимальна, частота же прогрессирования тяжести течения заболевания значительно выше, чем при других формах.
ИММУНОТЕРАПИЯ БРОНХИАЛЬНОЙ АСТМЫ
Иммунотерапия – один из действенных методов лечения бронхиальной астмы, включающий аллергенспецифическую иммунотерапию и иммунофармакотерапию.
Специфическая иммунотерапия (аллерговакцинация) показана детям с атопической бронхиальной астмой легкого и среднетяжелого течения при четкой доказанности этиологической значимости аллергенов в случаях невозможности их элиминировать из окружающей больного среды; при недостаточной эффективности фармакотерапии и при отсутствии противопоказаний, к которым относятся острый период бронхиальной астмы, ее тяжелое течение, сопутствующая патология. Специфическая иммунотерапия заключается в парентеральном, эндоназальном, сублингвальном, пероральном введении причинно значимых аллергенов в возрастающей дозе, что приводит к гипосенсибилизирующему эффекту. В основе последнего имеет место подавление Th2-ответа и индуцирование Th1-ответа, активация толерантности В-лимфоцитов, продуцирующих IgE, снижение продукции 1, 2, 4 интерлейкинов, повышение уровня специфических IgE антител. Обсуждаемый метод более эффективен при моновалентной сенсибилизации. К наиболее эффективной относится специфическая гипосенсибилизация аллергенами домашней пыли, клещевыми, а также грибковыми.
Специфическая иммунотерапия проводится детям, начиная с шестилетнего возраста в строгом соответствии с указаниями, представленными в инструкциях к стандартизованным аллергенным вакцинам. Возможно проведение нескольких курсов специфической иммунотерапии. Показателем ее эффективности является прекращение приступов бронхиальной астмы или урежение их частоты и тяжести с соответствующим снижением потребности в медикаментах.
В связи с возможностью возникновения местных и системных аллергических реакций специфическая аллерговакцинация проводится в условиях аллергического кабинета или специализированного аллергологического отделения. После введения аллергенной вакцины ребенок должен быть под наблюдением врача не менее 30 минут. Купирование системных аллергических реакций проводится с помощью адреналина, глюкокортикоидов и антигистаминных препаратов, вводимых парентерально.
АНТИБИОТИКИ ПРИ ЛЕЧЕНИИ БРОНХИАЛЬНОЙ АСТМЫ
Непосредственно для лечения бронхиальной астмы антибиотики не используются. Наряду с этим следует отметить, что инфекционный фактор (вирусы, вирусно-бактериальные ассоциации) относится к триггерам обострений бронхиальной астмы. Также установлено, что бактериальная флора (пневмококки, срептококки, стафилококки, микоплазма, хламидии) принимают участие в генезе эндобронхиального хронического воспалительного процесса при БА. Бактериальная инфекция может также осложнять течение бронхиальной астмы, вызывая развитие пневмонии, гнойного эндобронхита и других банальных воспалительных очагов. В этих случаях, наряду с наросшей тяжестью состояния, возникает рефрактерность к проводимой противоастматической терапии и прогрессирование бронхообструкции, повышение температуры, нейтрофилез, иногда повышение СОЭ. Эти обстоятельства диктуют необходимость назначения антибиотической терапии. Препаратами выбора в этих случаях являются цефалоспорины, макролиды и фторхинолоны. Следует помнить, что препараты пенициллинового ряда противопоказаны, как и внутривенное введение любого антибиотика. Длительность антибиотической терапии определяется динамикой клинической симптоматики и параклинических данных.
ОБУЧЕНИЕ ПАЦИЕНТА
Обучение пациента подразумевает установление партнерства между ним, его семьей и медицинским работником. Хорошее взаимопонимание очень важно как основа для дальнейшей хорошей подверженности лечению (комплаентности). Пациентов необходимо обучить:
- избегать факторов риска;
- правильно принимать лекарственные средства;
- различать лекарственные средства для контроля заболевания и для купирования симптомов обострения;
- мониторингу симптомов заболевания, пикфлоуметрии (у детей старше 5 лет);
- распознавать признаки, предполагающие ухудшение БА, и предпринимать соответствующие действия;
- обратиться за медицинской помощью при необходимости.
ДАЛЬНЕЙШЕЕ ВЕДЕНИЕ
Персистирующую БА гораздо эффективнее контролировать с помощью длительной противовоспалительной терапии, чем лечением только симптомов обострения заболевания.
Существует два подхода для достижения контроля над БА.
- Быстрое достижение контроля путем начала лечения с более высокого уровня (например, короткий курс пероральных ГКС и/или применение более высоких доз ИГКС в сочетании с β2-адреномиметиком длительного действия в дополнение к терапии, соответствующей степени тяжести БА у пациента).
- Начало лечения со ступени, соответствующей степени тяжести заболевания с последующим увеличением на ступень вверх при необходимости.
Первый подход более предпочтителен. Ступень вверх («step up»), если контроль над заболеванием не достигнут.
Улучшение состояния должно наступить в течение месяца (обязательно нужно проверить технику ингаляции ребенка, комплаентность, исключить факторы риска).
Терапию необходимо пересматривать каждые 3-6 месяцев (если контроль БА достигнут). Дополнительными и крайне важными компонентами ведения пациентов с БА являются постоянный мониторинг симптомов и пиковой скорости выдоха (ПСВ) с ведением дневника самоконтроля и разработка индивидуального плана действий.
САНАТОРНО-КУРОРТНОЕ ЛЕЧЕНИЕ
Санаторно-курортное лечение включает климатотерапию, бальнеотерапию и пелоидотерапию. Для проведения климатотерапии используют морской, горный, лесной и степной климаты. Следует помнить, что зоны, где имеется сочетание высоких температур и влажности, дети, больные бронхиальной астмой, переносят плохо. Они хорошо себя чувствуют на побережье Азовского моря, в Крыму, на Рижском взморье.
Горноклиматическое лечение с успехом осуществляется в горах Кавказа в условиях среднегорья. Терапия лесным и степным климатами используется в местных санаториях.
В основе бальнеотерапии лежит наружное применение естественных минеральных вод (купание в бассейнах, общие и местные ванны). Минеральными водами выбора являются хлоридные натриевые, гидрокарбонатные натриевые, азотно-термальные и родоновые. Кроме того, минеральные воды могут использоваться в качестве ингаляций, полосканий, энтерального применения. Они оказывают положительное влияние на метаболические процессы, а также противовоспалительное действие. В этом отношении хорошо зарекомендовала себя свежеталая вода, которую следует назначать энтерально в дозе 10 мл/кг массы в сутки, а также в ингаляциях. Она оказывает гипосенсибилизирующее, противовоспалительное действие и нормализирует функциональное состояние мерцательного эпителия. К бальнеологическим курортам относятся Моршин, Кисловодск, Пятигорск и др. Возможно сочетание бальнеотерапии с пелоидотерапией. Последняя может проводиться и отдельно. Используются различные пелоиды (лечебные грязи) – иловые, торфяные, сопочные и др., в виде аппликаций, а также электропроцедур, оказывающие противовоспалительный и рассасывающий эффекты.
Санаторно-курортное лечение показано во время стойкой ремиссии (спустя три и более месяцев после минования острого периода) при атопической и смешанной формах бронхиальной астмы легкого и среднетяжелого течения.
НЕТРАДИЦИОННЫЕ МЕТОДЫ ЛЕЧЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ
К нетрадиционным методам лечения относятся ирритотерапия, включающая иглорефлексотерапию, электроакупунктуру, лазерную терапию в импульсном и непрерывном режимах, гомеопатия, фитотерапия, аюрведческая медицина, гипно-, спелеотерапия и ряд других. Имеющиеся сведения об их эффективности довольно противоречивы и не апробированы с позиций доказательной медицины. Если проведенный курс не является эффективным, то повторение их в дальнейшем не является целесообразным. Факторами, оказывающими благоприятное влияние на организм больного бронхиальной астмой является чистота воздуха, его насыщенность ионами, мелкодисперсными частичками соляной пыли. Существенное положительное влияние оказывают микроклиматические условия: низкая влажность, комфортная температура и атмосферное давление. Воздух помещения лишен аллергенов, имеет низкое содержание инфекционной флоры.
Показаниями для проведения спелеотерапии являются бронхиальная астма интермиттирующего легкого и средней тяжести интермиттирующего течения. Длительность курса лечения – один месяц. В процессе спелеотерапии наблюдается постепенное улучшение самочувствия и общего состояния, заключающегося в нормализации у большинства больных (70-75%) функции внешнего дыхания, исчезновении приступов удушья, снижении выраженности сенсибилизации и воспалительных изменений в бронхиальном дереве. Длительность положительного воздействия спелеотерапии на состояние ребенка с бронхиальной астмой различна, достигая нескольких месяцев.
ПРОФИЛАКТИКА
ПЕРВИЧНАЯ ПРОФИЛАКТИКА.
Профилактика БА связана с предупреждением развития аллергии у ребенка. Первичная профилактика БА и аллергии направлена на предотвращение возникновения заболевания у лиц из группы риска. В настоящее время не существует эффективных пренатальных мер по первичной профилактике БА.
Постнатальная профилактика БА и аллергии предусматривает проведение следующих мероприятий.
- Следует поощрять грудное вскармливание, его преимущества включают защитный эффект от возникновения свистящих хрипов в раннем возрасте.
- Курящих родителей необходимо предупредить о вреде курения для ребенка, в том числе об увеличении частоты возникновения свистящих хрипов. Воздействие табачного дыма как пренатально, так и постнатально оказывает неблагоприятное влияние на течение заболеваний, сопровождающихся бронхиальной обструкцией.
ВТОРИЧНАЯ ПРОФИЛАКТИКА.
Мероприятия по вторичной профилактике БА и аллергии ориентированы на детей, у которых доказано наличие сенсибилизации, возможно наличие астмаподобных симптомов (кашля, свистящих хрипов, затруднения дыхания), но БА еще нет. Это дети из групп риска, у которых удается выявить:
- семейный анамнез БА или аллергии (риск БА до50%);
- другие аллергические заболевания (атопический дерматит, аллергический ринит, риск БА – 10-20%);
- повышенную концентрацию общего IgE (более 30 МЕ/мл) в сочетании с выявлением специфических IgE-AT к белкам коровьего молока/куриного яйца, к аэроаллергенам более 0,35 МЕ/мл (у ребенка с атопическим дерматитом или аллергическим ринитом риск возрастает до 70%).
В целях вторичной профилактики БА в группах риска предлагается превентивная терапия цетиризином. Назначение цетиризина в дозе 0,25 мг/кг/сут в течение 18 месяцев детям из группы высокого риска (с отягощенным аллергоанамнезом и кожными проявлениями аллергии) с бытовой или пыльцевой сенсибилизацией приводит к снижению частоты бронхообструкции с 40 до 20%. Установлена протективная роль специфической иммунотерапии в группах риска.
ТРЕТИЧНАЯ ПРОФИЛАКТИКА
Направлена на уменьшение воздействия провоцирующих факторов для улучшения контроля БА у больных детей и уменьшения потребности в лекарственной терапии.
ЭЛИМИНАЦИОННЫЙ РЕЖИМ
Соблюдение элиминационного режима может способствовать уменьшению тяжести течения уже существующего заболевания. Частый контакт с аллергенами у сенсибилизированных пациентов способствует усилению симптомов БА, бронхиальной гиперреактивности, ухудшению функции легких.
Из аллергенов, с которыми человек контактирует в быту, следует выделить аллерены клещей домашней пыли, животных (имеющих шерсть или мех), тараканов и грибов.
Мероприятия для уменьшения воздействия
аллергенов клещей домашней пыли.
- Необходимо использовать специальные непроницаемые чехлы для матрацев, подушек и одеял.
- Ковры или ковровые покрытия следует заменить на линолеум, деревянные полы либо паркет.
- Все постельные принадлежности нужно ежедневно стирать в горячей (55-60°С) воде.
- Ковры необходимо обрабатывать акарицидными жидкостями и/или таниновой кислотой.
- Для уборки желательно использовать пылесос со встроенным НЕРА-фильтром и пылесборником с толстыми стенками.
- Мягкие игрушки нужно стирать в горячей воде или периодически замораживать. Применение домашних ионизаторов воздуха не приводит к уменьшению выраженности симптомов БА.
- Необходимо устранить очаги плесени и не допускать высокой влажности в квартире в течение всего года.
Мероприятия для уменьшения контакта
с аллергенами домашних животных.
- Не следует пускать животное в спальню или основную жилую комнату.
- Для уборки желательно использовать пылесос со встроенным НЕРА-фильтром и пылесборником с толстыми стенками.
- Даже после полного удаления животных из дома может пройти много месяцев, прежде чем концентрация аллергена снизится до приемлемых величин.
Заселение квартиры тараканами – важная причина аллергической сенсибилизации, особенно в городских домах. Однако мероприятия по борьбе с тараканами оказывают лишь частичный эффект.
Пищевая аллергия редко является фактором обострения БА, главным образом у детей раннего возраста.
Риск аллергической сенсибилизации у детей увеличивает пассивное курение. Оно также повышает частоту и тяжесть симптомов у детей, страдающих БА. Всем пациентам с БА и родителям детей с БА следует воздерживаться от курения.
Важным в плане профилактики БА является ограничение контакта с поллютантами внутри и вне помещений. Адекватная вентиляция и вытяжные устройства позволяют снизить концентрацию оксидов азота, угарного и углекислого газа, бытовых аэрозолей. Для ограничения воздействия летучих эфирных соединений не следует проводить ремонт помещений в присутствии больных детей или допускать их в только что отремонтированные квартиры. Необходимо помнить, что иногда в результате погодных и атмосферных условий создаются периоды особо интенсивного загрязнения атмосферного воздуха, когда более предпочтительным является пребывание дома в чистом, хорошо кондиционируемом помещении.
Пищевые факторы как триггеры БА могут быть актуальными в группе детей раннего возраста или у больных с пыльцевой сенсибилизацией. В процессе проведения элиминационно-провокационных тестов должны быть выявлены и в дальнейшем исключены из питания больных продукты, вызывающие обострение болезни. Подлежат полному исключению из применения ацетилсалициловая кислота и другие НПВС в связи с их способностью запускать особые механизмы аллергии, которые могут привести к тяжелым и угрожающим жизни обострениям БА у детей с повышенной чувствительностью к ним. Важным является анамнестическое выявление аллергии на пенициллин с последующим исключением этой группы препаратов ввиду угрозы развития анафилактических реакций.
Одной из причин обострений и неконтролируемого тяжелого течения БА могут быть частые ОРВИ, а также сопутствующие риносинуситы. В связи с этим полезной может быть ежегодная противогриппозная вакцинация, хотя доказательных данных относительно этих рекомендаций недостаточно.
ПРОГНОЗ
У детей с повторяющимися эпизодами свистящих хрипов на фоне острой вирусной инфекции, не имеющих признаков атопии и атопических заболеваний в семейном анамнезе, симптомы обычно исчезают в дошкольном возрасте, и БА в дальнейшем не развивается, хотя могут сохраняться минимальные изменения функции легких и бронхиальная гиперреактивность. При возникновении свистящих хрипов в раннем возрасте (до 2 лет) вероятность того, что симптомы будут сохраняться и в более позднем возрасте, невелика. У детей раннего возраста с частыми эпизодами свистящих хрипов, БА в семейном анамнезе и проявлениями атопии риск развития БА в возрасте 6 лет значительно увеличивается. Мужской пол является фактором риска для возникновения БА в препубертатном периоде, однако существует большая вероятность того, что БА по достижении взрослого возраста исчезнет. Женский пол является фактором риска персистирования БА во взрослом возрасте.
Рекомендованная литература
- Глобальная стратегия лечения и профилактики бронхиальной астмы (пересмотр 2011 г.) Под ред. А.С. Белевского. – М.: Российское респираторное общество, 2012. – 108 с.,
- Острополец С.С. Бронхиальная астма у детей. – Севастополь: «Вебер», 2004. – 136 с.
- Бронхиальная астма у детей: диагностика, лечение и профилактика: Науч.-практ. программа (Союз педиатров России. Междунар. фонд…), 2004.
- Балаболкин И.И. Бронхиальная астма у детей. – М.: Медицина, 2003. – 304 с.
- Новик Г.А., Бовичев А.В. Спирометрия и пикфлоуметрия при бронхиальной астме у детей (учебное пособие). – СПб.: Издание ГПМА, 2005. – 68 с.








