Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "ДИАГНОСТИКА И ЛЕЧЕНИЕ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ"
Автор: Багрий А.Э., Хоменко М.В.
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Кардиология, Неврология, Ревматология, Семейная медицина/Терапия
Просмотров: 3 929
Дата проведения: с 18.11.2015 по 18.11.2016
 Термином хроническая сердечная недостаточность (ХСН) обозначают состояние, при котором сердце неспособно обеспечивать выброс в циркуляцию такого количества оксигенированной крови, которое бы удовлетворяло потребности тканей, в том числе при нагрузке. ХСН рассматривается как исход различных заболеваний сердца, она характеризуется истощением резервных возможностей миокарда и системных компенсаторных механизмов.
Термином хроническая сердечная недостаточность (ХСН) обозначают состояние, при котором сердце неспособно обеспечивать выброс в циркуляцию такого количества оксигенированной крови, которое бы удовлетворяло потребности тканей, в том числе при нагрузке. ХСН рассматривается как исход различных заболеваний сердца, она характеризуется истощением резервных возможностей миокарда и системных компенсаторных механизмов.
Клинически у больного обычно присутствуют:
1) жалобы, типичные для ХСН (одышка в покое или при нагрузке, слабость, утомляемость, сердцебиения, отеки);
2) данные объективного исследования, присущие сердечной недостаточности (тахикардия, тахипноэ, влажные хрипы в легких, плевральный выпот, повышение венозного давления, периферические отеки, гепатомегалия);
3) выявляемые при объективном и дополнительных обследованиях доказательства нарушений структуры и / или функции сердца (кардиомегалия, трехчленный ритм (галоп), аускультативные данные о врожденных / приобретенных пороках сердца, изменения при эхокардиографическом исследовании, свидетельствующие о структурно-функциональных нарушениях камер / клапанов сердца, повышение уровней натрийуретических гормонов).
Жалобы и данные объективного исследования при ХСН неспецифичны, что в ряде случаев затрудняет диагностику.
Эпидемиология
 Распространенность ХСН увеличивается с возрастом. Средний возраст при установлении диагноза ХСН в западных странах достигает 67-76 лет. В Украине (исследование UNIVERS, Л.Г. Воронков, 2012) и России (исследование ЭПОХА-О-ХСН) средний возраст больных ХСН составляет около 60 лет. По данным эпидемиологических исследований, ХСН имеется у 1 из 15 человек в возрасте >75 лет и у 1 из 7 – среди тех, возраст которых >85 лет. Распространенность ХСН в динамике увеличивается по мере старения населения (рост доли лиц пожилого возраста в структуре населения), а также по мере улучшения лечения артериальной гипертензии – АГ и ишемической болезни сердца – ИБС (все бόльшее число больных доживает до этапа ХСН).
Распространенность ХСН увеличивается с возрастом. Средний возраст при установлении диагноза ХСН в западных странах достигает 67-76 лет. В Украине (исследование UNIVERS, Л.Г. Воронков, 2012) и России (исследование ЭПОХА-О-ХСН) средний возраст больных ХСН составляет около 60 лет. По данным эпидемиологических исследований, ХСН имеется у 1 из 15 человек в возрасте >75 лет и у 1 из 7 – среди тех, возраст которых >85 лет. Распространенность ХСН в динамике увеличивается по мере старения населения (рост доли лиц пожилого возраста в структуре населения), а также по мере улучшения лечения артериальной гипертензии – АГ и ишемической болезни сердца – ИБС (все бόльшее число больных доживает до этапа ХСН).
Риск развития ХСН выше среди мужчин. В то же время, в связи с преобладанием женщин среди общей популяции пожилых лиц, доля женщин среди лиц с ХСН сравнима с таковой у мужчин или превышает ее. Смертность при ХСН остается высокой (по данным различных источников, за 5 лет погибают от 20-30 до 50% больных).
Фракция изгнания (фракция выброса) левого желудочка (ФИ ЛЖ)
и некоторые другие параметры структуры и функции ЛЖ
(данные эхокардиографии, табл. 1)
Определяемый в обычной клинической практике при эхокардиографическом исследовании показатель ФИ ЛЖ требует отдельного краткого обсуждения. Этот показатель является основным, применяемым в скрининговых целях для оценки систолической функции ЛЖ. Напомним, что в конце систолы ЛЖ его объем обозначается как конечно-систолический (он является наименьшим), в конце диастолы – как конечно-диастолический (наибольший). Разница между конечно-диастолическим и конечно-систолическим объемами определяется как ударный объем. Ударный объем показывает, какой объем крови изгоняется в ходе систолы ЛЖ. ФИ ЛЖ (табл. 1) показывает, какая часть конечно-диастолического объема изгоняется левым желудочком в ходе систолы. Уровень ФИ ЛЖ имеет практическую важность для выделения вариантов ХСН и для оценки прогноза больных с ХСН, ИБС и ряда других категорий больных сердечно-сосудистого профиля. В таблице 1 представлены некоторые важные для практикующего врача нормальные значения эхокардиографических показателей.
Таблица 1. Нормальные значения эхокардиографических показателей
|
Ударный объем ЛЖ (мл) ФИ ЛЖ = —————————————————————- х 100 % Конечно-диастолический объем ЛЖ (мл) |
Нормальные значения:
|
Принято разделять ХСН на стадии (по Н. Стражеско и В. Василенко), функциональные классы (Нью-Йоркская классификация – NYHA) и варианты (устанавливаются при наличии эхокардиографических данных о значении ФИ ЛЖ).
Стадии ХСН:
- I стадия: возникающие при умеренной физической нагрузке синусовая тахикардия и одышка, которые выражены резче и дольше, чем у здорового человека, выполняющего такую же работу.
- II A стадия: помимо усиления тахикардии и одышки появляются акроцианоз, застойные влажные хрипы в нижних отделах обоих легких, умеренное увеличение печени, отечность на стопах и лодыжках обеих ног, эти явления нарастают к концу дня, но исчезают после ночного отдыха.
- II Б стадия: интенсивная одышка беспокоит даже при небольшом физическом или эмоциональном напряжении; появляется ортопноэ, в легких сохраняются признаки хронического венозного застоя, влажные хрипы приобретают стойкий и более распространенный характер, расширяются яремные вены, печень отчетливо увеличивается и становится плотной, отеки распространяются на голени, бедра, определяется выпот в правой плевральной полости (гидроторакс); все эти признаки сохраняются после ночного отдыха, но могут несколько уменьшаться.
III стадия: тяжелая одышка в покое, ортопноэ, ночные пароксизмы удушья (кардиальная астма), интерстициальный и альвеолярный отек легких, правосторонний гидроторакс, гидроперикард, резкое расширение яремных вен, гепатомегалия, анасарка, асцит, выраженная олигурия.
Функциональные классы (ФК) ХСН:
- ФК I – пациенты с заболеванием сердца, у которых выполнение обычной физической нагрузки не вызывает одышки, усталости, сердцебиения.
- ФК II – пациенты с заболеванием сердца и умеренным ограничением физической активности. Одышка, усталость, сердцебиение наблюдаются при выполнении обычной физической нагрузки.
- ФК III – пациенты с заболеванием сердца и выраженным ограничением активности. В покое жалобы отсутствуют, но даже при незначительных физических нагрузках возникают одышка, усталость, сердцебиение.
- ФК IV – пациенты с заболеванием сердца, у которых любой уровень физической активности вызывает вышеперечисленные субъективные симптомы. Последние возникают и в покое.
- С систолической дисфункцией ЛЖ: ФИ ЛЖ ≤ 45%. Для установления этого варианта требуется наличие: (1) жалоб и (2) объективных данных, присущих ХСН; (3) подтвержденного снижения ФИ ЛЖ.
- С сохраненной фракцией выброса ЛЖ: ФИ ЛЖ > 45%. Для установления этого варианта требуется наличие: (1) жалоб и (2) объективных данных, присущих ХСН; (3) подтвержденного несниженного или незначительно сниженного уровня ФИ ЛЖ при отсутствии дилатации ЛЖ; (4) наличия гипертрофии ЛЖ / дилатации левого предсердия и/или эхокардиографических данных о наличии диастолической дисфункции (предпочтительна тканевая допплерография).
Этиология ХСН
Наиболее частыми причинами являются ИБС и АГ. Кроме того, к развитию ХСН приводят также: поражения клапанов сердца, перикарда, кардиомиопатии (в т.ч. вследствие действия алкоголя, антрациклиновых препаратов), миокардиты, нарушения ритма сердца (фибрилляция предсердий). Более редкими причинами являются саркоидоз, амилоидоз. При анемии, тиреотоксикозе может развиваться «ХСН с высоким сердечным выбросом».
Жалобы и объективные данные. Диагностика
Характерными для ХСН являются такие жалобы, как одышка, слабость, утомляемость, сердцебиение, отеки. Все эти симптомы неспецифичны. Данные объективного исследования при ХСН также неспецифичны; они могут включать: (1) изменения пульса: тахикардию, пульс может быть низкой амплитуды (малый), нерегулярный; (2) отечный синдром: увеличение массы тела, периферические отеки, отеки поясницы, отеки полостей, кардиальная астма, отек легких; (3) изменения со стороны органов дыхания: тахипноэ, влажные хрипы в легких, плевральный выпот; (4) изменения со стороны сердечно-сосудистой системы: расширение границ сердца, ритм галопа, аускультативная мелодия, свидетельствующая о наличии пороков сердца; (5) абдоминальные проявления: гепатомегалию, асцит. Считаем важным привести здесь перечень состояний, которые могут приводить к образованию отеков нижних конечностей (кроме ХСН): (1) прием нестероидных противовоспалительных препаратов, амлодипина; (2) хроническая венозная недостаточность (часто в сочетании с трофическими изменениями кожи); (3) острый тромбофлебит; (4) гипоальбуминемия (нарушения питания, повышенные потери белка через желудочно-кишечный тракт, нарушения всасывания – синдром мальабсорбции, нефротический синдром, сепсис); (5) нарушения лимфооттока (опухоли, лимфоаденопатия малого таза). Отметим, что у пациента с отеками всегда следует помнить о возможности тромбоза глубоких вен (особенно при асимметрии отеков)!
Обратим внимание практикующего врача на то, что ХСН не является нозологической единицей. Термин «ХСН» никогда не должен являться единственным диагнозом. Лабораторные и инструментальные исследования имеют целью установление причины ХСН, особенностей поражения сердца, прогноза.
 Стандартными лабораторными методами исследования у пациента с предположением о наличии ХСН являются: общеклинический анализ крови, глюкоза, креатинин (с подсчетом скорости клубочковой фильтрации), билирубин, трансаминазы, общий белок и фракции, электролиты, липиды, исследование функции щитовидной железы, общий анализ мочи, суточные потери белка.
Стандартными лабораторными методами исследования у пациента с предположением о наличии ХСН являются: общеклинический анализ крови, глюкоза, креатинин (с подсчетом скорости клубочковой фильтрации), билирубин, трансаминазы, общий белок и фракции, электролиты, липиды, исследование функции щитовидной железы, общий анализ мочи, суточные потери белка.
Обязательным является электрокардиографическое исследование, при котором у пациента с ХСН могут выявляться: (1) изменения, возможные при ИБС (зубец Q, отсутствие нарастания зубца R в грудных отведениях, изменения ST/T); (2) нарушения проводимости (атриовентрикулярные блокады, блокады ножек пучка Гиса); (3) нарушения ритма (особенно фибрилляция / трепетание предсердий, желудочковые аритмии); (4) гипертрофии отделов сердца.
Рентгеновское исследование органов грудной клетки должно быть проведено всем пациентам с предполагаемой ХСН. Могут выявляться кардиомегалия, признаки задержки жидкости (проявления интерстициального или альвеолярного отека легких, линии Керли, плевральный выпот). Следует обратить внимание на то, что при нормальных данных электрокардиографического и рентгеновского исследования диагноз СН маловероятен!
Отдельного краткого упоминания заслуживает такой достаточно новый для отечественных клиницистов, но стремительно занявший существенную позицию в диагностике и прогнозировании сердечной недостаточности показатель, как мозговой натрийуретический пептид (BNP) или аминотерминальный фрагмент его предшественника (NT-proBNP). Оба эти параметра находят применение в диагностике и прогнозировании ХСН, они имеют примерно равную диагностическую и прогностическую ценность. Их уровни повышаются при увеличении напряжения стенок желудочков. Нормальные их значения у нелеченного больного делают диагноз сердечной недостаточности маловероятным. Особенно пригодны для дифференциальной диагностики сердечной недостаточности у больного с одышкой неясного происхождения (остро возникшей). Повышенные концентрации для сердечной недостаточности характерны, но не специфичны (также могут повышаться при тахикардии, гипоксемии, снижении функции почек у лиц в возрасте >70-75 лет). Оценка уровней BNP и NT-proBNP может быть использована для контроля ответа на лечение и для прогнозирования: (1) если лечение эффективно, то концентрации этих пептидов снижаются; (2) высокие уровни несмотря на проведение оптимальной терапии указывают на неблагоприятный прогноз.
Важнейшее место в диагностике ХСН занимает эхокардиографическое исследование, которое должно быть выполнено, при возможности, у каждого больного. Во многих случаях оно позволяет уточнить этиологию ХСН, определить особенности структуры, систолической и диастолической функции ЛЖ. Широко используется для оценки прогноза при ХСН. Используются следующие режимы эхокардиографии: (1) двухмерное трансторакальное исследование (оценка размеров камер сердца, толщины стенок, параметров глобальной и региональной (участки локальной диссинергии – гипокинезия, акинезия, дискинезия, аневризма) систолической функции ЛЖ, внутриполостные тромбы, изменения структуры клапанов, перикардиальные нарушения, особенности структуры миокарда (кальцификация, амилоидоз) и др.); (2) импульсная и постоянно-волновая допплерография, цветное допплеровское картирование (оценка особенностей интракардиальных потоков крови, функции клапанов, диагностика клапанных пороков, септальных дефектов, оценка трансмитрального кровотока для выявления нарушений наполнения ЛЖ); (3) тканевая допплерография (особенно рекомендуется для диагностики нарушений диастолической функции ЛЖ).
Прочие инструментальные методы исследования могут выполняться, если несмотря на проведение перечисленных выше методов исследования диагноз остается недостаточно ясным. Так, магнитно-резонансная томография высокоинформативна в оценке структуры и систолической функции ЛЖ (она может плохо переноситься пожилыми из-за клаустрофобии; может быть противопоказана у лиц с имплантированными устройствами – водители ритма, протезы суставов и др.). Радионуклидное сканирование (особенно ценно для диагностики жизнеспособного (гибернированного) миокарда при наличии участков региональной диссинергии). Катетеризация сердца с вентрикулографией информативна в оценке особенностей поражений камер сердца, но является инвазивным подходом, требует введения рентген-контрастных веществ.
ХСН с сохранной фракцией изгнания ЛЖ
Этот вариант ХСН диагностируется при наличии: (1) жалоб и (2) объективных данных, присущих ХСН; (3) подтвержденного несниженного или незначительно сниженного уровня ФИ ЛЖ при отсутствии дилатации ЛЖ; (4) наличия гипертрофии ЛЖ / дилатации левого предсердия и/или эхокардиографических данных о наличии диастолической дисфункции (предпочтительна тканевая допплерография).
Среди больных с клиническими проявлениями ХСН около 50% имеют этот ее вариант, она более часто проявляется у пожилых лиц и у женщин.
ХСН с сохранной ФИ ЛЖ характеризуется достаточно неблагоприятным прогнозом. Сердечно-сосудистая смертность, не связанная с декомпенсацией сердечной недостаточности, у этих больных выше, чем при ХСН со сниженной систолической функцией ЛЖ (внутригоспитальная смертность составляет около 3%, смертность в течение года – 22-29%, в течение 5 лет – до 65%). У таких больных часто имеются сопутствующие состояния, которые увеличивают степень сердечно-сосудистого риска (АГ – более чем у 70%, ИБС – у 30-50%, фибрилляция / трепетание предсердий – у 30-40%, сахарный диабет 2 типа – у 35-50%, хроническое поражение почек – у 25%, церебро-васкулярное поражение – у 15%).
В настоящее время нет лечебных подходов, которые бы в масштабных рандомизированных контролируемых исследованиях при ХСН с сохранной ФИ ЛЖ отчетливо показывали бы улучшение сердечно-сосудистого прогноза (так, в нескольких крупных исследованиях применение ингибиторов АПФ, сартанов, а также антагонистов минералокортикоидных рецепторов существенного позитивного влияния на «первичную конечную точку» у лиц с этим вариантом ХСН не оказало) .
Ключевые моменты в лечении – (1) настойчивый контроль АД на уровне целевых значений (обычно применяют ингибитор АПФ / сартан блокатор кальциевых каналов (в т.ч. ЧСС-снижающие – верапамил, дилтиазем) диуретик) и (2) контроль частоты ритма у лиц с фибрилляцией предсердий. Для уменьшения отечного синдрома и застоя в легких могут применяться диуретики (обычно с бόльшей осторожностью, чем при ХСН с систолической дисфункцией ЛЖ). У больных с выраженным аортальным стенозом и тяжелой гипертрофией ЛЖ протезирование аортального клапана приводит к обратному развитию гипертрофии ЛЖ и уменьшает выраженность симптомов ХСН. У лиц с атеросклеротическими сосудистыми поражениями важная роль отводится вторичной профилактике с использованием стандартных изменений образа жизни, приемом небольших доз аспирина и статинов.
Лечение ХСН с систолической дисфункцией ЛЖ
Некоторые аспекты патофизиологии ХСН с систолической дисфункцией ЛЖ. Роль дефицита энергии и метаболических факторов
Для более четкого понимания излагаемых ниже вопросов лечения больных с систолической дисфункцией ЛЖ позволим себе кратко указать на некоторые аспекты ее патогенеза. Детальное рассмотрение вопросов патогенеза этого состояния выходит за пределы настоящего семинара. Здесь мы лишь перечислим важнейшие этапы той последовательности событий, которые от момента действия повреждающего фактора (например, перенесенного инфаркта миокарда, действия вирусной инфекции или токсина) приводят к формированию клинически явной ХСН. Важнейшее значение в процессе становления и развития нарушений систолической функции ЛЖ придается его ремоделированию (т.е. структурно-функциональному преобразованию). При этом развивается сложный комплекс изменений биологии миокардиоцитов (гипертрофия, нарушения функции саркоплазматического ретикулума, изменения сократительных и регуляторных протеинов, цитоскелета и рецепторного аппарата, систем микроРНК и др.), ускоряется их гибель (некроз, апоптоз, аутофагия), происходят разноплановые изменения в интерстиции миокарда (нарушения функции кардиальных фибробластов, дефекты системы матриксных металлопротеиназ, нарушения образования и метаболизма коллагенового матрикса миокарда). Ассоциированные с этими процессами изменения геометрии ЛЖ (приобретение им формы, близкой к сферической взамен эллиптоидной, дилатация, повышение напряжения стенок) способствуют снижению эффективности его сокращения.
Следует подчеркнуть высокую важность нарушений энергетики миокардиоцитов в развитии перечисленных выше многоступенчатых преобразований. Ключевыми моментами здесь являются связанные с мальадаптивной (т.е. патологической) гипертрофией миокардиоцитов повышение потребления и снижение продукции высокоэнергетических фосфатов (аденозинтрифосфата – АТФ), что определяет формирование и прогрессирование энергетического дефицита. Именно этот энергетический дисбаланс является мощным стимулом указанных выше изменений сократительного аппарата и саркоплазматического ретикулума (SERCA2a) миокардиоцитов и, в конечном итоге, их гибели. Дефицит продукции и утилизации энергии лежит в основе нарушений как систолической, так и диастолической функции ЛЖ (напомним читателю, что процесс расслабления миокарда является энерго-затратным и требует расхода АТФ).
На последующих этапах развития ХСН происходит ряд изменений нейрогуморальных систем (включая ренин-ангиотензин-альдостероновую, симпатическую и др.), что, в свою очередь, стимулирует формирование многообразных изменений в периферическом сосудистом русле, почках и, наконец, к реализации знакомых нам клинических проявлений ХСН.
Общий взгляд на лечебную тактику.
Самоконтроль пациента. Изменения образа жизни
Лечение больных с ХСН с систолической дисфункцией ЛЖ – актуальнейшая задача современной кардиологии. Во многих серьезных исследованиях показано, что возможности современной лечебной стратегии у таких больных весьма высоки. Далее мы будем рассматривать лечение именно этого варианта ХСН, ввиду чего сочли возможным воздержаться от постоянного указания на термин «ХСН с систолической дисфункцией ЛЖ», но вместо него ограничиться термином «ХСН».
Лечение больного с ХСН складывается из изменений образа жизни, медикаментозных лечебных подходов и высокотехнологичных не-медикаментозных подходов (ресинхронизация, имплантируемый кардиовертор-дефибриллятор и др.).
В 2014 г. эксперты Американской Ассоциации Сердца опубликовали весьма важные, на наш взгляд, рекомендации по самоконтролю при ХСН; в них врачу предписывается обсудить с пациентом / его родственниками ряд вопросов, необходимых для повышения эффективности лечебной программы. Мы сочли важным привести эти рекомендации в сокращенном виде (рис. 1).

Рисунок 1. Рекомендации для пациента с ХСН, предложенные экспертами США в 2014 г.
Примечания: стрелка вверх – повысить, повышение; стрелка вниз – снизить, снижение. Комментарии – в тексте.
С пациентом следует обсудить стратегию лечения в целом (его цели, возможные результаты), порекомендовать подходы, помогающие не забыть принять препараты (использование контейнера для таблеток, настройка соответствующего сигнала в смартфоне, прием лекарств после какого-то очень привычного и стандартного действия, например, после чистки зубов и др.).
Вне декомпенсации ХСН считают достаточным умеренное ограничение приема жидкости (≤ 1,5–2,0 л/сут.), но в случаях декомпенсации это ограничение должно быть более жестким (возможно, ≤ 1,0–1,5 л/сут.).
Очень большое значение придают рекомендации по ограничению в рационе поваренной соли. Указывают, что без четкого и действительно жесткого уменьшения приема соли не будет успешным проведение диуретической терапии – уже через небольшой промежуток времени после ее начала будет развиваться диуретическая резистентность. С учетом этого, вопрос об ограничении соли (нужно рекомендовать убрать со стола солонку, недосаливать пищу при приготовлении, затем – не присаливать ее) должен обсуждаться с больным настойчиво, с разъяснением, на каждом визите.
Первостепенное значение (особенно для успеха лечения диуретиками и бета-адреноблокаторами) имеет рекомендация по самоконтролю массы тела (обычно – с помощью напольных весов) с ведением дневника. В такой дневник также рекомендуют вносить и иные показатели – уровни артериального давления, частоты пульса, возможно – количество выпитой и выделенной жидкости (некоторым больным полезно порекомендовать вносить в дневник данные о гликемии, уровнях гемоглобина, креатинина, показателей функции щитовидной железы и др.).
Следует сориентировать пациента на необходимость постоянного самоконтроля своего состояния / самочувствия. Рекомендуют регулярно (каждодневно) оценивать степень выраженности одышки, слабости, отеков (возможно, с отражением в плюсах в том же дневнике). Нужно объяснять, что в случае нарастания подобных проявлений их не следует пытаться устранить самостоятельно – значительно более эффективным и безопасным будет безотлагательное обращение за помощью к специалисту. Желательно подчеркнуть, что небольшое усиление лечения, достаточное для устранения этих изменений на раннем этапе, может позволить предотвратить развитие декомпенсации и связанной с нею госпитализации в стационар.
В условиях отечественной традиционной лечебной практики требует особого внимания указание экспертов на нежелательность использования любых фитотерапевтических лечебных подходов при ХСН (это же касается и многих других категорий сердечно-сосудистых пациентов, в частности, пост-инфарктных). Такая принципиальная позиция связана с (1) отсутствием каких-либо серьезных исследований, где подобные препараты способствовали бы улучшению сердечно-сосудистого прогноза; (2) высокой вероятностью непредсказуемых взаимодействий фитопрепаратов со стандартными медикаментозными средствами, применяемыми при ХСН.
Казалось бы, не требуют пространного комментария рекомендации по исключению курения (в т.ч. пассивного) и ограничению алкоголя. Все же, по поводу курения укажем на несколько моментов, на которые считают важным специально обратить внимание пациента (структура приводимых ниже фраз умышленно адаптирована для неспециалиста): (1) «табачный дым содержит наиболее мощные из известных сейчас сосудистых ядов»; (2) «отказ от курения полезен в любом возрасте»; (3) «благоприятный эффект на здоровье от прекращения курения начинает сказываться уже через 2-4 недели, в полной мере он проявляется через год и более»; (4) «если курит один человек в семье, то нередко – «курит» вся семья».
Указанные на рисунке 1 дозы спиртного (не более 20 мл этанола в сутки для мужчин и не более 10 мл/сутки – для небеременных женщин) в настоящее время рассматриваются как «нейтральные» в отношении сердечно-сосудистой системы. Говорить о благоприятных эффектах на сосудистое здоровье каких-либо видов алкогольных напитков эксперты пока считают преждевременным. Указывают, что если пациент не употребляет спиртное, врач не должен рекомендовать ему начать его употребление «для улучшения состояния сосудов». Напомним читателю о существовании хорошо очерченной и нередкой формы дилатационной кардиомиопатии – алкогольной кардиомиопатии, при которой (как и при алкоголизме в целом) прием любых количеств спиртного противопоказан. Алкоголь также не рекомендуют употреблять вовсе лицам с заболеваниями печени.
Обращаем внимание на рекомендацию пациенту по поводу тревоги и депрессии. Советуют разъяснить больному, что обсуждение особенностей своего настроения с врачом может быть весьма полезным. Врачу следует самому постараться деликатно задать соответствующие вопросы (здесь их не приводим – имеются специальные вопросники, к которым следует обратиться), провести анализ результатов и принять адекватное решение (корректировать самому или обратиться за помощью к консультанту). Например, среди антидепрессивных препаратов представитель группы селективных ингибиторов обратного захвата серотонина – сертралин – показал себя как эффективный и безопасный препарат в лечении депрессии у кардиологических пациентов (в т.ч. с ХСН). Нужно осознавать, что лечение депрессии самостоятельного благоприятного эффекта на прогноз при ХСН не оказывает, но может существенно улучшить приверженность пациента к лечению.
Малоизвестной отечественному клиницисту пока остается проблема храпа и тесно связанного с ним синдрома обструктивного апноэ во сне. Между тем, при наличии этого синдрома (следует обсудить с больным и его / ее супругом / супругой особенности дыхания во сне – паузы и храп) из-за гипоксемии может ухудшаться сердечно-сосудистый прогноз, в т.ч. при ХСН. В то же время, следует иметь в виду, что сейчас имеются вполне надежные возможности диагностики (сомнологическое обследование) и относительно доступные средства эффективного контроля подобных ситуаций (например, устройства, создающие положительное давление в верхних воздухоносных путях – СРАР).
Положительное влияние на симптоматику, переносимость физической нагрузки и гемодинамические показатели при ХСН оказывает выполнение регулярных физических нагрузок. Пациент должен быть информирован о том, что: (1) умеренные физические нагрузки на свежем воздухе рекомендуются при стабильном самочувствии, т.е. вне декомпенсации; (2) их регулярное выполнение полезно для сердца и сосудов; (3) объем нагрузок индивидуален, зависит от состояния больного и должен быть согласован с лечащим врачом (например, для относительно менее тяжелых пациентов это могут быть прогулки по 30-40 минут в день в умеренном темпе – не менее 5 дней в неделю, а лучше – ежедневно); (4) если объем нагрузки становится некомфортным из-за слабости / одышки или по иным причинам – нужно посоветоваться с врачом.
Регулярность визитов к врачу – обязательный раздел для обсуждения с пациентом. Следует нацелить его на то, что сложившийся обыденный взгляд на визит к врачу как на шаг, предпринимаемый «в крайнем случае», совершенно неверен. Нужно разъяснить, что регулярные визиты к врачу необходимы для подбора дозы препаратов (на начальном этапе такие визиты должны быть, вероятно, с частотой около 1 раза в 2-3 недели на протяжении 2-3 месяцев). В последующем визиты также должны быть регулярными – не реже чем 1 раз в 3-4 месяца, даже при стабильном самочувствии. Обратить внимание пациента на то, что значительно сложнее добиться улучшения самочувствия тогда, когда декомпенсация уже наступила, чем преодолеть с врачебной помощью небольшое увеличение слабости / одышки / отеков. «Предупреждение ухудшения – значительно эффективнее и безопаснее, чем его лечение».
Пациент с ХСН нередко имеет целый ряд сопутствующих состояний (например, сахарный диабет, хроническое заболевание почек и др.). Большое значение для успешного лечения ХСН имеет тщательный контроль за течением этих состояний. Нужно непременно обсудить с больным целевые уровни артериального давления (обычно – 130-139 / 80-89 мм рт.ст., ближе к нижней из этих границ), гликозилированного гемоглобина (чаще – < 7%, в части случаев – 7,0-8,0%), холестерина липопротеидов низкой плотности (для постинфарктных больных – обычно – < 1,8 ммоль/л). Следует также порекомендовать пациенту с ХСН: (1) исключение или максимальное ограничение приема нестероидных противовоспалительных препаратов; (2) исключение применения блокаторов кальциевых каналов (кроме амлодипина и фелодипина); (3) исключение приема ингибиторов фосфодиэстеразы-5 (силденафила и др.) в сочетании с нитратами; (4) ограничение приема глюкокортикоидов, альфа-адреноблокаторов, тиазолидиндионов (пиоглитазона).
В рекомендациях международных экспертов по лечению ХСН обязательным подходом (при отсутствии противопоказаний) считают проведение профилактических прививок, в первую очередь, против гриппа и пневмококка. В серьезных работах показано, что развитие при таких инфекциях респираторных заболеваний зачастую является провоцирующим фактором декомпенсаций при ХСН, способствует ускорению прогрессирования кардиальных нарушений и ухудшает прогноз. Проведение прививок способно сократить риск подобных респираторных инфекций и ассоциировано с уменьшением заболеваемости и смертности при ХСН. Этот вопрос также нужно обсудить с пациентом.
Медикаментозная терапия при ХСН (рис. 2)
На рисунке 2 представлены стратегические подходы к лечению обсуждаемой категории больных с ХСН. Как видно из рисунка, наряду с изменениями образа жизни, большинству пациентов будет требоваться назначение комбинации из 3 классов лекарственных препаратов: (1) блокатора ренин-ангиотензиновой системы (ингибитора АПФ либо сартана); (2) бета-адреноблокатора; (3) антагониста минералокортикоидных рецепторов. В добавление к ним при наличии признаков задержки жидкости к лечению добавляют диуретики. У лиц с фибрилляцией / трепетанием предсердий (а также у некоторых иных пациентов) для уменьшения риска тромбоэмболических осложнений используют пероральные антикоагулянты. Среди противоаритмических препаратов при ХСН предпочтительным является амиодарон. У части пациентов применяют также сердечные гликозиды (обычно дигоксин), статины (преимущественно у постинфарктных больных, ивабрадин (только при синусовом ритме). Определенное место в структуре медикаментозных подходов при ХСН отводится препаратам с метаболическим действием (в т.ч. Мельдонию – см. ниже в отдельном подразделе).
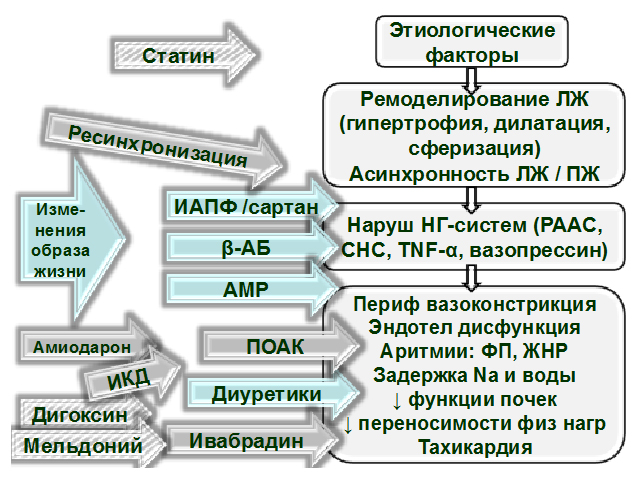
Рисунок 2. Стратегические подходы к лечению при ХСН с систолической дисфункцией левого желудочка
Примечания: ЛЖ – левый желудочек; ПЖ – правый желудочек; НГ – нейрогуморальный; РААС – ренин-ангиотензин-альдостероновая система; СНС – симпатическая нервная система; TNF – фактор некроза опухоли; ФП – фибрилляция предсердий; ЖНР – желудочковые нарушения ритма; ИАПФ – ингибитор ангиотензин-превращающего фермента; β-АБ – β-адреноблокатор; АМР – антагонист минералокортикоидных рецепторов; ПОАК – пероральный антикоагулянт; ИКД – имплантируемый кардиовертор-дефибриллятор.
Пояснения: Справа на рисунке – упрощенная схема патогенеза ХСН (на начальном этапе – действие этиологического фактора, например, инфаркта миокарда; затем ремоделирование ЛЖ, активация нейрогуморальных систем; далее – развитие клинических проявлений). Слева – лечебные подходы. Те из них, которые применяют практически у всех пациентов, указаны на светло-синем фоне; остальные – на сером фоне; подходы, рассматриваемые как важные дополнительные – на фоне серой штриховки (включая Мельдоний). Направление стрелки на схеме указывает точку приложения соответствующего лечебного подхода.
Для удобства восприятия информации по каждому из перечисленных лечебных подходов мы сочли возможным представить материал в виде отдельных подразделов, каждый из которых включает по 5 основных принципов их применения.
Основные принципы применения блокаторов ренин-ангиотензиновой системы (ингибиторов АПФ / сартанов) при ХСН с систолической дисфункцией ЛЖ
1. Кому и когда? Как ингибиторы АПФ, так и сартаны при ХСН в крупных исследованиях показали увеличение выживаемости. В силу этого они назначаются (при переносимости) каждому больному с систолической дисфункцией ЛЖ (при ФИ ЛЖ ≤ 45%), включая бессимптомных пациентов.
2. Какие препараты? Среди ингибиторов АПФ чаще используются эналаприл (стартовые и целевые дозы соответственно: по 1,25 мг 2 р/сут и по 10-20 мг 2 р/сут); лизиноприл (соответственно – 2,5 мг 1 р/сут и 20-35 мг 1 р/сут); рамиприл (соответственно – 1,25-2,5 мг 1 р/сут и по 5 мг 2 р/сут); периндоприл (соответственно – 2,5 мг 1 р/сут и 10 мг 1 р/сут). Среди сартанов могут применяться валсартан (соответственно – по 40мг 2 р/сут и по 160 мг 2 р/сут); кандесартан (соответственно – 4 мг 1 р/сут и 32 мг 1 р/сут); лозартан (соответственно – по 50 мг 1 р/сут и по 150 мг 1 р/сут).
3. Сколько? Чем доза этих препаратов выше (в пределах целевой), тем выше их благоприятное действие на прогноз. Начинать лечение рекомендуют с малых доз и постепенно их повышать (не реже чем 1 раз в 2 недели) в ходе титрования до целевой (или максимально переносимой в пределах целевой) дозы.
4. Как длительно? Прием должен быть длительным (неопределенно долгим).
5. Безопасность? (1) не рекомендуют сочетать ингибитор АПФ с сартаном; (2) у 10-15% больных при приеме ингибиторов АПФ развивается кашель, он нехарактерен для сартанов; (3) при применении препаратов обеих групп требуется контроль уровней креатинина (с подсчетом скорости клубочковой фильтрации) и калия.
Основные принципы применения β-адреноблокаторов (β-АБ) при ХСН с систолической дисфункцией ЛЖ
1. Кому и когда? β-АБ также улучшают прогноз при ХСН, что продемонстрировано в целом ряде серьезных исследований. Они должны быть назначены (при переносимости) каждому больному с систолической дисфункцией ЛЖ (при ФИ ЛЖ ≤ 45%), включая бессимптомных пациентов.
2. Какие препараты? Могут быть использованы: бисопролол (стартовые и целевые дозы соответственно – 1,25 мг 1 р/сут и 10 мг 1 р/сут); карведилол (соответственно – по 3,125 мг 2 р/сут и по 25-50 мг 2 р/сут); метопролола сукцинат (соответственно – 12,5-25 мг 1 р/сут и 200 мг 1 р/сут); небиволол (соответственно – 1,25 мг 1 р/сут и 10 мг 1 р/сут).
3. Сколько? Влияние β-АБ на сердечно-сосудистый прогноз при ХСН также тем лучше, чем выше доза. Начинать лечение рекомендуют с малых доз и постепенно их повышать (не реже чем 1 раз в 2 недели) в ходе титрования до целевой (или максимально переносимой в пределах целевой) дозы. Впрочем, даже самые небольшие дозы β-АБ (например, при невозможности их повышения ввиду гипотензии) способны существенно улучшать прогноз.
4. Как длительно? Прием β-АБ должен быть длительным (неопределенно долгим).
5. Безопасность? (1) в ходе титрования и постоянного приема β-АБ необходим контроль частоты сердечных сокращений (ЧСС), артериального давления (АД), массы тела; (2) при развитии у лиц, принимающих β-АБ, декомпенсации ХСН и/или умеренной гипотензии (систолическое АД не ниже 100 мм рт.ст.) следует постараться, при возможности, не отменять β-АБ (варианты тактики – уменьшение дозы нитратов, изменения доз ингибиторов АПФ и диуретиков, снижение дозы β-АБ); (3) помнить, что среди побочных эффектов β-АБ – брадикардия и бронхоспазм.
Основные принципы применения антагонистов минералокортикоидных рецепторов (АМР) при ХСН с систолической дисфункцией ЛЖ
1. Кому и когда? Ввиду того, что АМР улучшают прогноз при ХСН, их следует назначать (при переносимости) каждому больному с ХСН I-IV ФК с систолической дисфункцией ЛЖ (при ФИ ЛЖ ≤ 45%).
2. Какие препараты? Могут быть использованы: эплеренон или спиронолактон. У пациентов, перенесших инфаркт миокарда, предпочтителен эплеренон.
3. Сколько? Как эплеренон, так и спиронолактон с кардиопротекторной целью используются обычно в так называемых «недиуретических» дозах – 25-50 мг/сут. Полагают, что более высокая доза лучше влияет на прогноз (повышают с 25 до 50 мг/сут примерно через 1 месяц лечения). При уровнях калия 5,5-5,9 ммоль/л, креатинина крови 150-200 мкмоль/л возможен прием эплеренона через день.
4. Как длительно? Прием АМР должен быть длительным.
5. Безопасность? (1) до начала и в процессе лечения требуется контроль уровней калия и креатинина крови; (2) не применять при скорости клубочковой фильтрации < 30 мл/мин, при уровнях калия крови ≥ 6,0 ммоль/л; (3) применение неселективного АМР спиронолактона может быть ассоциировано с развитием гинекомастии, дисменореи, снижения либидо; эти эффекты нехарактерны для селективного АМР эплеренона.
Основные принципы применения диуретиков при ХСН с систолической дисфункцией ЛЖ
1. Кому и когда? Данные о благоприятном влиянии диуретиков на прогноз при ХСН не представлены. Диуретики применяются у лиц с ХСН, имеющих признаки задержки жидкости в организме (периферические отеки, отеки полостей, кардиальная астма), а также при угрозе такой задержки. Они широко используются и у больных с декомпенсацией ХСН. У лиц, не имеющих (и не имевших) отечного синдрома и проявлений легочного застоя, диуретики не применяют.
2. Какие препараты? Наиболее часто при ХСН используют петлевые диуретики (фуросемид, торасемид). На начальных этапах развития отечного синдрома могут применяться тиазидовые препараты (гидрохлоротиазид). Также могут назначаться и калийсберегающие (спиронолактон).
3. Сколько? Дозы для хронического приема: фуросемид чаще 20-40 мг/сут, возможно – 80 мг/сут и более – обычно на 2-3 приема; торасемид – 10-20 мг/сут, при необходимости – 40 мг/сут и более – обычно на 1-2 приема. Более высокие дозы петлевых диуретиков применяются чаще при сопутствующем снижении функции почек. Гидрохлоротиазид – 25-50 мг/сут. Диуретические дозы спиронолактона – 75-200 мг/сут.
4. Как длительно? Длительность и интенсивность диуретической терапии при ХСН зависят от особенностей задержки жидкости в организме больного. Даже после полного устранения отечного синдрома диуретики обычно не отменяют полностью, но, скорее, уменьшают их дозы. Таким образом, у пациентов с ХСН II-IV ФК диуретическая терапия должна быть длительной.
5. Безопасность? (1) в процессе лечения требуется контроль массы тела, водного баланса, ведение дневника; также важен контроль электролитов (калий, натрий), креатинина крови, гликемии; (2) при интенсивной диуретической терапии темп потери массы тела больного не должен быть более 0,5-1,0 кг/сут (такая терапия требует пребывания в стационаре); (3) при диуретической резистентности возможны: длительное внутривенное инфузионное введение петлевого диуретика (в дозе в 2-2,5 раза выше ранее применявшейся пероральной); комбинация петлевого диуретика с тиазидовым (эти подходы требуют особой осторожности, тщательного лабораторного контроля и врачебного наблюдения).
Основные принципы применения пероральных антикоагулянтов (ПОАК) при ХСН с систолической дисфункцией ЛЖ
1. Кому и когда? ПОАК применяются при ХСН для снижения риска тромбоэмболических осложнений у следующих категорий пациентов: с фибрилляцией / трепетанием предсердий (наиболее частое показание), с эпизодами тромбоэмболий ранее; с внутрисердечными тромбами; с клапанными протезами. ПОАК не используются у лиц без вышеперечисленных состояний.
2. Какие препараты? При всех упомянутых показаниях могут быть применены антагонисты витамина К (наиболее часто – варфарин, существенно реже – аценокумарол и фениндион). У лиц с неклапанными фибрилляцией / трепетанием предсердий альтернативу варфарину составляют новые ПОАК – ингибиторы Ха фактора свертывания ривароксабан и апиксабан, а также прямой ингибитор тромбина дабигатран.
3. Сколько? Начало терапии варфарином – обычно с дозы 5 мг/сут (у пожилых – 2,5 мг/сут), в дальнейшем дозу препарата подбирают с учетом уровней международного нормализующего отношения; его целевые уровни обычно составляют 2,0-3,0. Дозы новых ПОАК: (1) ривароксабан – стандартная – по 20 мг 1 раз в сутки во время еды, а при высоком риске кровоточивости, т.е. при уровне баллов по шкале HAS-BLЕD ≥ 3, а также при скорости клубочковой фильтрации 30-50 мл/мин – по 15 мг 1 раз в сутки; (2) дабигатран – стандартная – по 150 мг 2 раза в сутки, а у лиц в возрасте ≥ 80 лет, при HAS-BLЕD ≥ 3, а также при скорости клубочковой фильтрации 30-60 мл/мин – по 110 мг 2 раза в сутки.
4. Как длительно? У больных с фибрилляцией / трепетанием предсердий ПОАК следует использовать длительно (неопределенно долго). При иных перечисленных выше показаниях длительность их приема определяется врачом индивидуально (например, после первого тромбоэмболического эпизода – не менее 3 месяцев).
5. Безопасность? (1) при отсутствии возможности регулярно (не реже 1 раза в месяц) контролировать международное нормализующее отношение – лечение варфарином проводить нельзя; в таком случае это следует отразить в выводах врача, назначить альтернативный препарат (новый ПОАК, возможно – ацетилсалициловую кислоту или клопидогрель); (2) иметь в виду возможность широких взаимодействий варфарина с другими лекарственными препаратами и продуктами питания; (3) для новых ПОАК – обязательно информировать больного о крайней нежелательности пропусков их приема и о необходимости постоянно иметь запас препарата.
Основные принципы применения противоаритмических препаратов (ПАП) при ХСН с систолической дисфункцией ЛЖ
1. Кому и когда? Распространенность нарушений ритма сердца при ХСН весьма высока. Не менее 40% пациентов с ХСН имеют фибрилляцию предсердий. Внезапная смерть аритмического генеза, связанная с жизнеопасными желудочковыми нарушениями ритма является одной из основных причин смерти лиц с ХСН. С учетом этого, применение ПАП у больных с ХСН достаточно распространено.
2. Какие препараты? Среди ПАП при ХСН: (1) противоаритмики I класса ( прокаинамид, пропафенон), III класса (дронедарон) и IV класса (верапамил, дилтиазем) противопоказаны; (2) препараты II класса (бета-адреноблокаторы) используются широко (см. выше); (3) среди препаратов III класса амиодарон рассматривается сейчас как наиболее часто применяемый, эффективный и безопасный классический ПАП при любых ФК ХСН, а также при декомпенсации ХСН; соталол может быть применен при компенсированной ХСН I-II ФК.
3. Сколько? Выбор доз амиодарона и соталола определяется конкретной клинической ситуацией. Для амиодарона дозы в период пребывания в стационаре могут доходить до 1200 мг/сут, в последующем в течение 2-4 недель составлять по 600-400 мг/сут, затем – по 200-100 мг/сут. Соталол может применяться в дозах по 40-160 мг 2 раза в день.
4. Как длительно? Амиодарон и соталол при ХСН используются по мере необходимости; в ряде ситуаций их прием может быть длительным.
5. Безопасность? (1) при использовании ПАП требуется контроль ЧСС, продолжительности РQ, QRS, QT на ЭКГ, их использование не показано лицам с синдромом слабости синусового узла и атриоветрикулярными блокадами ≥ 2 степени (при отсутствии имплантированного кардиостимулятора); (2) для амиодарона – иметь в виду возможность развития нарушений функции щитовидной железы, воспалительных / фибротических поражений легких, нейропатии, пигментации кожи; (3) для соталола – в начале лечения требуется, чтобы больной не менее 3 дней находился в условиях стационара; возможно развитие брадикардии, бронхоспазма; не применять при декомпенсации ХСН и гипокалиемии.
Основные принципы применения ивабрадина при ХСН с систолической дисфункцией ЛЖ
1. Кому? Ивабрадин (блокатор f-каналов синусового узла) улучшает прогноз у лиц с ХСН ишемического и неишемического происхождения II-III ФК с ФИ ЛЖ < 35% при синусовом ритме с ЧСС > 70 в минуту, удерживающейся несмотря на титрование бета-адреноблокаторов. У такой категории больных его и следует применять.
2. Когда? Ивабрадин обычно добавляют к бета-адреноблокаторам (или используют вместо них при их непереносимости). Следует иметь в виду, что у лиц с сопутствующей стабильной стенокардией ивабрадин может оказывать самостоятельный антиангинальный эффект.
3. Сколько? Начальная доза – по 5 мг 2 раза в день; под контролем ЧСС ее можно увеличить до 7,5 мг 2 раза в день.
4. Как длительно? Ввиду способности улучшать прогноз препарат при ХСН может использоваться длительно.
5. Безопасность? Переносится обычно достаточно хорошо; в ходе лечения требуется контроль ЧСС, т.к. препарат может вызывать развитие чрезмерной брадикардии.
Основные принципы применения сердечных гликозидов при ХСН с систолической дисфункцией ЛЖ
1. Кому и когда? Сейчас многими экспертами рассматриваются как дополнительный лечебный подход при ХСН с систолической дисфункцией ЛЖ (однако до 40% таких больных, по данным регистров США и Европы, их принимают). Показаны лицам с ФИ ЛЖ < 40-45% следующих категорий: (1) с фибрилляцией предсердий при тахисистолии желудочков – с целью урежения желудочкового ритма – обычно в добавление к бета-адреноблокаторам, либо вместо них, при противопоказаниях к их применению (например, при гипотензии); (2) при синусовом ритме – если несмотря на применение ингибиторов АПФ / сартанов, бета-адреноблокаторов, АМР и диуретиков у больного еще удерживаются клинические проявления ХСН.
2. Какие препараты? Наиболее часто применяется дигоксин; альтернативой ему может быть дигиланид. Во многих странах мира такие препараты, как строфантин и коргликон не рекомендованы к применению и устранены из лечебной практики ввиду высокого риска развития гликозидной интоксикации.
3. Сколько? Обычные начальные и поддерживающие дозы дигоксина – 0,25 мг/сут (а у пожилых лиц и при сниженной функции почек – 0,125 мг/сут или даже через день). При фибрилляции предсердий с тахисистолией желудочков могут быть применены дозы 0,375-0,5 мг/сут, но обычно – непродолжительное время. Использование режимов ускоренной дигитализации не рекомендуется (в зарубежных странах это считают возможным только под контролем сывороточных концентраций дигоксина и в условиях, когда имеются современные средства лечения гликозидной интоксикации – антидигоксиновые антитела (точнее – Fab-фрагменты антител), что отсутствует в арсенале отечественного клинициста).
4. Как длительно? Продолжительность применения дигоксина при ХСН определяется врачом; у некоторых больных оно может быть длительным.
5. Безопасность? Наиболее важным побочным эффектом является гликозидная интоксикация (однако при использовании указанных выше доз и при отсутствии гипокалиемии она развивается нечасто). Требуется контроль ЧСС, электрокардиограммы, уровней калия крови, самочувствия.
Основные принципы применения статинов при ХСН с систолической дисфункцией ЛЖ
1. Кому и когда? Статины не представляют собой стандартный элемент лечебной стратегии при ХСН, однако они находят применение у постинфарктных пациентов с ХСН для уменьшения риска развития повторных инфарктов миокарда. Статины не назначают при неишемической этиологии ХСН. Их также не применяют при ХСН IV ФК.
2. Какие препараты? Наиболее распространенными статинами (в т.ч. при ХСН) сейчас являются аторвастатин и розувастатин.
3. Сколько? Выбор дозировки статина зависит от степени коронарного риска (у больного, недавно перенесшего инфаркт миокарда, она должна быть более высокой, например, аторвастатина – 40-80 мг/сут), возраста больного, состояния функции почек и печени, уровня холестерина липопротеидов низкой плотности.
4. Как длительно? Прием статина у постинфарктного (и постстентового) больного должен быть длительным. Его обычно прекращают при развитии ХСН ФК IV / кахексии.
5. Безопасность? (1) при приеме статинов требуется контроль уровней аминотрансфераз (АСТ, АЛТ), билирубина, самочувствия пациента (мышечная боль?); (2) наличие у пациента нарушенной толерантности к глюкозе или явного сахарного диабета не требует коррекции дозировок статина.
Возможности применения Мельдония при ХСН с систолической дисфункцией ЛЖ
Применение препаратов с метаболическим действием (например, Мельдония) у лиц с ХСН обычно играет вспомогательную роль; такие лекарственные средства назначаются обычно в дополнение к стандартной лечебной программе, включающей, как говорилось выше, для большинства больных – ингибитор АПФ или сартан бета-адреноблокатор антагонист минералокортикоидных рецепторов диуретик. Использование Мельдония в комплексном лечении подобных пациентов, по данным ряда авторов, способно обеспечить ряд позитивных эффектов на самочувствие больного, а также на клинико-лабораторные и инструментальные параметры.
О механизме действия Мельдония достаточно подробно говорилось в недавно представленном семинаре по лечению больных с ИБС. Здесь мы позволим себе лишь напомнить о некоторых особенностях его действия, представляющих ценность в лечении рассматриваемой здесь категории пациентов, а также остановиться на возможностях использования препарата при ХСН.
Выше упоминалось о важности хронического дефицита энергетического баланса миокардиоцитов при ХСН с систолической дисфункцией ЛЖ. Именно этот аспект патогенеза миокардиальных нарушений, присущих ХСН, и является мишенью для действия Мельдония. Применяется он, главным образом, при ХСН ишемического генеза (т.е. у лиц с хронической ишемической болезнью сердца с ХСН, в т.ч. у постинфарктных). В основе позитивных влияний на энергетический дисбаланс миокардиоцитов лежит его свойство снижать биосинтез карнитина с последующим переключением метаболизма клеток на более эффективный и экономный путь метаболизма – гликолиз. Кроме того, уменьшение под влиянием Мельдония карнитин-зависимого поступления длинноцепочечных свободных жирных кислот (СЖК) в митохондрии обеспечивает снижение интенсивности β-окисления СЖК без перегрузки митохондрий недоокисленными жирными кислотами, и без нарушения их нормального функционирования. Важной особенностью действия препарата является то, что он улучшает транспорт АТФ внутри миокардиоцитов. Мельдоний оказывает также целый ряд цитопротекторных эффектов, включая антиоксидантные, антигипоксические, позитивное влияние на систему NO (с развитием вазодилататорных эффектов), снижение инсулинорезистентности.
Комплекс перечисленных выше позитивных эффектов Мельдония на энергетику миокардиоцитов в сочетании с его цитопротективным действием определяет следующие благоприятные эффекты препарата при ХСН (по данным работ Бойцова С.А. и соавт; Воронкова Л.Г.; Гейченко В.П.; Дзерве В.Я., Калвиньш И.Я.; Недошивина А.О. и соавт.; Сергиенко И.В. и соавт; Стаценко М.Е. и соавт.; Шабалина А.В. и соавт, и др.) – см. также рис. 3: (1) замедление постинфарктного ремоделирования ЛЖ; (2) улучшение переносимости физической нагрузки; (3) снижение функционального класса ХСН; (4) улучшение качества жизни; (5) повышение фракции изгнания ЛЖ; (6) улучшение функции эндотелия; (7) улучшение каротидных барорефлексов; (8) благоприятные эффекты на периферическое кровообращение. Важно отметить, что благоприятные эффекты препарата при ХСН продемонстрированы в том числе у больных с сахарным диабетом, метаболическим синдромом, у лиц пожилого возраста.

Рисунок 3. Возможности применения Мельдония при ХСН
Примечание: СД – сахарный диабет; МС – метаболический синдром
Назначают Мельдоний при ХСН обычно в дозе 750-1000 мг/сут (т.е. 3-4 таблетки в сутки), продолжительность лечения определяется врачом индивидуально, она может достигать 2-3 месяцев. В течение года возможно проведение нескольких подобных курсов лечения. Переносимость препарата обычно хорошая, что в сочетании с благоприятными эффектами на самочувствие пациентов и переносимость физических нагрузок определяет высокую приверженность пациентов к лечению.
Высокотехнологичные немедикаментозные методы лечения ХСН (кардиальная ресинхронизация, имплантируемые кардиоверторы дефибрилляторы)
Обычно говорить о показаниях к применению этих весьма дорогих лечебных подходов можно у лиц с ХСН ФК II-IV при выраженном снижении систолической функции ЛЖ (т.е. при уровнях ФИ ЛЖ ≤ 30-35%), которое удерживается несмотря на использование оптимального медикаментозного лечения, если ожидаемая продолжительность жизни больного составляет >1 года при относительно удовлетворительном функциональном состоянии пациента. Для кардиальной ресинхронизации будут подходить пациенты, имеющие уширение комплекса QRS на электрокардиограмме ≥ 120 мс (и, особенно, ≥ 150 мс). Отбор больных для такого лечения проводится кардиологом.
В заключение обсуждения темы ХСН необходимо отметить, что корректная диагностика и выбор адекватной лечебной программы, в соответствии с принятыми в мировой практике Рекомендациями, являются основой современной стратегии для этих пациентов. Важны тщательная эхокардиографическая оценка, регулярный контроль лабораторных параметров, тесный контакт с пациентом, обсуждение с ним и родственниками вопросов терапевтической тактики и приверженности к лечению. Врачу следует быть настойчивым в разъяснении необходимости соответствующих изменений образа жизни. При назначении медикаментозной терапии приоритетное место нужно отводить ингибиторам АПФ / сартанам, бета-адреноблокаторам и антагонистам минералокортикоидных рецепторов; особое внимание уделять титрованию их дозировок. Для части пациентов ценным дополнением к лечебной программе может явиться назначение препарата с метаболическим действием, например Мельдония.









