Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "Гастроэзофагеальная рефлюксная болезнь: сопоставительная оценка эффективности и безопасности омепразола в комбинации с домперидоном, в сравнении с омепразолом"
Автор: Мараховский К,Ю. 2, Василевская С.А. 1, Карасева Г.А. 1, Уласевич Д.Н. 1 , Мараховский Ю.Х.1
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Гастроэнтерология, Семейная медицина/Терапия
Просмотров: 2 327
Дата проведения:
 Патофизиология гастроэзофагеальной рефлюксной болезни (ГЭРБ) мультифакториальна и сопровождается сложными взаимоотношениями расстройств моторики эзофагогастродуоденальной зоны, но с обязательным агрессивным воздействием рефлюксанта (содержимого в пищеводе, появившегося как результат рефлюкса) и степенью его агрессивности, способностью пищевода к клиренсу (самоочищению), степенью резистентности слизистой пищевода к рефлюксанту, вкладом расстройств нижнего пищеводного сфинктера.
Патофизиология гастроэзофагеальной рефлюксной болезни (ГЭРБ) мультифакториальна и сопровождается сложными взаимоотношениями расстройств моторики эзофагогастродуоденальной зоны, но с обязательным агрессивным воздействием рефлюксанта (содержимого в пищеводе, появившегося как результат рефлюкса) и степенью его агрессивности, способностью пищевода к клиренсу (самоочищению), степенью резистентности слизистой пищевода к рефлюксанту, вкладом расстройств нижнего пищеводного сфинктера.
По определению Монреальского консенсуса (2006 г.), ГЭРБ – это состояние, при котором рефлюкс желудочного содержимого обуславливает причиняющие беспокойство симптомы и/или осложнения (рефлюкс-эзофагит, кровотечение, стриктуры, эзофагит Барретта, аденокарциному) [1].
При этом у большинства пациентов именно изжога и является тем «причиняющим беспокойство симптомом», который заставляет принимать какие-либо меры самостоятельно или обращаться за медицинской помощью.
ГЭРБ является одним из наиболее частых заболеваний органов пищеварения. Ее распространенность достигает 13-29% в США, 17% – в Швеции, 10% – в Великобритании и Испании [2].
Проявления ГЭРБ оказывают существенное влияние на психологическое самочувствие пациентов и уменьшают психологические показатели качества жизни. Опубликована серия работ, в которых показано, что ГЭРБ оказывает существенное негативное воздействие на психологические показатели качества жизни, более негативные, чем артериальная гипертензия и стенокардия. Так на основании анализа унифицированного индекса психологического благополучия(Psychological General Well Being (PGWB)) было показано, что у пациентов с ГЭРБ в сочетании с эзофагитом индекс значительно ниже, чем в общей сравниваемой популяции, и этот индекс у данной группы пациентов ниже по сравнению с группой пациентов со стенокардией. Аналогичные данные опубликованы по влиянию ГЭРБ без эзофагита на показатели качества жизни. Учитывая существенное воздействие проявлений ГЭРБ на психологические показатели качества жизни, можно утверждать, что точный своевременный диагноз и эффективное лечение являются существенным императивным социальным фактором для врачей всех специальностей по овладению и адекватному использованию диагностических приемов данного заболевания.
Тактика медикаментозного лечения ГЭРБ основана на рекомендациях по применению, прежде всего, ингибиторов протонной помпы(ИПП), как лекарственных средств, которые доказанно превосходят другие варианты медикаментозного лечения[3].
В ряде публикаций показано, что все ИПП имеют сопоставимые показатели по эффективности при ГЭРБ [4–10].
Начиная с 2005г. стали обсуждать рефрактерность ГЭРБ к ИПП. Рефрактерными считаются пациенты с ГЭРБ, у которых нет достаточной эффективности при лечении в течение 4-8 недель, доля таких пациентов колеблется от 20 до 40%. В числе причин рефрактерности обсуждаются следующие: неправильная верификация ГЭРБ (имеется функциональная диспепсия и т.д.), неадекватная доза ИПП и/или быстрый метаболизм ИПП, эозинофильный эзофагит, и т.д. [11, 12].
Частичный (неполный – рartialsymptom-response) ответ симтоматики при применении ИПП был оценен у 2645 пациентов с неэрозивной формой ГЭРБ и у 3151 с эрозивной [13]. Результаты показали, что частичный ответ на ИПП отмечается в 20% случаев c неэрозивной формой ГЭРБ, и у 14% при эрозивной.
Омепразол – классический ннгибитор протонного насоса, снижает кислотопродукциюза счет торможения активности Н+/К±АТФазы в париетальных клетках желудка и блокирует тем самым заключительную стадию секреции соляной кислоты. Из всех ИПП наибольшее число публикаций имеется именно по омепразолу. Порезультатом поиска по базе данных PubMed на 25.12.2012, за 10 лет опубликовано 896 клинических исследований по омепразолу, 209 обзоров, из которых 55 систематизированных и 22 мета-аналитических исследований. За пять лет – 524 клинических исследований, 24 систематизированных обзоров и 9 –мета-аналитических исследований. Как следует из этих публикаций, сопоставление омепразол 20мг/плацебо показывает NNT = 4, омепразол 40мг/плацебо дает те же значения NNT = 4 [14].
Японские авторы опубликовали в 2012г. результаты исследованияJ-FOCUS, в котором проведено сопоставление эффективности лечения симптомов со стороны верхних отделов ЖКТ омепразолом, фамотидином и мозапридом (прокинетик). Результаты этого рандомизированного контролируемого исследования в 162 центрах показали, что через 4 недели полное исчезновение изжоги отмечено в 28%, 10% и 6% в группах с омепразолом, фамотидином м мозапридом соответственно, частичное улучшение в этих группах было отмечено в 68%, 46% и 48%. Более того, авторы по симптомам выделили группу с ГЭРБ, и провели анализ эффективности в этой группе: омепразол был эффективен в 78%, фамотидин в 22%, мозаприд в 46% [15].
Наличие в патогенезе ГЭРБ изменений в координации моторики кардио-эзофагеальной зоны желудка и частое присутствие тошноты при ГЭРБ диктует необходимость включения в схемы ее терапии и препаратов из группы прокинетиков(гастрокинетиков). Среди прокинетеков наиболее часто используются домперидон (ДП).
Опубликованы результаты по эффективности лечения ГЭРБ ДП: всего 38 исследований, с общим числом пациентов – 467, средняя эффективность ДП по симптомам составила 86%, плацебо – 55%, по ликвидации эзофагита 65% на ДП и 60% на плацебо.
В 2000 году было опубликовано масштабное исследование по прокинетикам, в котором было указано, что общее число детей в Канаде и Великобритании, получивших лечение прокинетиками, составило более 50 тысяч, при этом была показана большая эффективность ДП (65-85%) по сравнению с метоклопрамидом при ГЭРБ [16].
В период 1995-2005гг. по ДП было опубликовано 1239 клинических исследований, из которых мета-аналитических -14. Анализ публикаций показывает наличие противоречивых результатов по оценке эффективности домперидона при ГЭРБ. В публикации 2003г. как раз и указывается на противоречивость результатов эффективности домперидона [17].
В соответствии с базой данных clinicaltrial.gov, имеется 30 зарегистрированных клинических исследований по домперидону на 5.02.2013, их них 3 напрямую касающихся ГЭРБ.
Одно из первых, мощных по выборке клинических исследований по эффективности сочетанного приема ИПП с прокинетиком при ГЭРБ опубликовано в 2008г. Результаты этого исследования позволили авторам сделать вывод о большей эффективности при ГЭРБ сочетанного приема ИПП с прокинетиком: эффективность составила 88% [18].
Фармацевтические компании стали производить лекарственную форму омепразола в комбинации с домперидоном.
Все вышеизложенное послужило основанием для проведения клинического исследования по сопоставительной оценки эффективности омепразола в комбинации с домперидоном, в сравнении с омепразолом.
Материал и методы
В соответствии утвержденной ГКНТ инициативной НИР кафедры гастроэнтерологии и нутрициологии БелМАПО, «Разработка вариантов рациональной фармакотерапии основных социально и демографически значимых заболеваний органов пищеварения» (госрегистрация: № 20130896 от 11.06.2013), этап 1 «Провести клиническое исследование по сопоставительной оценки эффективности омепразола и омепразола в сочетании с прокинетиком, при лечении гастроэзофагеальной рефлюксной болезни (ГЭРБ)», было проведено клиническое исследованиеомепразола в комбинации с домперидоном,в сравнении с омепразолом«Исследование рационального применения омепразола в комбинации с домперидоном при гастроэзофагеальной рефлюксной болезни легкой и средней степени тяжести».
Исследование проведено по программе (протоколу), утвержденному администрацией БелМАПО и одобренному этическим комитетом (комитетом по этике) БелМАПО протокол №2, от 17 октября 2013г.
Цель исследования
Определить эффективность и переносимость омепразола в сочетании с домперидоном при лечении ГЭРБ для последующей рациональной фармакотерапии ГЭРБ.
Дизайн исследования
Первичные и вторичные конечные точки
Первичная конечная точка:
- уменьшение частоты и выраженности изжоги через 8 недель лечения при лечении омепразолом в сочетании с домперидоном, в сравнении с омепразолом.
Вторичные конечные точки:
- уменьшение выраженности изжоги, оцененной по визуально-аналоговой шкале, через 8 недель лечения;
- частота эпизодов изжоги через 4 и 8 недели лечения;
- доля пациентов с полным купированием изжоги на 4 и 8 недель лечения;
- число дней без изжоги через 4 недели лечения;
- доля пациентов с разрешением эзофагита через 8 недель лечения среди лиц, имевших эзофагит на момент включения в исследование.
Конечные точки безопасности:
- частота побочных явлений в группе пациентов, получивших после рандомизации как минимум одну дозу лекарственного средства;
- частота серьезных побочных явлений;
- частота тяжелых побочных явлений;
- частота побочных явлений, определенно связанных с приемом испытываемого лекарственного средства.
Стадии исследования:
- Скрининг – предварительный отбор пациентов в соответствии с клиническими критериями; подписание информированного согласия; назначение и проведение скрининговых процедур; принятие решения о включении/невключении пациента в исследование по результатам скрининговых процедур в соответствии с критериями включения/невключения.
- Рандомизация – распределение пациентов, включенных в исследование, по двум группам: Группа 1 – лечение исследуемым омепразолом в сочетании с домперидоном, группа 2 – лечение ЛС сравнения омепразолом случайным образом.
- Лечение – Пациенты согласно рандомизационному номеру получают либо омепразол в сочетании с домперидоном, либо омепразол в назначенном режиме. Лечение проводилось амбулаторно; с установленной периодичностью пациенты посещали исследовательскую базу.
- После окончания лечения пациенты возвращались к своему обычному режиму жизни, однако за ними продолжается наблюдение с целью оценки эффективности проведенной терапии и регистрации побочных явлений.
По дизайну исследование является рандомизированным, открытым, сопоставительным, параллельным, с отслеживанием эффектов. Схема исследования представлена на рисунке 1.
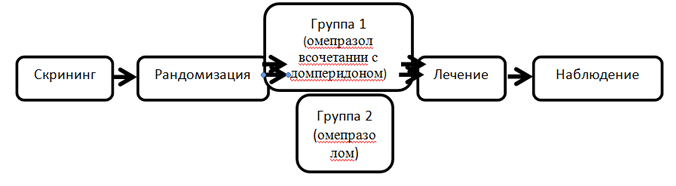
Рисунок 1. Схема исследования
Выбор и исключение испытуемых
Выбор испытуемых проводился исключительно на добровольной основе
Критерии включения испытуемых
1) желание участвовать в исследовании и способность подписать информированное согласие;
2) возраст старше 18 лет;
3) гастроэзофагеальнаярефлюксная болезнь, проявляющаяся изжогой с частотой не менее 2 раз в неделю, предшествующую 0-му визиту;
3) использование на период исследования надежных методов контрацепции для женщин фертильного возраста;
4) наличие результатов ультразвукового исследования (УЗИ) органов брюшной полости (ОБП), проведенного в последние 6 месяцев перед включением в исследование.
Критерии невключения
1) отказ от проведения эндоскопического исследования;
2) гастроэзофагеальнаярефлюксная болезнь с тяжелым эзофагитом (степень С или D по Лос-Анджелесской классификации);
3) пищевод Барретта;
4) беременность или лактация;
5) прием нестероидных противовоспалительных средств (НПВС), ацетилсалициловой кислоты, бисфосфонатов, нитратов, антагонистов кальция, ингибиторов протонного насоса или Н2-блокаторов, прокинетиков, клопидогреля;
6) участие в ином клиническом испытании;
7) анамнез аллергической реакции или непереносимости компонентов лекарственных средств;
8) стриктура пищевода;
9) гастрэктомия или резекция желудка;
10) злокачественные новообразования любой локализации в настоящее время;
11) злоупотребление алкоголем;
12) тяжелая сердечно-сосудистая или дыхательная недостаточность;
13) печеночная недостаточность;
14) почечная недостаточность.
Критерии исключения
1) мнение исследователя о необходимости исключения пациента в интересах самого пациента;
2) ошибочное включение в испытание;
3) решение исследователя исключить пациента вследствие серьезного отклонения от программы испытания;
3) серьезные побочные эффекты (СПЯ), в том числе смерть (с указанием даты смерти);
4) побочные явления (ПЯ), требующие наблюдения и медикаментозного лечения;
5) острые заболевания или состояния, которые, по мнению исследователя, требуют исключения пациента из испытания;
6) прием во время испытания НПВС, ацетилсалициловой кислоты, бисфосфонатов, нитратов, антагонистов кальция, ингибиторов протонного насоса или Н2-блокаторов, прокинетиков, антацидов (кроме исследуемого ЛС или ЛС сравнения) или необходимость назначения такого лечения;
7) положительный тест на беременность (для женщин);
8) неявка пациента на визит;
9) отказ пациента от продолжения участия в исследовании;
10) непереносимость исследуемого ЛС или ЛС сравнения;
11) острое состояние, при котором имеется потребность в хирургическом вмешательстве
Комментарий к эндоскопическому обследованию.
Осмотр пищевода осуществлялся видеогастроскопом высокого разрешения, диаметром 9 мм, с поддержкой формата видеосигнала HDc возможностью освещения слизистой узковолновым светом. Каждое исследование сопровождается видеозаписью в формате avi.
Градационная характеристика рефлюкс-эзофагита проводится в соответствии с классификацией эзофагита[19]:
Степень А: Одна или несколько зон изменений слизистой(в том числе гиперемии), располагающихся изолированно по складкам, не носящих сливного характера, каждая на длине 5 мм.
Степень В: Как минимум одна зона изменений(повреждений) слизистой более чем 5 мм в длину, располагающихся изолированно по складкам, без признаков слияния.
Степень С: Одна или несколько зон повреждений слизистой(в том числе гиперемии) более 5 мм в длину, повреждения распространяются между складками, занимая менее 75% окружности.
Степень D: Повреждения слизистой оболочки занимают более 75% окружности пищевода.
Осложнения: язва, кровотечение, перфорация, стриктура, пищевод Барретта, аденокарцинома.
При этом наличие осложнений является критерием исключения пациента из исследования.
Проводилась оценка распространения цилиндрической метаплазии слизистой пищевода в соответствии с пражскими критериями: измеряется расстояние от места гастроэзофагеального перехода до нижней границы плоского и цилиндрического эпителия(С) и расстояние до верхней границы плоского и цилиндрического эпителия(М) [20].
При этом, С > 2 см являлись критерием исключения пациента из исследования, как и подозрение на эзофагит, не связанный с ГЭРБ (например – эозинофильный эзофагит).
Проводилась оценка микроархитектоники слизистой абдоминального отдела пищевода(зоны, располагающейся под границей перехода плоского эпителия в цилиндрический) в соответствии с критериями классификацией Toyoda(2004) [21]:
Тип 1 Нормальный паттерн
Тип 2 Щелевидно-ретикулярный
Тип 3 Извилисто-ворсинчатый паттерн
При этом визуальное определение характера паттерна как тип 3 является критерием исключения пациента из исследования.
Проводилась оценка наличия и степени недостаточности нижнего пищеводного сфинктера в соответствии с приведенной ниже классификацией(проводится на инверсии из просвета желудка) [22]:
степень 1 – четко видимая циркулярная складка ткани, расположенная по большой кривизне плотно облегающая эндоскоп,
степень 2 – складка присутствует, но возникают периоды быстрого открытия и закрытия отверстия НПС,
степень 3 – складка отсутствует, а эндоскоп не облегается слизистой,
степень 4 – складка отсутствует, просвет пищевода зияет, плоский эпителий четко визуализируется выше.
Лечение испытуемых представлено в таблице 1.
Таблица 1. Характеристика лечения для испытуемых каждой группы
|
Группа |
Разовая доза |
Схема введения |
Путь введения |
Длительность лечения |
Длительность наблюдения |
|
Группа 1 омепразол всочетании с домперидоном |
2 капсулы |
1 раз/сут: утром За 30 мин до завтрака, |
Внутрь |
56 дней +/-3 дня |
56 дней +/-3 дня |
|
Группа 2 омепразол |
2 капсулы |
1 раз/сут: за 30 мин до завтрака |
Внутрь |
56 дней +/-3 дня |
56 дней +/-3 дня |
Статистический анализ
Статистический анализ проводился с учетом рекомендаций, указанных в приложении 13, таблица 2, Приказ Министерства здравоохранения Республики Беларусь №237 от 14.03.2011 «О внесении изменений и дополнений в приказ Министерства здравоохранения Республики Беларусь № 610 от 23.06.2009.
Статистическую обработку результатов проводили с помощью пакета прикладных программ Statistica-6 версия 6.1, серия 1203d, WinPepi(2004г.), программы NCSS 2004 R., с использованием методов описательной статистики, дисперсионного анализа на персональном компьютере.
Все данные клинического исследования проверяли на соответствие распределению Гаусса. Для этого применяли количественный тест Шапиро-Уилка(Shapiro-WilkW), строили квантильные графики, сопоставляли гистограмму распределения изучаемого показателя с теоретической кривой нормального распределения при оцененных значениях среднего и стандартного отклонения. При значении теста, существенно превышающего принятый за критический уровень значимости p = 0,05, а также при отсутствии существенных отклонений от прямой на квантильных графиках, считали, что нет оснований отвергать предположение о соответствии изучаемого параметра Гауссовому распределению. При значениях теста, близких к критическому значению, решение о соответствии распределения нормальному принимали на основании вида квантильных графиков. Дополнительно нормальность распределения оценивалась по семи критериям: Shapiro-WilkW,Anderson-Darling, Martinez-Iglewicz, Kolmogorov-Smirnov, D’AgostinoSkewness, D’AgostinoKurtosis, D’AgostinoOmnibus. Окончательное решение о нормальности распределения принималось с учетом всех критериев, но при разных вариантах значений преимущество отдавалось двум критериям – Шапиро-Уилка(Shapiro-WilkW) и Колмогорова-Смирнова (Kolmogorov-Smirnov).
При значительных отклонениях распределения от Гауссового делалась попытка нормализовать данные, применяя различные обратимые преобразования: логарифмирование, двойное логарифмирование, вычисление обратных значений. Распределение полученных значений изучалось и на основании этого принималось решение об использовании в дальнейшем параметрических или непараметрических методов анализа. При соответствии распределения изучаемого количественного параметра (или его преобразования) распределению Гаусса данные представлялись в виде среднего арифметического значения и стандартного отклонения. В противном случае данные представлялись в виде медианы и квартилей.
Для описательной статистики учитывались: N наблюдений, среднее, доверительный интервал (ДИ -95,0% – +95,0%), геометрическая средняя, медиана, сумма, квартили(нижняя и верхняя), процентили, дисперсия, стандартное отклонение, стандартная ошибка.
При сравнении в одной группе результатов до и после приема лекарственного средства использовались следующие критерии: Вилкоксона (критерий знаков) и Мак-Нимана и др.
Данные о распределении качественных параметров (градация в оценке), а также сгруппированных количественных данных (возрастная группа) представлялись в виде частотных распределений с указанием удельного веса категории параметра (если количество наблюдений было достаточно большим) и/или в виде абсолютного количества наблюдений.
Для сравнения качественных данных, которые можно представить в виде таблиц сопряженности 2×2, применяли двусторонний точный тест Фишера. Для сравнения качественных стратифицированных данных, которые можно представить в виде k таблиц сопряженности 2×2, применяли тест Кохрейна-Мантеля-Ханцеля.
При сравнении частотных распределений в группах использовали критерий χ2 с поправкой на непрерывность.
При сравнении количественных показателей, имеющих нормальное или близкое к нормальному распределение, в 3-х группах и более использовался дисперсионный анализ. При сравнении значений количественных признаков, не имеющих нормальное распределение, в группах использовался двусторонний тест Уилкоксона–Манна–Уитни с поправкой на непрерывность. При этом учитывалось наличие или отсутствие повторяющихся значений.
При решении вопроса о принятии нулевой гипотезы в качестве критического уровня значимости (двусторонних тестов) использовалось значение: p тренда = 0,05(2,5%).
При уровне значимости нулевой гипотезы p тренд< 0,05 различия считались статистически значимыми. При p тренде> 0,05 предполагалось, что нет достаточных статистических оснований для отклонения нулевой гипотезы о равенстве анализируемых значений между группами.
Результаты.
Характеристика рандомизированной группы.
В соответствии с программой (протоколом) исследования, в данном клиническом испытании набрано 60 добровольцев (волонтеров). Для набора данного числа наблюдений потребовался скрининг 181 пациента.
Суммарные данные результатов скрининга, и причины невключения в исследование, представлены в таблице 2.
Таблица 2. Причины невключения в исследования
|
Эзофагит С и D по Л-А. |
ГПОД |
Язвы и прочие |
Подозрение на особые формы эзофагитов, включая эозинофильный |
Пищевод Барретта |
Другие заболевания |
Прием лекарств |
Не явились на визит рандомизации |
Всего |
|
23 |
33 |
10 |
20 |
8 |
10 |
10 |
7 |
121 |
Общая характеристика группы скрининга представлена ниже.
Доля лиц мужского пола составила 49,2% (ДИ95% (Exact 95% C.I. (Fisher’s) = 41,7 – 56,7). Доля лиц с эзофагитом А составила 41,4% (ДИ95% Exact 95% C.I. (Fisher’s) = 34,2 – 49,0). Доля лиц с эзофагитом В составила 35,4% (ДИ95% Exact 95% C.I. (Fisher’s) = 28,4 – 42,8). Доля лиц с эзофагитом С составила 12,7% (ДИ95% Exact 95% C.I. (Fisher’s) = 8,2 -18,5). Без эзофагита 10,5% (ДИ95% Exact 95% C.I. (Fisher’s) = 6,4–15,9). Доля лиц с грыжами пищеводного отверстия диафрагмы (ГП) составила 18,2%(ДИ95% Exact 95% C.I. (Fisher’s) = 12,9 – 24,6). Доля лиц с эзофагитом Барретта составила 4,4% (ДИ95% Exact 95% C.I. (Fisher’s) = 1,9 – 8,5).
Всего было рандомизировано 60 пациентов с ГЭРБ.
В таблице 3 представлены результаты статистического анализа возраста и индекса массы тела (ИМТ) у мужчин иженщин в общей группе и другие общие показатели. В этой таблице: 0 – женщины, 1 – мужчины.
Таблица 3. Значения возраста и ИМТ у мужчин и женщин
|
Итоговая таблица средних N=60 |
|
||||||
|
|
Пол |
Возраст Среднее |
Возраст N |
Возраст Ст.откл. |
ИМТ Среднее |
ИМТ N |
ИМТ Ст.откл. |
|
|
0 |
50,33 |
33 |
10,99 |
27,08 |
33 |
4,52 |
|
|
1 |
41,33 |
27 |
11,16 |
26,95 |
27 |
4,52 |
|
|
Всего |
46,28 |
60 |
11,87 |
27,02 |
60 |
4,48 |
Примечание: 0 – женщины, 1 – мужчины.
Общая характеристика рандомизированной группы по медианной статистике: Ме(25-75 квартили) выглядит следующим образом. Возраст пациентов – 46,5(36,0 – 57,5), ИМТ – 27,0 (23,8 – 30,0), длительность заболевания(годы) – 2,0 (1,0 – 3,0), диагностическая шкала ГЭРБ – 8,0 (7,0- 9,0).
Характеристика групп Омез-DSR и Омез.
В группе омепразола в сочетании с домперидономдоля мужчин составляет 36,7% (ДИ95%, Exact 95% C.I. (Fisher’s) = 19,9–56,1). В группе омепразола доля мужчин составила 53,3% (ДИ95%, Exact 95% C.I. (Fisher’s) = 34,3–71,7), разность недостоверна. Группа омепразола в сочетании с домперидоном имела достоверно более высокие значения ИМТ (28,2 против 25,9) и большие значения возраста 47,1 против 45,7, однако разность недостоверна.
Сопоставление по анамнестическим данным показало отсутствие статистической разности в частоте возникновения рефлюксных симптомов, выраженности таких симптомов, факторам их провокации. Достоверные отличия обнаружены по прогрессированию изжоги: в группе омепразола в сочетании с домперидономбольшая часть пациентов отметила наличие прогрессирования изжоги- 73,3% против 46,7% в группе омепразола.
Отмечается гомогенность групп по основным данным анамнеза болезни (ГЭРБ), однако имеется гетерогенность по прогрессированию изжоги, при этом группа омепразола в сочетании с домперидоном, по данному показателю, имеет хуже динамику изжоги (прогрессирование) по сравнению с группой омепразола.
Сопоставительная характеристика, по частотным таблицам и таблицам 2хk, основных жалоб пациентов с ГЭРБ в двух группах показала отсутствие достоверных отличий по: изжоге, кислой регургитация (ощущение заброса желудочного содержимого в рот или глотку), боль в груди, дисфагии, тошноте, рвоте, одинофагии, ситофобии, боли в эпигастральной области, снижении массы тела, хроническом кашле, одышке, нарушении сна, связанные с вышеперечисленными жалобами.
Таким образом, по основным жалобам группы омепразола в сочетании с домперидономи омепразола гомогенны (похожи).
Полученные результаты статистического анализа гомогенности(похожести) выделенных групп по клинических характеристикам указывают на их гомогенность и возможность последующего сопоставления без существенных ошибок системного плана.
Статистический анализ гомогенности групп по эндоскопическим данным представлен ниже.
Гомогенность групп по частоте эзофагита: в группе омепразола в сочетании с домперидоном– 83,3%, в группе омепразола – 76,7%, при Хи-квадрат (ст.св.=1) = 0,42 (ртренд = 0,52), поправка Йетса = 0,10 (р тренд= 0,75). Гомогенность групп по степени тяжести эзофагита: Хи-квадрат (ст.св.=1) = 0,64 (ртренд = 0,42), поправка Йетса = 0,22 (р тренд= 0,63).
Полученные результаты указывают на то, что группы гомогенны по категориальным переменным частота эзофагита и степени тяжести эзофагитов.
Оценка эффективности лечения.
Уменьшение выраженности изжоги одинаково часто отмечено в обеих группах, и отмечено у всех (100%) пациентов.
В группе омепразола в сочетании с домперидономдостоверно чаше отмечается полное купирование рефлюксных симптомов через 8 недель лечения: 83,3% (ДИ95% = Exact 95% C.I. (Fisher’s) = 65,3 – 94,4) против 43,3%(ДИ 95% = Exact 95% C.I. (Fisher’s) = 25,5 – 62,6). Отношение шансов (OR) купирования симптомов составляет 6,54(ДИ95%=2,06-21,73), т.е. прогностически в 6 раз выше при лечении омепразолом в комбинации с домперидоном. NNT (number needed to treat), за период лечения 8 недель, для омепразола в сочетании с домперидоном= 2.5 (95% C.I.: 1.7 to 7.5), т.е. в 2,5 раза лучше по сравнению с омепразолом.
Лечение омепразолом в комбинации с домперидоном на протяжении 8 недель сопровождается достоверно более длительным промежутком времени дней без изжоги: 23 дня (ДИ95% = 22-24),против 12 дней(ДИ95%= 10-14) на омепразоле.
Эффективность по эндоскопическим результатам наличия эзофагита после лечения оказалась следующей. Доля пациентов с эзофагитом в группе омепразола в комбинации с домперидоном меньше, по сравнению с долей эзофагитов в группе омепразола. Эффективность лечения омепразолом с домперидоном выше по сравнению с омепразолом: без эзофагита – 92,0% (ДИ95%= Exact 95% C.I. (Fisher’s) = 74,0 – 99,0) от всех пациентов с эзофагитом на старте для группы омепразола с домперидоном, против без эзофагита 65,2% ДИ95% = Exact 95% C.I. (Fisher’s) = 42,7 – 83,6) от всех пациентов с эзофагитом на старте для группы омепразола. Отношение шансов составляет 6,13 (ДИ95% = 0,99-64,57). Значение NNT = 3,7(ДИ95%=2,0-194).
Используя известную градацию критерии оценки NNT (1,0 – идеальный препарат; >1,0 <2,5 – очень хороший(по эффективности) препарат; > 2,5 < 10 – хороший (по эффективности) препарат), омепразол в комбинации с домперидоном можно оценить следующим образом: по полному купированию симптомов рефлекса (NNT = 2,5) как очень хороший препарат, по ликвидации эзофагита как хороший препарат (NNT= 3,7).
Переносимость и безопасность
Всего было зарегистрировано 5 случаев неблагоприятных реакций (НЯ) у 60 пациентов, прошедших курс лечения. Все относятся к НЯ легкой степени: галакторея – 1 случай, ощущение набухания грудных желез – 1 случай, головная боль – 3. Все НЯ не нуждались в дополнительном лечении или прекращении лечения и купировались самостоятельно. Частота НЯ составила 8,3% (ДИ95% = 2,8 – 18,0). НЯ в группе 1 было зарегистрировано 2 случая, что составляет 6,7% (ДИ95% = 0,8 – 22,1), в группе 2 – 3 случая, т.е. 10% (ДИ95% = 2,1-26,5).
Особое внимание было уделено состоянию частоты сердечных сокращений (ЧСС), простому и доступному варианту контроля возможного развития аритмий. До лечения в 97% случаев ЧСС находилась в пределах 65-80, после лечения омепразолом с домперидоном в этих пределах находится 100% случаев. Случаев сердечных аритмий зарегистрировано не было. Систолическое артериальное давление (САД): на нижний размах значений САД 110-115 ммHg до лечения приходилось 10%, после завершения леченияомепразолом с домперидоном–7%, на значении 140 ммHg и более приходилось до начала лечения 20%, после – 10%. Диастолическое артериальное давление (ДАД): на нижний размах значений 60-65 ммHg приходится 3% до начала лечения и 3% после окончания лечения омепразолом с домперидоном, на значения ДАД 90 ммHg и более приходилось 13% до лечения и 10%после лечения омепразолом с домперидоном.
Полученные результаты указывают на то, что лечение омепразолом с домперидономна протяжении 8 недель не оказывало воздействие на частоту сердечных сокращений и артериальное давление, не было зарегистрировано сердечных аритмий.
В группе омепразола с домперидономхорошая и очень хорошая переносимость лечения составила 25 и 5 случаев (всего 30, или 100%), в группе омепразола– 19 и 10 случаев (всего 29, или 96,7%), достоверного отличия нет. Все добровольцы завершили исследование, исключений добровольцев из исследования не было.
Обсуждение полученных результатов
В данном исследовании установлено, что в группе пациентов с ГЭРБ лечение омепразолом с домперидоном достоверно чаще приводило к полному купированию рефлюксных симптомов через 8 недель лечения: 83,3% (ДИ 95% = 65,3–94,4) против 43,3%(ДИ 95% = 25,5–62,6) при леченииомепразолом. Отношение шансов (OR) купирования симптомов составляет 6,54(ДИ95%=2,06–21,73). Полученные результаты соответствуют опубликованным. Результаты по эффективности лечения ГЭРБ домперидоном опубликованы в 38 исследованиях, с общим числом пациентов – 467, средняя эффективность домперидона по симптомам составила 86%, плацебо – 55%, по ликвидации эзофагита 65% на домперидоне и 60% на плацебо.
В частности, в 2000 году было опубликовано масштабное исследование по прокинетикам, в котором было указано, что общее число детей в Канаде и Великобритании, получивших лечение прокинетиками, составило более 50 тысяч, при этом была показана большая эффективность домперидона (65-85%) по сравнению с метоклопромидом при ГЭРБ [16].
Клиническая значимость омепразола с домперидоном заключается в повышении эффективности лечения двух форм заболеваний ГЭРБ и диспепсии, являющихся заболеваниями с высоким уровнем популяционной распространенности (общей заболеваемости), превышающей 10% по эпидемиологическим данным, т.е. при демографически значимых для республики заболеваний.
Дополнительно, клиническая значимость заключается в возможности лечения форм ГЭРБ резистентных к ингибиторам протонной помпы, доля таких форм составляет от 20% до 40%.
В данном исследовании не было зарегистрировано неблагоприяных сердечно-сосудистых реакций при лечении омепразолом в комбинации с домперидоном, в суточной дозе домперидона – 30 мг, на протяжении 8 недель.
Домперидон в качестве противорвотного средства используется с середины 20 века. В ряде стран отнесен к группе безрецептурных лекарственных средств. В США с 2010 г. незарегистрирован в качестве лекарственного средства. Федеральное агентство по лекарственным препаратам и продуктам питания США (FDA) в ряде своих публикаций отмечало негативное отношение к домперидону. Важно при этом обратить внимание на то, что в США метоклопрамид к 2012г. вошел в список 100 основных лекарственных средств, не имея доказательств преимущества как по эффективности, так и по безопасности, по сравнению с домперидоном. Такое сопоставление вызывает сомнение в объективности оценки самого домперидона.
Накопление данных по безопасности домперидона к 2013г. позволяет многим авторам публикаций по домперидону оценивать его безопасность следующим образом: «Домперидон противорвотный препарат с относительно небольшим количеством побочных эффектов» («Domperidone is an antiemetic drug with relatively few side-effects») van Roeden SE, et al. [23]. Указанные в ссылке авторы из Нидерландов провели систематический поиск литературы по расследованию опасений в отношении повышенного риска внезапной сердечной смерти у домперидона. Авторы обнаружили всего три публикации, из четырех исследований случай-контроль (низкий уровень доказательности), в которых выявлено статистически значимое повышение вероятности внезапной сердечной смерти при использовании домперидона. Зависимость доза-реакция была описана только в одном исследовании. Авторы указывают, что имеет место влияние нескольких вмешивающихся дополнительных факторов в сочетании с домперидоном на развитие внезапной сердечной смерти. Авторы пришли к выводу, что существует взаимосвязь между употреблением домперидона и внезапной сердечной смерти в дозах только более 30 мг в сутки. Одним из основных заключений, к которым пришли авторы, является следующее: «При дозе 30 мг в сутки домперидон может назначаться безопасно» («At a dose of 30 mg per day, domperidone can be prescribed safely»).
В 2013 г. было проведено специальное клиническое исследование по оценке безопасности домперидона с акцентом на индукцию нарушений сердечной проводимости [24]. Результаты исследования позволили прийти к следующему заключению: клинически значимого увеличения QTCP не наблюдалось при разовой дозе 10 мг домперидона, как и при дозе в 10 мг четыре раза в день, включая и максимальные дозы по 20 мг четыре раза в сутки.
Тем не менее, 1 марта 2013 г. по обращению бельгийского агентства – Федеральное агентство по лекарственным средствам и медицинской продукции – в Европейский комитет по оценке фармакологического риска (PRAC), началось рассмотрение безопасности домперидона по отношению к риску внезапной сердечной смерти. Рекомендации PRAC были отправлены в координационную группу по взаимному признанию и децентрализованным процедурам у человека (CMDh), которое приняло окончательную позицию. CMDh, орган, представляющий государства-члены Европейского союза (ЕС), несет ответственность за обеспечение согласованных стандартов безопасности для лекарственных средств, разрешенных с помощью национальных процедур в странах ЕС. Так как рекомендации CMDh были приняты большинством голосов, позиция CMDh теперь будет направлена в Европейскую комиссию, которая будет рассматривать обязательность предложений CMDh на всей территории ЕС (данные на апрель 2014г.).
Сутьосновныхрекомендаций CMDh заключаетсявследующем (CMDh confirms recommendations on restricting use of domperidone-containing medicines. 25/04/2014):
– домперидон-содержащие препараты должны оставаться доступными, и могут продолжать использоваться в ЕС для воздействия на симптомы тошноты и рвоты, но рекомендуемая доза должна быть снижена до 10 мг три раза в день перорально (суточная = 30мг), для взрослых и подростков с массой тела 35 кг и более.
Суточная доза домперидона в лекарственном средствеомепразолав сочетании с домперидоном составляет 30мг, по данным биоэквивалентным исследованиям эта доза при медленном высвобождении соответствует дозе 10 мг.
В Канаде (провинция Saskatchewan) было проведено ретроспективное популяционное исследование по оценке риска серьезных неблагоприятных реакций (СНЯ) в виде желудочковых аритмий и внезапной сердечной смерти на популяции выбора в виде 1608 случаев таких реакций и 6428 контрольных случаев [25]. Авторы представили данные, которые показывают минимальную степень риска СНЯ у домперидона по отношению к лечению без домперидона, со стремлением этого риска к нулевому значению, при использовании многофакторной логистической модели (объективной и доказательной модели риска), что доказывает в большей степени влияние неизвестных факторов, а не домперидона на риск внезапной сердечной смерти и желудочковые аритмии.
На основании опубликованных данных [26] можно представить шансы рисков (Odds ratio, OR) серьезных неблагоприятных сердечных реакций у некоторых лекарств по отношению к домперидону (Domperidone – OR = 1.6 (95%C.I.= 1.4 – 1.8):Metoclopramide – 2.6 (2.2 – 3.1) Phenoxymethylpenicillin – 2.6 (2.3 – 2.9) Ceftriaxone -5.2 (2.1 – 13.1) Erythromycin 2.6 (1.9 – 3.40. Эти данные показывают, что риск серьезных сердечных реакций у метоклопрамида, феноксиметилпенициллина и эритромицина в 1,6 раза выше по сравнению с домперидоном, а цефтриаксона в 3 раза выше.
В сборнике тезисов Американской гастроэнтерологической недели за 2014г. представлены тезисы исследования профиля безопасности домперидона в отношении сердечно-сосудистых неблагоприятных реакций [27]. Авторы представили следующее заключение: «OurdatafromalargeclinicalexperienceoftreatingpatientsbyonephysicianindicatethatDOM, anon-FDAapprovedprokinetic/antiemeticagent, hasalowriskofcardiovascularadverseeventswhileexhibitinggoodclinicalefficacy», т.е. указывают на низкий риск у домперидона в отношении неблагоприятных сердечно-сосудистых реакций, в сочетании с хорошей клинической эффективностью.
Таким образом, на основании всего изложенного, при использовании омепразола в сочетании с домперидоном степень риска может быть определена как минимальная и не превышает степень риска при проведении лечения по утвержденным МЗ РБ протоколам для гастроэзофагеальной рефлюксной болезни (ГЭРБ) и диспепсии, в частности при использовании метоклопрамида. Отрицательные последствия лечения омепразолом в сочетании с домперидоном не превышают опасность самих заболеваний.
Заключение
Проведено пострегистрационное, проспективное, рандомизированное исследование с отслеживаниемрационального применения омепразола в комбинации с домперидоном при гастроэзофагеальной рефлюксной болезни легкой и средней степени тяжести. Исследование зарегистрировано в международной базе данных клинических исследований (clinicaltrial.gov)- NCT02140073.
Для обеспечения рандомизации проведен скрининг 181 случая с проявлениями ГЭРБ. Рандомизация проведена в две группы, по 30 случаев в каждой: группа, получившая лечение омепразолом с домперидоном(исследуемый препарат) и группа получившая лечениеомепразолом (препарат сравнения).
Сопоставительный анализ гомогенности двух групп показал высокую степень гомогенности по многочисленным клиническим и эндоскопическим показателям.
В обеих группах ощущение тошноты 2-3 дня в неделю и более отмечено в 56,6% и в 76,7% случаев, т.е. часто, что является с одной стороны типичным симптомом для ГЭРБ, с другой стороны отмечается часто.
В группе омепразола в сочетании с домперидоном достоверно чаше отмечается полное купирование рефлюксных симптомов через 8 недель лечения: 83,3% (ДИ 95% = 65,3–94,4) против 43,3%(ДИ95% = 25,5–62,6). Отношение шансов (OR) купирования симптомов составляет 6,54(ДИ95%=2,06–21,73), т.е. прогностически в 6 раз выше при лечении омепразолом в комбинации с домперидоном. NNT (number needed to treat), за период лечения 8 недель, для омепразола в сочетании с домперидоном = 2.5 (95% C.I.: 1.7 to 7.5).Лечение омепразолом в комбинации с домперидоном на протяжении 8 недель сопровождается достоверно более длительным промежутком времени дней без изжоги: 23 дня (ДИ95% = 22-24),против 12 дней(ДИ95%= 10 – 14) на омепразоле.
Доля пациентов с эзофагитом в группеомепразола в сочетании с домперидоном меньше, по сравнению с долей эзофагитов в группе омепразола. Эффективность лечения омепразолом с домперидоном выше по сравнению с омепразолом: без эзофагита 92,0% (ДИ95%= 74,0 – 99,0) от всех пациентов с эзофагитом на старте для группы омепразола в сочетании с домперидоном, против без эзофагита 65,2% ДИ95% = 42,7 – 83,6) от всех пациентов с эзофагитом на старте для группы омепразола. Отношение шансов составляет 6,13 (ДИ95% = 0,99-64,57). Значение NNT = 3,7(ДИ95%=2,0-194).
Неблагоприятные реакции в группе омепразола в сочетании с домперидоном составили 6,7% (ДИ95% = 0,8 – 22,1), в группе омепразола – 10% (ДИ95% = 2,1-26,5). Тахикардии, брадикардии или аритмии не было зафиксировано.
Полученные результаты показывают следующее:
- омепразол в сочетании с домперидоном можно охарактеризовать как рациональное для лечения ГЭРБ по композиции действующих веществ, что определяется наличием у пациентов с ГЭРБ частым ощущением тошноты (более 80% лиц), при этом тошнота 2-3 дня в неделю и более отмечена более чем в 60% случаев;
- омепразол в сочетании с домперидоном является более эффективным по сравнению с омепразолом при 8-недельной длительности: NNT полному купированию симптомов рефлекса = 2,5, по ликвидации эзофагита NNT= 3,7;
- омепразол в сочетании с домперидоном хорошо переносится (очень хорошая и хорошая переносимость в 100%) иявляется безопасным (частота неблагоприятных реакций легкой степени составляет 6,7% (ДИ95% = 0,8 – 22,1).
Использованнаялитература
- The Montreal Definitionand Classification of Gastroesophageal Reflux Disease: A Global Evidence-Based Consensus // Am. J. Gastroenterol. – 2006. – V.101. – P. 1900–1920.
- Dent J.et al., Epidemiology of gastrooesophageal reflux disease: a systematic review // Gut. – 2005. – V. 54. – P. 710–717.
- Bytzer P. Goals of therapy and guidelines for year treatment success in symptomatic gastroesophageal efflux disease patients // Am J. Gastroenterology.- 2003 . – V.98.– P 31-39..
- Edwards S.J., Lind T., Lundell L. Systematic review of proton pump inhibitors for the acute treatment of reflux oesophagitis // Aliment Pharmacol Ther 2001 . – V.15.– P 1729-1736;.
- Castell D.O., Kahrilas P.J., Richter J.E. et al. Esomeprazole (40 mg) compared with lansoprazole (30 mg) in the treatment of erosive esophagitis // Am J Gastroenterol.- 2002. – V. – P. 575-583.
- Carting L., Axelsson C.K., Forssell H. et al. Lansoprazole and omeprazole in the prevention of relapse of reflux oesophagitis: a long-term comparative study // Aliment Pharmacol Ther.- 1998. – V. 12– P. 985—990.
- DupasJ.L., Houcke P., Samoyeau R. Pantoprazole versus lansoprazole in French patients with reflux esophagitis // Gastroenterol Clin Biol.- 2001. – V.25– P. 245-250;
- Howden C.W., Bollard E.D., Robieson W. Evidence for therapeutic equivalence of lansoprazole 30 mg and esomeprazole 40 mg in the treatment of erosive oesophagitis // Clin Drug Invest.- 2002 . – V. 22– P. 99—109.
- Sharma V.K., Leontiadis G.I., Howden C.W. Meta-analysis of randomized controlled trials comparing standard clinical doses ofomeprazole and lansoprazole in erosive oesophagitis // Aliment Pharmacol Ther.- 2001 . – V.15– P. 227-231.
10. Thjodleifsson B., Beker J.A., Dekkers C., Bjaaland T., Finnegan V., Humphries T.J. Rabeprazole versus omeprazole in preventing relapse of erosive or ulcerative gastroesophageal reflux disease: a double-blind, multicenter, European trial. The European Rabeprazole Study Group // Dig Dis Sci.- 2000 . – V.45– P. 845-853.







