Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "Место бета-блокаторов в терапии артериальной гипертонии"
Автор: Исабекова А.Х.
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Кардиология, Семейная медицина/Терапия
Просмотров: 3 301
Дата проведения: с 02.06.2015 по 02.06.2016
 Гипертензией является повышение систолического артериального давления (САД)≥140 мм рт.ст. и/или повышение диастолического артериального давления (ДАД) ≥ 90 мм рт.ст. [1].
Гипертензией является повышение систолического артериального давления (САД)≥140 мм рт.ст. и/или повышение диастолического артериального давления (ДАД) ≥ 90 мм рт.ст. [1].
Артериальная гипертензия – хроническое стабильное повышение АД, при котором уровень систолического АД равен или более 140 мм рт.ст., и (или) уровень диастолического АД равен или более 90 мм рт.ст. у людей, которые не получают антигипертензивных препаратов. [ Рекомендации Всемирной организации здравоохранения и Международного общества по гипертензии 1999 г.] [2].
Первичная причина возникновения артериальной гипертонии (АГ) не установлена.
Установленные механизмы патогенеза АГ:
– Мембранная концепция АГ
– Генетические дефекты
– Повреждение эндотелия
– Роль РАС (АТ II) в формировании АГ
– Роль СНС в формировании АГ
– Депрессорные факторы
– Ремоделирование ССС
Пусковые механизмы (триггеры)
1. Факторы, связанные с окружающей средой и образом жизни:
– Избыточное потребление соли
– Избыточное потребление алкоголя
– Стресс
– Ожирение
– Недостаточная физическая активность
2. Генетические факторы
Гены-кандидаты АГ
– ген рецепторов АТ II
– ген АПФ
– альфа-альдуцин
– ген трансформирующего фактора роста 1
– ген рецепторов глюкокортикоидов
– ген рецепторов инсулина
– ген бета2-адренергических рецепторов
– ген рецепторов дофамина 1а
– ген адренергических рецепторов
– ген альфа2-адренергических рецепторов
– ген глюкозо-6-фосфатдегидрогеназы
– ген липопротеидной липазы
– ген эндотелиальной NO-синтетазы
– ген простациклиновой синтетазы
– ген соматотропного гормона
– ген панкреатической фосфолипазы
– SA-ген
Артериальная гипертензия – это самостоятельное, обычно прогрессирующее заболевание, главным проявлением которого является повышение систолического и/или диастолического артериального давления (> 140/90 мм рт.ст.), либо только систолического (систолическая гипертония), с постепенным вовлечением в патологический процесс органов-мишеней. Если систолическое или диастолическое АД находятся в разных категориях, то пациента причисляют к более высокой категории. Единая классификация используется для молодых, пожилых и людей среднего возраста.
Таблица 1. Классификация уровней АД (мм рт.ст.), ВОЗ/МОАГ, 1999 г.
|
Категории АД |
Систолическое АД |
Диастолическое АД |
|
|
Оптимальное |
< 120 |
и |
< 80 |
|
Нормальное |
120 – 129 |
и/или |
80 – 84 |
|
Высокое нормальное |
130 – 139 |
и/или |
85 – 89 |
|
АГ 1-й степени |
140 – 159 |
и/или |
90 – 99 |
|
АГ 2-й степени |
160 – 179 |
и/или |
100 – 109 |
|
АГ 3-й степени |
≥ 180 |
и/или |
≥ 110 |
|
Изолированная систолическая АГ * |
≥ 140 |
и |
< 90 |
* ИСАГ должна классифицироваться на 1, 2, 3 ст. согласно уровню систолического АД.
У больных АГ прогноз зависит не только от уровня артериального давления. Наличие сопутствующих факторов риска, степень вовлечения в процесс органов-мишеней, наличие ассоциированных клинических состояний имеет большее значение, чем степень повышения АД. В связи с чем, в современную классификацию введена стратификация больных в зависимости от степени риска. Клинические проявления сердечно-сосудистых заболеваний и поражения органов-мишеней рассматриваются как более сильные факторы, по сравнению с факторами риска (табл. 2).
Таблица 2. Стратификация общего СС риска на категории (низкий, средний, высокий и очень высокий риск) на основании САД и ДАД, наличия ФР, бессимптомного ПОМ, диабета, стадии ХБП и клинических ЗССС [1]
|
Другие факторы риска, бессимптомное ПОМ или заболевание |
Артериальное давление (мм рт. ст.) |
|||
|
Высокое нормальное САД 130-139 или ДАД 85-89 |
АГ 1 ст. САД 140-159 или ДАД 90-99 |
АГ 2 ст. САД 160-179 или ДАД 100-109 |
САД >= 180 или ДАД >= 110 |
|
|
Нет ФР |
Низкий риск |
Средний риск |
Высокий риск |
|
|
1-2 ФР |
Низкий риск |
Средний риск |
Средний/высокий риск |
Высокий риск |
|
≥3 ФР |
Низкий/средний риск |
Средний/высокий риск |
Высокий риск |
Высокий риск |
|
ПОМ, ХБП 3 стадии или СД |
Средний/высокий риск |
Высокий риск |
Высокий риск |
Высокий/очень высокий риск |
|
Клиническое ЗССС, ХБП 4 стадии и выше , при наличии ПОМ/РФ |
Очень высокий риск |
Очень высокий риск |
Очень высокий риск |
Очень высокий риск |
АД = артериальное давление; ХБП = хронические болезни почек; СС = сердечно-сосудистый; ЗССС = заболевания сердечно-сосудистой системы; ДАД = диастолическое давление; АГ = артериальная гипертензия; ПОМ = поражение органов-мишеней; ФР = факторы риска; САД = систолическое давление.
У пациентов с высоким нормальным АД при измерении в медицинском учреждении, но нормальным АД вне медицинского учреждения (“гипертензия белого халата”), особенно при отсутствии диабета, ПОМ, ЗССС или ХБП, риск ниже, чем при стабильной гипертензии и таких же показателях АД. У пациентов с гипертензией без симптомов и без наличия ЗССС, ХБП, СД, как минимум, требуется стратификация общего СС риска с использованием модели SCORE.
Ассоциированные (сопутствующие) клинические состояния
• Цереброваскулярное заболевание: ишемический инсульт, геморрагический инсульт, преходящее ОНМК.
• Заболевание сердца: инфаркт миокарда, стенокардия, коронарная реваскуляризация, ХСН.
• Заболевание почек: диабетическая нефропатия; почечная недостаточность (сывороточный креатинин > 133 мкмоль/л (> 1,5 мг/дл) для мужчин или > 124 мкмоль/л (> 1,4 мг/дл) для женщин; протеинурия (>300 мг/сут).
• Заболевание периферических артерий: расслаивающая аневризма аорты, поражение периферических артерий.
• Гипертоническая ретинопатия: кровоизлияния или экссудаты, отек соска зрительного нерва.
• Сахарный диабет.
Прогноз больных АГ и выбор тактики лечения зависят от уровня АД и наличия сопутствующих факторов риска, вовлечения в патологический процесс органов-мишеней, наличия ассоциированных заболеваний, в связи с чем, экспертами ВОЗ/МОАГ предложена стратификация риска по 4 категориям. Риск в каждой категории рассчитан по усредненному за 10 лет риску смерти от ССЗ, риску инсульта и инфаркта миокарда по результатам Фремингемского исследования (чем выше риск, тем хуже прогноз).
Группы риска
• Низкий риск (риск 1) – АГ 1 степени, нет факторов риска, поражения органов-мишеней и ассоциированных заболеваний. Риск развития ССЗ и осложнений в ближайшие 10 лет составляет 15%.
• Средний риск (риск 2) – АГ 2-3 степени, нет факторов риска, поражения органов-мишеней и ассоциированных заболеваний. 1-3 ст. АГ, есть 1 или более факторов риска, нет поражения органов-мишеней (ПОМ) и ассоциированных заболеваний. Риск развития сердечно-сосудистых осложнений в ближайшие 10 лет составляет 15-20%.
• Высокий риск (риск 3) – АГ 1-3 степени, есть поражение органов-мишеней и другие факторы риска, нет ассоциированных заболеваний. Риск развития сердечно-сосудистых осложнений в ближайшие 10 лет – более 20%
• Очень высокий риск (риск 4) – АГ 1-3 степени, есть факторы риска, ПОМ, ассоциированные заболевания. Риск развития сердечно-сосудистых осложнений в ближайшие 10 лет превышает 30% (табл. 2).
Риск определяется на основании оценки сочетания уровня АД, наличия других факторов риска поражения органов-мишеней, сахарного диабета и установленных сердечно-сосудистых заболеваний (табл. 2).
Для стратификации по риску рекомендуется оценивать ряд факторов и состояний, влияющих на прогноз (табл. 3).
Таблица 3. Факторы (помимо АД в мед. учреждении), влияющие на прогноз и применяющиеся при определении общего СС риска в таблице 2 [1]
| Факторы риска |
|
Мужской пол |
|
Возраст (≥ 55 лет – мужчины, ≥ 65 лет – женщины) |
|
Курение |
|
Дислипидемия |
|
Общ. холестерин > 4,9 ммоль/л (190 мг/дЛ) и/или |
|
Липопротеиды низкой плотности >3,0 ммоль/л (115 мг/дЛ), и/или |
|
Липопротеиды высокой плотности: у мужчин <1.0 ммоль/л (40 мг/дЛ), у женщин < 1,2 ммоль/л (46 мг/дЛ), и/или |
|
Триглицериды >1,7 ммоль/л (150 мг/дЛ) |
|
Глюкоза плазмы натощак 5,6–6,9 ммоль/л (102-125 мг/дЛ) |
|
Нарушенная торерантность к глюкозе |
|
Ожирение (РВИ ≥30 кг/м2 (рост2)) |
|
Брюшное ожирение (обхват талии у мужчин ≥ 102 см, у женщин ≥88 см) |
|
Семейный анамнез ранних ЗССС (у мужчин <55 лет; у женщин <65 лет) |
|
Бессимптомное ПОМ |
|
Пульсовое давление (у пожилых) ≥ 60 мм рт.ст. |
|
Гипертрофия ЛЖ на ЭКГ (индекс Соколова-Лиона >3,5 мВ; RaVL >1,1 мВ; Корнельское произведение > 244 мВ*мс, или |
|
На ЭхоКГ: гипертрофия левого желудочка (ГЛЖ) [ИМЛЖ у мужчин >115 г/м2, у женщин >95 г/м2 (ППТ)] |
|
Утолщение стенки сонных артерий (ТИМ > 0,9 мм) или атеросклеротические бляшки |
|
Каротидно-бедренная СПВ >10 м/с |
|
Лодыжечно-плечевой индекс <0,9 |
|
ХБП со СКФ 30-60 мл/мин/1,73м2 (ППТ) |
|
Микроальбуминурия (30-300 мг/сут) или соотношение альбумин/креатинин (30-300 мг/г; 3,4-34 мг/ммоль) (предпочтительно в утренней моче) |
|
Сахарный диабет |
|
Глюкоза плазмы натощак ≥ 7 ммоль/л (126 мг/дЛ) в двух разных анализах, и/или |
|
Гликозилированный гемоглобин HbA1c >7% (53 ммоль/моль), и/или |
|
Глюкоза плазмы после нагрузки >11 ммоль/л (198 мг/дл) |
|
Ассоциированные ЗССС или заболевания почек |
|
ЗССС: ишемический инсульт, кровоизлияние в мозг, ТИА |
|
ЗКС: ИМ, ИБС, реваскуляризация миокарда с помощью АКШ или ЧКВ |
|
Сердечная недостаточность, включая недостаточность с сохранной ФВ |
|
Клиническое заболевание периферических артерий нижних конечностей |
|
ХБП со СКФ <30 мл/мин/1,73м2 (ППТ); протеинурия (>300 мг/сут) |
|
Ретинопатия: геморрагии или экссудаты, отек зрительного нерва |
Риск максимален при концентрической ГЛЖ: увеличение ИМЛЖ при соотношении между толщиной стенки и радиусом >0,42.
Прогноз больных АГ и выбор тактики лечения зависят от уровня АД и наличия сопутствующих факторов риска, вовлечения в патологический процесс органов-мишеней, наличия ассоциированных заболеваний.
ДИАГНОСТИКА АГ [1]
Этапы диагностики артериальной гипертонии по-прежнему включают:
1. Установление стабильности повышения АД.
2. Анамнез заболевания и жизни пациента.
3. Физическое исследование.
4. Лабораторно-инструментальные методы исследования.
Диагностика АГ и обследование пациентов проводятся в строгой последовательности, отвечая определенным задачам:
– определение стабильности повышения АД и его степени;
– исключение симптоматической АГ или идентификация ее формы;
– выявление наличия других факторов риска сердечно-сосудистых заболеваний и клинических состояний, которые могут повлиять на прогноз и лечение, а также отнесение больного к той или иной группе риска;
– определение наличия поражений “органов-мишеней” и оценку их тяжести.
Согласно международным критериям ВОЗ/МОАГ 1999 года, АГ определяется как состояние, при котором САД составляет 140 мм рт. ст. или выше и/или ДАД – 90 мм рт. ст. или выше у лиц, которые не получали антигипертензивную терапию.
Точность измерения артериального давления, и, соответственно, правильность установления диагноза и степени АГ, зависят от соблюдения правил по измерению АД.
Диагностические критерии.
1. Связь повышения АД с хронической нервно-психологической травматизацией, профессиональными вредностями.
2. Наследственная предрасположенность (40-60%).
3. Значительные колебания АД, особенно систолического, в течение суток. Кризовый характер течения.
4. Клинические признаки повышенной симпатикотонии, склонность к тахикардии, потливость, чувство тревоги.
5. Клинические, ЭКГ и рентгенологические признаки синдрома АГ.
6. Синдром Салюса-Гунна 1-3 степени на глазном дне.
7. Умеренное снижение концентрационной функции почек (изогипостенурия, протеинурия).
8. Наличие осложнений АГ (ИБС, ХСН, нарушение мозгового кровообращения).
Жалобы и анамнез
Медицинский анамнез. У больного с впервые выявленной АГ необходим тщательный сбор анамнеза, который должен включать:
– время постановки диагноза АГ, текущие и прошлые показатели АД, длительность существования АГ в анамнезе, а также результаты применявшегося ранее лечения антигипертензивными средствами, данные о приверженности или неприверженности к лечению, текущие антигипертензивные препараты, эффективность и побочные эффекты препаратов, наличие в анамнезе гипертонических кризов;
– анамнез о ЗССС, включая сопутствующие заболевания, данные о наличии симптомов ишемической болезни сердца (наличие ранней гипертензии и/или преждевременной ИБС являются важными первыми индикаторами о генетической предрасположенности к гипертензии и ЗССС и могут потребовать генетических тестов – по показаниям), сердечной недостаточности, заболевании клапанного аппарата, сердцебиении, обморочных состояний, неврологических проблем с особым акцентом на инсульты и транзиторные ишемические атаки, поражений периферических сосудов, сахарного диабета, подагры, нарушений липидного обмена, бронхообструктивных заболеваний, заболеваний почек, сексуальных расстройств и другой патологии, а также сведения о лекарственных препаратах, используемых для лечения этих заболеваний, особенно тех, которые могут способствовать повышению АД;
– выявление специфических симптомов, которые давали бы основание предполагать вторичный характер АГ (молодой возраст, тремор, потливость, тяжелая резистентная к лечению АГ, тяжелая ретинопатия, повышение уровня креатинина, спонтанная гипокалиемия);
– у женщин – гинекологический анамнез: связь повышения АД с беременностью, менопаузой, приемом гормональных контрацептивов, гормонально-заместительной терапией;
– тщательная оценка образа жизни, включая потребление жирной пищи, поваренной соли, алкогольных напитков, количественную оценку курения и физической активности, а также данные об изменении массы тела в течение жизни, спросить о никотиновой зависимости и дислипидемии, храпе, апноэ во сне, низкий вес при рождении;
– личностные и психологические особенности, а также факторы окружающей среды, которые могли бы влиять на течение и исход лечения гипертонической болезни, включая семейное положение, ситуацию на работе и в семье, уровень образования;
– семейный анамнез АГ, сахарного диабета, нарушений липидного обмена, ишемической болезни сердца, инсульта или заболеваний почек (упомянуть тип и продолжительность поражения почек);
– для выявления вторичной гипертензии: поликистоз почек – семейный анамнез; заболевания паренхимы почек – в анамнезе заболевания почек, ИМВП, гематурия, чрезмерное применение анальгетиков; прием лекарственных средств – оральные контрацептивы, карбеноксолон, капли для носа, кокаин, амфетамины, стероиды, нестероидные противовоспалительные препараты, эритропоэтин, циклоспорин; феохромоцитома – приступы потливости, головной боли, тревоги, сердцебиении; альдостеронизм – эпизоды мышечной слабости и спазмов; симптомы заболевания щитовидной железы.
После установления факта АГ следует провести обследование пациента на предмет исключения симптоматических АГ. Далее определяются степень АГ, риска и стадия заболевания.
Физикальное обследование
Физикальное обследование больного АГ направлено на определение ФР, признаков вторичного характера АГ и органных поражений.
– В положении стоя измеряется рост, вес, окружность талии (в положении стоя, измеряемое между краем последнего ребра и подвздошной костью), рассчитывается ИМТ [масса тела, (кг)/рост, (м)2].
– Оценка состояния сердечно-сосудистой системы, в особенности, размеров сердца, наличия патологических шумов, АД должно измеряться в соответствии с рекомендациями (дополнительное обследование для поиска поражения сосудов показано в том случае, если при измерении АД на обеих руках обнаруживается разница САД >20 мм рт.ст. и ДАД >10 мм рт.ст.), на периферических артериях должен быть измерен пульс в состоянии покоя (для определения частоты сокращений и аритмий, особенно фибрилляции предсердий), выявление патологических шумов в проекции почечных артерий, аускультация сонных артерий.
– Для выявления вторичной гипертензии: признаки синдрома Иценко-Кушинга; кожные проявления нейрофиброматоза (феохромоцитома); увеличение почек при пальпации (поликистоз); наличие шумов в проекции почечных артерий (реноваскулярная гипертония); шумы в сердце (коарктация и другие заболевания аорты, заболевание артерий верхних конечностей); снижение пульсации и АД на бедренной артерии, по сравнению с одновременным измерением АД на руке (коарктация и другие заболевания аорты, поражение артерий нижних конечностей); разница между АД на правой и левой руках (коарктация аорты, стеноз подключичной артерии).
– Признаки поражения органов-мишеней: головной мозг (нарушения подвижности или чувствительности), сетчатка (изменения на глазном дне), сердце (пульс, локализация и характеристики верхушечного толчка, аритмия, ритм галопа, хрипы в легких, периферические отеки), периферические артерии (отсутствие, ослабление или асимметрия пульса, холодные конечности, ишемические язвы на коже), сонные артерии (систолический шум).
Измерение АД в медицинском учреждении.
Точность измерения артериального давления, и, соответственно, правильность установления диагноза и степени АГ, зависит от соблюдения правил по измерению АД.
1. Для корректного измерения АД с целью классификации гипертензии необходимо соблюдать ряд условий, для исключения дополнительных прессорных нагрузок (табл. 4). Техника измерения.
Манжета накладывается на плечо таким образом, чтобы средняя часть пневмокамеры находилась над проекцией артерии. Между манжетой и поверхностью плеча должно помещаться два пальца (для детей и взрослых с маленьким объемом руки – один палец), а ее нижний край должен располагаться на 2,5 см выше локтевой ямки. Не рекомендуется накладывать манжету на ткань одежды, запрещено закатывать рукава с образованием сдавливающих валиков из ткани. Головка стетофонендоскопа фиксируется у нижнего края манжеты над проекцией плечевой артерии, причем не допускается создание значительного давления на кожу, а расположение головки под манжетой приводит к ошибкам в определении в первую очередь диастолического АД.
В ходе первого измерения АД (или перед ним) необходимо дополнительно провести оценку систолического АД пальпаторно. Пальпируется лучевая или плечевая артерии. При нагнетании воздуха в манжету фиксируются показания манометра в момент прекращения пульсаций артерии, как оценочное значение систолического АД, после чего компрессия продолжается еще на 30 мм рт.ст. Необходимо учитывать, что избыточно высокое давление компрессии вызывает дополнительные болевые ощущения и повышение АД.
Скорость снижения давления воздуха в манжете должна составлять 2–3 мм рт.ст. за секунду (или за время между последовательными сокращениями сердца). При давлении более 200 мм рт.ст. допускается увеличение этого показателя до 4–5 мм рт.ст. за секунду.
Появление первого тона соответствует систолическому АД (первая фаза тонов Короткова). Диастолическое АД определяют по моменту исчезновения тонов Короткова (пятая фаза). Определение диастолического АД по 4-ой фазе (момента резкого ослабления тонов) рекомендовано при проведении измерения АД у детей до 12–14-ти лет, беременных женщин, а также у пациентов с высоким минутным объемом сердца, обусловленным физической нагрузкой, заболеванием или физиологическими особенностями. Для контроля полного исчезновения тонов необходимо продолжить аускультацию до снижения давления в манжете на 15–20 мм рт.ст. относительно последнего тона.
При слабых тонах Короткова перед измерением целесообразно поднять руку и выполнить несколько сжимающих движений без значительных усилий.
2. Кратность измерений.
Повторные измерения проводятся с интервалом не менее 2-х минут.
Во время первого визита пациента необходимо измерить АД на обеих руках. При выявлении устойчивой значительной асимметрии (более 10 мм рт.ст. для систолического АД и 5 мм рт.ст. для диастолического АД), все последующие измерения проводятся на руке с более высокими цифрами. Разница показателей считается достоверной, если присутствует при одновременном измерении на обеих руках; при последовательном измерении разница может быть обусловлена перепадами АД. Если показатели АД на обеих руках отличаются значительно (>10 мм рт.ст.) и постоянно (что сопряжено с повышением СС риска), то необходимо использовать руку с более высоким показателем.
3. Затруднения при измерении артериального давления.
«Аускультативный провал» (резкое ослабление и исчезновение тонов после прослушивания первых двух-трех отчетливых тонов) может служить причиной серьезной недооценки систолического АД, если при первом измерении не проводится его пальпаторная оценка.
Нарушения ритма сердца. Необходимо пальпировать лучевую артерию для оценки степени неравномерности сокращений сердца в ходе измерений. При выраженной неравномерности необходимо ориентироваться на средние значения АД по результатам нескольких последующих измерений. При редких нерегулярных сокращениях ориентироваться на значения АД, полученные при эпизодах регулярного ритма.
Стенозирующие поражения артерий. При одностороннем поражении сосудов необходимо проводить измерение на контралатеральной руке, а при двустороннем поражении рекомендуется измерение на бедре. Для этого используется специальная бедренная манжета, при этом необходимо учитывать, что систолическое давление на бедре на 15–20% выше, чем на плече.
Повышенная ригидность крупных артерий. У пациентов старшей возрастной группы (старше 65 лет), а также у пациентов, длительное время страдающих сахарным диабетом, наблюдается повышенная ригидность крупных артерий, в некоторых случаях препятствующая их спадению при компрессии. При этом метод Н.С. Короткова дает завышение АД, т.е. «псевдогипертензию». Для ее исключения полезно одновременно с аускультацией определять АД пальпаторно и при отличии в систолическом АД более 15 мм рт.ст. провести определение ригидности плечевой артерии (например, ультразвуковыми методами). При выраженной ригидности определение АД возможно только инвазивным методом.
4. Наиболее частые ошибки, приводящие к неправильному измерению АД: использование манжеты, не соответствующей охвату плеча, малое время адаптации пациента к условиям кабинета, высокая скорость снижения давления в манжете, отсутствие контроля асимметрии АД, неиспользование пальпации при первом измерении АД, неправильное положение руки пациента.
Измерение АД вне медицинского учреждения подразделяется на амбулаторное измерение АД (АИАД) и домашнее измерение АД (ДИАД). Данное измерение позволяет более достоверно оценить существующее АД по сравнению с офисным АД. Артериальное давление вне офиса чаще всего оценивается с помощью АИАД или ДИАД (табл. 4). В диагностических целях АД требуется измерять ежедневно в течение, как минимум, 3–4 дней (предпочтительнее 7 дней), по утрам и вечерам. Измерения лучше производить в тихой комнате, в сидячем положении, при котором имеется опора для спины и руки, после 5 минут покоя. За раз производится 2 замера, с интервалом в 1-2 минуты; результаты следует сразу занести в дневник измерения АД. Однако результаты, предоставляемые пациентом, иногда могут быть недостоверными, этой проблемы можно избежать при помощи использования аппарата со встроенной памятью. Домашнее АД – это средний показатель всех результатов, за исключением результата утром первого дня наблюдения.
Таблица 4. Пороговые параметры гипертензии при измерении АД в офисе и вне офиса
| Категория | САД (мм рт.ст.) | ДАД (мм рт.ст.) | |
|
Офисное АД |
≥140 |
и |
≥90 |
|
Амбулаторное АД |
|||
|
a. в дневное время (период бодрствования) |
≥ 135 |
и/или |
≥85 |
|
b. в ночное время (во время сна) |
≥120 |
и/или |
≥70 |
|
c. суточное АД |
≥130 |
и/или |
≥80 |
|
Измерение в домашних условиях |
≥135 |
и/или |
≥85 |
В некоторых случаях самостоятельное измерение АД в домашних условиях невозможно (например, при когнитивных расстройствах, физической неспособности) или противопоказано (при тревожных или навязчивых состояниях). В этих случаях АИАД будет более уместным.
Амбулаторное измерение АД (АИАД) в настоящее время является эталоном диагностики вне офиса и дает дополнительную информацию о показателях АД ночью (табл. 4). АИАД выполняется с помощью портативного тонометра, обычно на недоминантной руке, в течение 24–25 часов таким образом, чтобы были зарегистрированы показатели АД в период активности и ночью во время сна. Первое измерение АД, сделанное в момент наложения портативного аппарата, не должно отличаться от полученного оператором показателя более чем на 5 мм рт.ст. В случае большего расхождения данных манжету необходимо снять и наложить снова. Пациент должен быть проинформирован, что он может сохранять обычный уровень активности, но при этом избегать высоких нагрузок, а в момент нагнетания манжеты остановиться и прекратить разговор и держать руку в неподвижном состоянии так, чтобы манжета находилась на уровне сердца. Пациент должен записывать симптомы и события, могущие повлиять на АД, а также время приема препаратов, приема пищи, начало и окончание сна. В клинической практике измерения обычно производятся каждые 15 мин в течение дня и каждые 30 мин – ночью. Следует избегать слишком коротких интервалов, так как это снижает точность среднесуточных показателей. Допустимо производить измерения через равные промежутки в течение дня и ночи, например, каждые 20 мин. Результаты загружаются в компьютер и подвергаются разнообразному анализу. Как минимум, 70% показателей АД в дневной и ночной период должны быть удовлетворительными, иначе исследование следует переделать. Наличие артефактов и показателей, выходящих за пределы чтений, послужили причиной многочисленных споров, но если имеется достаточное число удовлетворительных показателей, то только явно неверные показатели должны быть исключены при оценке. Надо заметить, что при нарушении сердечного ритма показатели будут неточными.
В клинической практике чаще всего используются показатели среднего дневного, ночного и суточного АД. Среднее дневное и среднее ночное АД можно вычислить с помощью дневника, где указывается время пробуждения и отхода ко сну.
Амбулаторное АД является более чувствительным прогностическим фактором, чем офисное АД, в плане симптоматических СС осложнений, например, заболеваний коронарных сосудов со смертельным исходом и инсультов. Значения дневного и ночного АД показали, что ночное АД обладает большей прогностической ценностью, чем дневное. Отношение ночного/дневного АД дает ценную информацию о СС осложнениях. Интересно заметить, что число СС осложнений систематически выше у пациентов с меньшим “падением” АД в ночное время, хотя из-за сложности воспроизведения данного феномена достоверность этих результатов ограничена. У пациентов с высоким уровнем ночного “падения” АД увеличен риск инсульта, органных поражений.
Существуют также дополнительные показатели, характеризующие прессорную нагрузку на органы-мишени, изменчивость АД, степень снижения АД в ночные часы, пульсовое АД и т.д. Они считаются дополнительными (по отношению к средним величинам АД) факторами риска развития сердечно-сосудистых осложнений и поражений органов-мишеней.
Измерение АД в домашних условиях. Чаще всего производится самостоятельное измерение АД, но для некоторых пациентов требуется помощь обученного медработника или членов семьи. В настоящее время не рекомендуется производить измерения приборами, надеваемыми на запястье, но их можно применять у пациентов с ожирением и крайне большим обхватом плеча. В диагностических целях АД требуется измерять ежедневно в течение, как минимум, 3–4 дней (предпочтительнее, 7 дней), по утрам и вечерам. Измерения лучше производить в тихой комнате, в сидячем положении, при котором имеется опора для спины и руки, после 5 минут покоя. За раз производится 2 замера с интервалом в 1–2 мин; результаты следует сразу занести в дневник измерения АД. Однако результаты, предоставляемые пациентом, иногда могут быть недостоверными, этой проблемы можно избежать при помощи использования аппарата со встроенной памятью. Домашнее АД – это средний показатель всех результатов, за исключением результата утром первого дня наблюдения. Для облегчения мониторинга можно использовать телемониторинг и программы для смартфонов. Интерпретация должна производиться под наблюдением врача.
По сравнению с офисным АД, ДИАД предоставляет несколько измерений, сделанных на протяжении нескольких дней, оно дает информацию о состоянии АД за более длительный период наблюдения, о вариабельности АД, является более дешевым, доступным и легко воспроизводимым методом. Однако в отличие от АИАД, ДИАД не отражает состояние АД во время рутинной повседневной деятельности или во время сна и не позволяет оценить колебания АД за короткий промежуток времени. Показатели АД в домашних условиях лучше отражают развитие СС осложнений и смертности, чем показатели АД в медучреждении.
Лабораторные исследования направлены на выявление дополнительных данных о наличии дополнительных факторов риска, поиск причин вторичной гипертензии и наличия ПОМ [1].
• Стандартные тесты: гемоглобин и гематокрит, глюкоза плазмы натощак, общий холестерин, ЛПНП, ЛПВП, триглицериды натощак, калий и натрий, мочевая кислота, креатинин сыворотки крови (с расчетом СКФ), анализ мочи (микроскопия, определение протеина с помощью тест-полосок, микроальбуминурия), ЭКГ.
• Дополнительные исследования (на основании анамнеза, осмотра и результатов стандартных анализов): гликозилированный гемоглобин (если глюкоза плазмы натощак >5,6 ммоль/л (102 мг/дл) или ранее существующий СД), количественное определение белка в моче (если экспресс-анализ положительный); концентрация натрия и калия в моче и их соотношение, суточное АИАД или ДИАД, эхокардиограмма, холтеровское мониторирование при наличии аритмии, ультразвуковое исследование сонных артерий, допплерография сосудов брюшной полости и периферических артерий, скорость пульсовой волны, осмотр глазного дна.
• Специальные исследования (чаще всего назначаемые узкими специалистами): Дополнительные исследования для оценки поражения головного мозга, сердца, почек и сосудов. Подтверждение диагноза вторичной гипертонии, заподозренной на основании анамнеза, физикального исследования или стандартных тестов Обязательны при осложненной гипертонии!
• Генетический анализ. Доказан наследственный характер амбулаторного АД. Описано несколько вариантов моногенной гипертонии, таких как глюкокортикоид-зависимый альдостеронизм, синдром Лиддля и другие. При этих состояниях мутации одного гена полностью объясняют патогенез развития АГ и определяют выбор подходов к ее лечению.
Инструментальные исследования
- Стандартные тесты: ЭКГ в 12 отведениях.
- Дополнительные исследования: суточное АИАД или ДИАД, эхокардиограмма, холтер-монитор при наличии аритмии, ультразвуковое исследование сонных артерий, допплерография сосудов брюшной полости и периферических артерий, скорость пульсовой волны, осмотр глазного дна.
- Специальные исследования (чаще всего назначаемые узкими специалистами): Обязательны при осложненной гипертонии!
Выявление субклинического поражения органов-мишеней:
В настоящее время доказано неблагоприятное прогностическое значение бессимптомного поражения органов-мишеней у пациентов, страдающих и не страдающих повышенным АД. Каждый из четырех маркеров ПОМ (микроальбуминурия, повышение скорости пульсовой волны (СПВ), гипертрофия левого желудочка (ГЛЖ) и атеросклеротические бляшки на сонных артериях) являются независимыми прогностическими факторами СС смертности, независимо от стратификации по SCORE. Поэтому в клинической практике рекомендуется оценивать ПОМ.
1. Сердце.
А. ЭКГ. Чувствительность метода в диагностике гипертрофии левого желудочка низкая, но тем не менее, гипертрофия левого желудочка, диагностированная на основании индекса Соколова-Лайона, является независимым сердечно-сосудистым фактором риска; позволяет также выявить перегрузку левого желудочка, указывающую на более высокий риск, ишемию миокарда, нарушения проводимости, дилатацию левого предсердия и аритмии, включая фибрилляцию предсердий. Холтеровское мониторирование проводят с целью диагностики аритмии, что является обязательным исследованием у всех больных с высоким АД.
Б. ЭХОКГ несмотря на определенные технические ограничения является более чувствительным методом диагностики гипертрофии левого желудочка и оценки сердечно-сосудистого риска: измерение толщины задней стенки левого желудочка и межжелудочковой перегородки, конечного диастолического размера левого желудочка, индекса массы миокарда левого желудочка (ИММЛЖ) определяет гипертрофию левого желудочка; повышенную частоту сердечно-сосудистых исходов позволяют предсказать концентрическая гипертрофия левого желудочка (характеризуется наиболее неблагоприятным прогнозом), эксцентрическая гипертрофия и концентрическое ремоделирование; диастолическая дисфункция в соответствии с последними эхокардиологическими рекомендациями должна комбинироваться с пульсовой тканевой допплерографией отверстия митрального клапана (соотношение Е/е`≥13 [5] сопряжено с повышенным СС риском, независимо от ИММЛЖ и относительной толщины стенки у пациентов с гипертензией), размер левого предсердия является независимым прогностическим фактором смертельного исхода, сердечной недостаточности и ишемического инсульта.
В. МРТ сердца проводится для оценки размера и массы ЛЖ в тех случаях, когда эхокардиография невозможна по техническим причинам или когда визуализация отсроченного усиления сигнала может повлиять на тактику лечения.
Г. Стресс МРТ сердца, перфузионная сцинтиграфия или стресс-эхокардиография для достоверной диагностики ишемии миокарда, если ЭКГ при нагрузке положительная или неоднозначная.
2. Кровеносные сосуды.
А. Сонные артерии измерением толщины интимы-медиа (ТИМ) и/или наличие атеросклеротических бляшек позволяют предсказать развитие инсульта и инфаркта независимо от традиционных факторов риска. ТИМ на уровне бифуркации сонных артерий отражает в основном наличие атеросклеротического поражения сосудов, а ТИМ на уровне общих сонных артерий – гипертрофию сосудов. Связь между ТИМ сонных артерий и сердечно-сосудистыми исходами непрерывна и порог повышения СС риска определяется произвольно. О наличии бляшки свидетельствует увеличение ТИМ более 1,5 мм или локальное увеличение толщины на 0,5 мм или на 50% по сравнению с соседними участками.
Б. Скорость пульсовой волны (увеличение скорости пульсовой волны более 12 м/с). Жесткость стенок аорты является независимым прогностическим фактором СС осложнений со смертельным исходом и без него у пациентов с гипертензией. Сонно-бедренная СПВ является “золотым стандартом” для определения увеличения жесткости аорты. Определение жесткости артерий позволяет перенести значительное число пациентов из средней группы риска в более высокую или низкую группу.
В. Лодыжечно-плечевой индекс (ЛПИ) измеряется либо с помощью автоматических приборов, либо с помощью допплера и тонометра. Низкий лодыжечно-плечевой индекс указывает на поражение периферических артерий и далеко зашедший атеросклероз, позволяет предсказать развитие СС осложнений, а также связан с приблизительно двукратным повышением 10-летней СС смертности и крупных коронарных исходов.
Г. Другие методы исследования существуют и применяются в основном с научными целями: увеличение содержания кальция в коронарных артериях, которое оценивают с помощью компьютерной томографии высокого разрешения, также является сердечно-сосудистым фактором риска, однако препятствиями к использованию метода служат ограниченная доступность и высокая стоимость; эндотелиальная дисфункция имеет прогностическое значение при некоторых сердечно-сосудистых заболеваниях, но ее информативность при АГ изучена недостаточно, кроме того методы анализа эндотелиального ответа на различные факторы остаются инвазивными и трудоемкими.
3. Почки. Критериями диагностики поражения почек при АГ являются снижение их функции и/или экскреция альбуминов с мочой. Почечную недостаточность в настоящее время классифицируют в соответствии со скоростью клубочковой фильтрации, рассчитанной по формуле MDRD, Кокрофта-Галта или СKD-EPI. У больных АГ, страдающих и не страдающих сахарным диабетом, микроальбуминурия (даже ниже пороговых значений) является фактором риска сердечно-сосудистых осложнений. Выявлена непрерывная связь между сердечно-сосудистой и общей смертностью, и значением коэффициента белок/креатинин мочи у мужчин (≥3,9 мг/г) и женщин (≥7,5 мг/г). Сочетание повышенной экскреции белка в моче и пониженной расчетной СКФ являются независимыми и кумулятивными (сочетание обоих факторов представляет больший риск, чем их наличие по отдельности) факторами риска по развитию осложнений со стороны ССС и почек как у пациентов с диабетом, так и среди общего населения. Произвольное пороговое значение креатинина 30 мг/г считается микроальбуминурией.
Таким образом, нарушения функции почек, которые диагностируют с помощью перечисленных выше параметров, часто встречаются у больных АГ и являются мощным фактором риска сердечно-сосудистых осложнений и смерти [6-11]. Поэтому всем пациентам с гипертензией рекомендуется производить расчет СКФ и проверять уровень микроальбуминурии в разовой порции мочи.
4. Осмотр глазного дна проводится с помощью фотографии сетчатки и интерпретации снимков офтальмологами, что повышает чувствительность анализа по сравнению с прямой офтальмоскопией/фундоскопией. Ретинопатия 3-й степени (геморрагии, микроаневризмы, экссудаты и “ватные очаги”) и 4-ой степени (признаки 3-ей степени плюс отек зрительного нерва и/или отек макулы) означают тяжелую степень ретинопатии и ассоциируются с высоким риском смертности. 1-я степень (фокальное или генерализованное сужение артериол) и 2-я степень (артериовенозные перекресты) соответствуют ранним стадиям ретинопатии и их прогностическое значение сомнительно.
5. Головной мозг. МРТ головного мозга (инсульт, бессимптомное поражения ГМ), адекватные тесты на когнитивную функцию.
Диагностика вторичных форм гипертензии (таблицы 5, 6)
Таблица 5. Клинические признаки и диагностика вторичной гипертензии [1]
|
Клинические показатели |
Диагностика |
||||
|
Распространенные причины |
Анамнез |
Осмотр |
Лабораторные исследования |
Исследования первого ряда |
Дополнительные/подтверждающие исследования |
|
Поражение паренхимы почек |
Анамнез инфекции мочевыводящих путей, обструкция, гематурия, злоупотребление обезболивающими, поликистоз почек в семейном анамнезе |
Образования/уплотнения в брюшной полости (поликистоз почек) |
Протеинурия, эритроциты, лейкоциты в моче, снижение СКФ |
УЗИ почек |
Детализированное обследование почек |
|
Стеноз почечной артерии |
Фибромышечная дисплазия: гипертензия молодого возраста (особенно у женщин) Атеросклеротический стеноз: внезапное начало АГ, ухудшение или затруднение контроля, острый отек легких |
Шум при аускультации почечных артерий |
Разница в длине почек в > 1,5 см (УЗИ почек), быстрое ухудшение функции почек (спонтанное или в ответ на блокаторы ренин-ангиотензи-альдостероновой системы) |
Двухмерная допплерография почек |
МРТ, спиральная КТ, внутриартериальная цифровая ангиография |
|
Первичный альдостеронизм |
Мышечная слабость, гипертензия в раннем возрасте в семейном анамнезе или СС осложнения до 40 лет |
Аритмии (при тяжелой гипокалиемии) |
Гипокалиемия (спонтанная или вызванная диуретиками), случайная находка опухоли надпочечников |
Соотношение альдостерона/ренина в стандартизованных условиях (при коррекции гипокалиемии и отмены препаратов, влияющих на РАА систему) |
Натриевая нагрузка, инфузия физраствора, супрессия флудрокортизоном или каптоприловый тест; КТ надпочечников; биопсия надпочечниковой вены |
|
Феохромоцитома |
Пароксизмы повышения АД или кризы при существующей гипертензии; головная боль, потливость, сердцебиение, бледность, феохромоцитома в семейеном анамнезе |
Кожные проявления нейрофиброматоза (пятна “кофе с молоком”, нейрофибромы) |
Случайная находка опухолей надпочечников (или вне надпочечников) |
Измерение конъюгированиных метанефринов в моче или свободных метанефринов в плазме |
КТ или МРТ брюшной полости и малого таза; сцинтиграфия мета-123 I-бензил-гуанидином; генетическое обследование на наличие мутаций |
|
Синдром Кушинга |
Быстрый набор веса, полиурия, полидипсия, психологические расстройства |
Типичный внешний вид (центральное ожирение, луноподобное лицо, стрии, гирсутизм) |
Гипергликемия |
Суточная экскреция кортизола с мочой |
Дексаметазоновая проба |
Таблица 6. Дифференциальный диагноз АГ [1]
| Клинические показатели | Диагностика | ||||
|
Распространенные причины |
Анамнез |
Осмотр |
Лабораторные исследования |
Исследования первого ря да |
Дополнительные/подтверждающие исследования |
|
Поражение паренхимы почек |
Анамнез инфекции мочевыводящих путей, обструкция, гематурия, злоупотребление обезболивающими, поликистоз почек в семейном анамнезе |
Образования/уплотнения в брюшной полости (поликистоз почек) |
Протеинурия, эритроциты, лейкоциты в моче, снижение СКФ |
УЗИ почек |
Детализированное обследование почек |
|
Стеноз почечной артерии |
Фибромышечная дисплазия: гипертензия молодого возраста (особенно у женщин) Атеросклеротический стеноз: внезапное начало АГ, ухудшение или затруднение контроля, острый отек легких |
Шум при аускультации почечных артерий |
Разница в длине почек в > 1,5 см (УЗИ почек), быстрое ухудшение функции почек (спонтанное или в ответ на блокаторы ренин-ангиотензин-альдостероновой системы) |
Двухмерная допплерография почек |
МРТ, спиральная КТ, внутриартериальная цифровая ангиография |
|
Первичный альдостеронизм |
Мышечная слабость, гипертензия в раннем возрасте в семейном анамнезе или СС осложнения до 40 лет |
Аритмии (при тяжелой гипокалиемии) |
Гипокалиемия (спонтанная или вызванная диуретиками), случайная находка опухоли надпочечников |
Соотношение альдостерона/ренина в стандартизованных условиях (при коррекции гипокалиемии и отмены препаратов, влияющих на РАА систему) |
Натриевая нагрузка, инфузия физраствора, супрессия флудрокортизоном или каптоприловый тест; КТ надпочечников; биопсия надпочечниковой вены |
|
Редкие причины |
|||||
|
Феохромоцитома |
Пароксизмы повышения АД или кризы при существующей гипертензии; головная боль, потливость, сердцебиение, бледность, феохромоцитома в семейном анамнезе |
Кожные проявления нейрофиброматоза (пятна “кофе с молоком”, нейрофибромы) |
Случайная находка опухолей надпочечников (или вне надпочечников) |
Измерение конъюгированных метанефринов в моче или свободных метанефринов в плазме |
КТ или МРТ брюшной полости и малого таза; сцинтиграфия мета-123 I-бензил-гуанидином; генетическое обследование на наличие мутаций |
|
Синдром Кушинга |
Быстрый набор веса, полиурия, полидипсия, психологические расстройства |
Типичный внешний вид (центральное ожирение, луноподобное лицо, стрии, гирсутизм) |
Гипергликемия |
Суточная экскреция кортизола с мочой |
Дексаметазоновая проба |
ЛЕЧЕНИЕ АРТЕРИАЛЬНОЙ ГИПЕРТОНИИ [1]
На сегодняшний день существуют общепринятые принципы антигипертензивной терапии:
1. Лечение должно проводиться постоянно, в течение всей жизни.
2. Комбинированная терапия.
3. Одно-, двукратное применение лекарств.
4. Предпочтение отдается антигипертензивным препаратам длительного действия.
5. Немедикаментозная коррекция АД.
В профилактике гипертензии изменение образа жизни играет ключевую роль. Несмотря на его важное значение при лечении гипертензии, изменение образа жизни не должно стать поводом для отсрочки медикаментозной терапии у пациентов с высоким риском. Клинические исследования свидетельствуют о том, что целенаправленная модификация образа жизни может быть эквивалентна лекарственной монотерапии для снижения АД [3], хотя низкая приверженность является большим недостатком. Соответствующие изменения образа жизни могут безопасно и эффективно отсрочить или предотвратить развитие АГ у здоровых людей, отсрочить или устранить потребность в медикаментозном лечении АГ 1-ой степени, а также снизить количество и дозы употребляемых препаратов у пациентов, принимающих лечение [4]. Помимо снижения АД, изменение образа жизни влияет на другие СС факторы риска и заболевания [5] (табл. 7).
Таблица 7. Сумма рекомендаций о модификации образа жизни [1]
| Рекомендации | Классa | Уровеньb,d | Уровеньb,e |
|
Рекомендовано ограничение потребления соли до 5-6 г/день |
I |
А |
B |
|
Рекомендовано ограничение употребления алкоголя до не более 20-30 г этанола в день (для мужчин) и 10-20 г/день – для женщин. |
I |
А |
B |
|
Рекомендовано увеличение потребления овощей, фруктов, нежирной молочной продукции. |
I |
А |
B |
|
При отсутствии противопоказаний рекомендуется снижение веса до РВИ 25кг/м2 и обхвата талии до < 102 см у мужчин и <80 см – у женщин. |
I |
А |
B |
|
Регулярная физическая активность – 30 мин умеренных динамических упражнений 5-7 раз в неделю. |
I |
А |
B |
|
Рекомендовано советовать всем курящим пациентам бросить курить и предложить им помощь в этом. |
I |
А |
B |
РВИ =росто-весовой индекс
a Класс рекомендаций
b Уровень доказательств
c Ссылки, поддерживающие уровни доказательств
Большая часть доказательств в пользу назначения антигипертензивных препаратов для снижения значительных СС исходов (фатальный и нефатальный инсульт, ИМ, сердечная недостаточность и другие причины СС смертности) получены в результате множества рандомизированных контролируемых исследований (чаще с плацебо-контролем), проводимых с 1965 по 1995 г. На их мета-анализ [6] ссылаются Рекомендации ESH/ESC за 2007 г.
Доказано, что диуретики (тиазиды, хлорталидон и индапамид), бета-блокаторы, антагонисты кальция, ингибиторы АПФ и блокаторы рецепторов ангиотензина – все подходят для начальной и поддерживающей терапии АГ, в виде монотерапии или в комбинациях. Некоторые классы препаратов предпочтительнее назначать в особых клинических состояниях [7] (табл. 8).
Таблица 8. Состояния, требующие выбора отдельных препаратов [1]
| Состояния | Препараты |
|
Бессимптомное поражение органов-мишеней |
|
|
ГЛЖ |
ИАПФ, антагонисты кальция, БАР |
|
Бессимптомный атеросклероз |
Антагонисты кальция, ИАПФ |
|
Микроальбуминурия |
ИАПФ, БАР |
|
Нарушение функции почек |
ИАПФ, БАР |
|
Симптоматические поражения ССС |
|
|
Перенесенный инсульт |
Любой препарат, эффективно снижающий АД |
|
Перенесенный инфаркт |
ББ, ИАПФ, БАР |
|
ИБС |
ББ, антагонисты кальция |
|
Сердечная недостаточность |
Диуретики, ББ, ИАПФ, БАР, антагонисты рецепторов металлокортикоидов |
|
Аневризма аорты |
ББ |
|
Фибрилляция предсердий (профилактика) |
Можно БАР, ИАПФ, ББ или антагонисты рецепторов металлокортикоидов |
|
Фибрилляция предсердий (контроль сокращений желудочков) |
ББ, антагонисты кальция (не-дигидропиридиновые) |
|
Терминальная почечная недостаточность/протеинурия |
ИАПФ, БАР |
|
Заболевания периферических артерий |
ИАПФ, антагонисты кальция |
|
Другие |
|
|
ИСГ (у пожилых) |
Диуретики, антагонисты кальция |
|
Метаболический синдром |
ИАПФ, антагонисты кальция, БАР |
|
Сахарный диабет |
ИАПФ, БАР |
|
Беременность |
Метилдопа, ББ, антагонисты кальция |
|
Представитель черной расы |
Диуретики, антагонисты кальция |
ИАПФ = ингибиторы ангиотензин-превращающего фактора; БАР = блокаторы ангиотензиновых рецепторов; ББ = бета-блокаторы; АД = артериальное давление; ИСГ = изолированная систолическая гипертензия; ГЛЖ = гипертрофия левого желудочка.
Каково же место бета-адреноблокаторов (БАБ) в лечение больных с артериальной гипертензией? Первые сообщения о гемодинамических эффектах бета-адреноблокаторов сделаны B. Prichard в 1964 г. За более чем 35-летний период изучения и применения этих препаратов накоплен значительный научный и практический материал. В настоящее время этим препаратам приписывают многочисленные физиологические эффекты: блокада адренорецепторов на уровне нейронов и действие на центральную нервную систему; устранение влияния катехоламинов на мембранную аденилатциклазу, посредством чего блокируется транспорт ионов кальция и снижается сократимость миокарда; антирениновый эффект; опосредованное влияние на барорецепторы, воздействие на постсинаптические периферические b-адренорецепторы, конкурентный антагонизм с катехоламинами за рецепторное связывание, повышение уровня простагландинов в крови. Широта использования, несомненная польза, многообразные эффекты препаратов этой группы явились основанием для присуждения Нобелевской премии по медицине в 1988 г. J. Black, G. Elion, и G. Hutchings за разработку и обоснование принципов лекарственной терапии b-адреноблокаторами.
Механизм действия препаратов связан с обратимым блокированием бета-адренергических рецепторов. Это общее свойство БАБ. Однако препараты различаются между собой по степени избирательности действия на различные виды данных рецепторов. С практической целью важно представлять основные b-рецепторные поля и эффекты b-адреноблокаторов (табл. 9).
Очевидно, что представительство b-адренорецепторов в тканях и органах многочисленно, что обусловливает широту их терапевтического действия и многообразие сфер клинического применения.
В 1980 г. L. Opie сформулировал требования к идеальному b-адреноблокатору: кардиоселективность, способность модулировать симпатический тонус, малая растворимость в липидах и отчетливая вазодилататорная способность. Все указанные свойства отражены в классификации b-блокаторов, знание которой позволяет эффективно использовать эти препараты для лечения сердечно-сосудистой патологии.
В практических целях целесообразно подразделять b-адреноблокаторы на следующие подгруппы:
Неселективные:
· Неселективные без собственной симпатомиметической активности – пропранолол, тимолол, надолол, соталол, хлоранолол, терталолол и др.
· Неселективные с собственной симпатомиметической активностью – окспренолол, пиндолол, пенбутолол, бопиндолол, алпренолол, картеолол и др.
· Неселективные с вазодилатирующими свойствами – картеолол, карведилол, пиндолол, л абеталол, нипрандилол и др.
Селективные:
· Кардиоселективные без собственной симпатомиметической активности – атенолол, метопролол, б етаксолол, бисопролол, эсмолол, талинолол, бевантолол и др.
· Кардиоселективные с собственной симпатомиметической активностью – ацебутолол, практолол, ц елипролол и др.
· Кардиоселективные с вазодилатирующими свойствами – целипролол, бевантолол и др.
Новые различного механизма действия – н ебиволол .
Альфа -, бета-адреноблокаторы – лабеталол, карведилол, проксодолол и др.
Таблица 9. Основные b-рецепторные поля и эффекты b-адреноблокаторов
|
Орган-мишень |
Класс рецепторов |
Эффект рецепторной блокады |
|
Сердце |
Бета-1 |
Уменьшение сократимости |
|
Почки |
Бета-1 |
Ингибирование выделения ренина |
|
Бронхи |
Бета-2 |
Констрикция |
|
Гладкая мускулатура – матки – кишечника – сосудов |
Бета-2 Бета-1 Бета-1 Бета-2 |
Констрикция Констрикция Констрикция коронарных артерий Констрикция |
|
Скелетная мускулатура |
Бета-2 |
Ингибирование гликогенолиза |
|
Жировая ткань – подкожная “белые” жировые клетки – висцеральная “коричневые” жировые клетки |
Бета-1,2,3 Бета-3 |
Ингибирование липолиза, отложение жира в липоцитах Подавление термогенеза |
|
Поджелудочная железа |
Бета -2 |
Подавление секреции инсулина, стимуляция ожирения |
|
Глаз – внутриглазное давление – секреция слезы |
Бета-1 Бета-2 |
снижение снижение |
|
– ренин – инсулин – глюкагон |
Бета-1>2 Бета-2 Бета-2 |
Ингибирование Ингибирование Ингибирование |
Кардиоселективные бета-блокаторы вследствие преимущественной блокады b1-рецепторов сердца вызывают меньше побочных эффектов со стороны сосудов (ухудшение кровообращения в конечностях у больных с облитерирующими заболеваниями), бронхов (бронхоспазм при обструтивных болезнях легких), почек (ухудшение функции) и поджелудочной железы (нарушение толерантности к углеводам), хотя при увеличении дозы эти различия нивелируются. По селективности b-адреноблокаторы можно распределить следующим образом: небиволол >бисопролол = бетаксолол > метопролол > атенолол >= талинолол > ацебутолол = целипролол. Состояния, при которых преимущество в назначении имеют селективные b-адреноблокаторы, включают: облитерирующие заболевания артерий, хронические обструктивные болезни легких, высокая физическая активность пациентов, сахарный диабет II типа, портальная гипертензия, беременность. Для некоторых БАБ характерна собственная симпатомиметическая активность, проявляющаяся наряду с b-блокирующим действием слабым агонистическим эффектом на те же рецепторы. Препараты, имеющие СМА, в меньшей степени уменьшают ЧСС и сердечный выброс в покое и во время сна, что важно для больных с недостаточностью кровообращения, препятствуют повышению периферического сосудистого сопротивления благодаря частичной стимуляции b-адренорецепторов в артериолах, в меньшей степени вызывают бронхоконстрикцию, не провоцируют ухудшение кровоснабжения почек и нарушения липидного обмена, обладают менее выраженным синдромом отмены. Перечисленные эффекты позволяют препаратам этой подгруппы избежать ряда нежелательных свойств b-адреноблокаторов и расширить показания для их применения. Однако эти препараты не увеличивают продолжительность жизни пациентов и не показаны пациентам с инфарктом миокарда [8-9].
БАБ различаются также по своей способности растворяться в липидах и делятся на жирорастворимые (пропранолол, метопролол) и водорастворимые (атенолол, соталол, налдолол). Промежуточное положение занимают бетаксолол и бисопролол. Жирорастворимые b-адреноблокаторы проникают через гематоэнцефалический барьер и выделяются через печень в большей степени, чем другие препараты. Это свойство обусловливает большее количество побочных эффектов со стороны ЦНС, чем это наблюдается при использовании гидрофильных препаратов. В то же время водорастворимые b-адреноблокаторы выделяются в основном через почки, поэтому при хронической почечной недостаточности требуется уменьшение их дозы.
На сегодняшний день одним из самых перспективных БАБ с максимально высокой кардиоселективностью и способностью стимулировать высвобождение оксида азота (NO) является небиволол [8] (рис. 1).
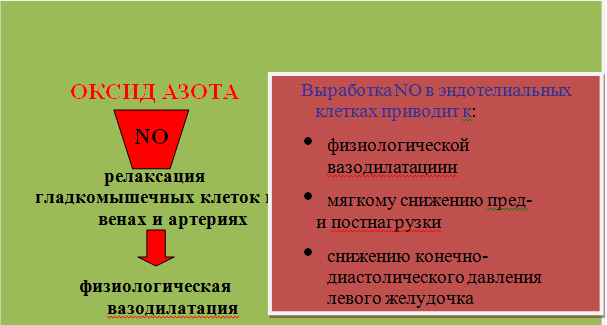
Рисунок 1. Схема этапов вазодилатации под влиянием небиволола
Специфическая прямая стимуляция продукции оксида азота доказана лишь для аргинина – непосредственного субстрата синтеза оксида азота и небиволола, молекула которого обладает уникальными свойствами воздействия на путь образования оксида азота из L-аргинина, что делает этот препарат чрезвычайно привлекательным с точки зрения использования во всех ситуациях, когда требуется β-блокада и имеется эндотелиальная дисфункция. В настоящее время эндотелиальная дисфункция рассматривается как один из важнейших компонентов патогенеза сердечно-сосудистых заболеваний, включая ИБС, артериальную гипертонию, сердечную недостаточность [10].
При артериальной гипертонии вазодилататорные свойства препарата дают ему существенные преимущества в отношении влияния на ремоделирование сердечно-сосудистой системы, обеспечивают отсутствие отрицательных метаболических эффектов, оптимальный профиль переносимости. Вазодилатационный эффект препарата имеет существенное клиническое значение не только с позиций нивелирования побочных эффектов лечения, свойственных β-блокаторам, но и с точки зрения возможного улучшения коронарного резерва сердца за счет вазодилатации.
Известно, что терапия АГ β-блокаторами снижает сердечно-сосудистую смертность и заболеваемость [11]. Тем не менее, данные мета-анализов показали, что уменьшение риска развития ИБС в группах пациентов с АГ, принимавших в качестве антигипертензивных препаратов β-блокаторы или диуретики, оказалось значительно меньше, чем ожидалось [12-14]. Предполагают, что данное несоответствие обусловлено негативными метаболическими эффектами β-блокаторов, такими как уменьшение чувствительности к инсулину, повышение уровня триглицеридов, снижение уровня холестерина липопротеидов высокой плотности, повышение массы тела, увеличение риска развития диабета [15]. Это положение отображено в Европейских рекомендациях по лечению артериальной гипертонии (2013), в которых указано, что β-блокаторы не следует назначать больным с сопутствующим метаболическим синдромом. Исключение составляют лишь вазодилатирующие препараты – небиволол и карведилол [16-17].
Небиволол – препарат, созданный с целью преодоления отрицательных метаболических эффектов β-блокаторов, сочетающий максимального высокую кардиоселективность и вазодилатирующий эффект, опосредованный модуляцией синтеза оксида азота эндотелиальными клетками. Под действием небиволола агонисты рецепторов, такие как ацетилхолин стимулируют выработку оксида азота в эндотелии. Достигая гладкомышечных клеток, NO активирует гуанилатциклазу, повышенное содержание которой приводит к расслаблению гладкомышечных клеток (рис. 2).
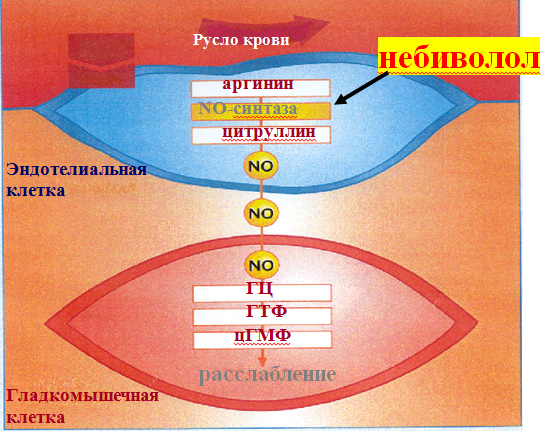
Рисунок 2. Механизм действия небиволола
По данным ряда клинических исследований, небиволол не только не обладает отрицательным воздействием на показатели углеводного и липидного обмена, но даже способен улучшать ряд метаболических параметров.
Список литературы:
1. ESH-ESC Guidelines Committee. 2013 guidelines for the management of arterial hypertension. J Hypertension 2013.
2. Elmer PJ, Obarzanek E, Vollmer WM, Simons-Morton D, Stevens VJ, Young DR, et al. Effects of comprehensive lifestyle modification on diet, weight, physical fitness and blood pressure control: 18-month results of a randomized trial. Ann Intern Med 2006; 144:485–495.
3. Elmer PJ, Obarzanek E, Vollmer WM, Simons-Morton D, Stevens VJ, Young DR, et al. Effects of comprehensive lifestyle modification on diet, weight, physical fitness and blood pressure control: 18-month results of a randomized trial. Ann Intern Med 2006; 144:485–495.
4. Frisoli TM, Schmieder RE, Grodzicki T, Messerli FH. Beyond salt: lifestyle modifications and blood pressure. Eur Heart J 2011; 32:3081–3087.
5. Perk J, De Backer G, Gohlke H, Graham I, Reiner Z, Verschuren M, et al. European Guidelines on cardiovascular disease prevention in clinical practice (version 2012): The Fifth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of nine societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Eur Heart J 2012; 33:1635–1701.
6. Collins R, Mac Mahon S. Blood pressure, antihypertensive drug treatment and the risks of stroke and of coronary heart disease. Br Med Bull 1994; 50:272–298.
7. Mancia G, De Backer G, Dominiczak A, Cifkova R, Fagard R, Germano G, et al. 2007 Guidelines for the Management of Arterial Hypertension: The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J Hypertens 2007; 25:1105–1187
8.Сидоренко Б.А., Преображенский Д.В. Бета-адреноблокаторы. Практическая кардиология. Москва. 1996 г. С.4.
9. Hansson L. Hemodynamics of metoprolol and pindolol in systemic hypertension with particular reference to reversal of structural vascular changes. // Am J Cardiol 1986; 57:29-32.
10. Мареев В.Ю. Изменение стратегии лечения хронической сердечной недос-таточности. Время В – адреноблокаторов. Кардиология, №12, 1998, с.4-11.
11. Беленков Ю.Н., Мареев В.Ю. Принципы рационального лечения сердечной недостаточности. 2000, изд. «Диа Медика», 263 с.
12. Рекомендации Американской коллегии кардиологов и Американской ассоциации сердца, 2001. Современные подходы к диагностике и лечению хронической сердечной недостаточности. Contemporary Approaches to Diagnosis and Management of Chronic Heart Failure (Summary of the American College of Cardiology/ American Heart Allocation Guidelines). Кардиология, №6, 2002, с. 65-78.
13. Рекомендации Европейского общества кардиологов. Экспертный комитет по разработке и проведению методических конференций с целью повышения качества лечения в европейских странах. Рекомендации по диагностике и лечению хронической сердечной недостаточности. Сердечная недостаточность, Т.2,2005, №6,с. 251-276.
14. Mac Mahon N.B., Cauman S. Effects of ACE inhibitors, calcium antagonists, and other blood lowering drugs: results of prospetivtly designed overviews of randomized trials, BPLTCT. Lancet. 2004; 345; 1076-78.
15. Messerli F.H., Grossman E., Goldbourt U. Are β-blocrtrs efficacious as first-line therapy for hypertension in the elderly? A systematic revieew. JAMA 1998; 279:1903-1907.
16. Messerli F.H., Grossman E.,Leonetti Antihypertensive therapy and new onset diabetes. J. Hypertens 2004; 22:1845-7.
17. ESH-ESC Guidelines Committee. 2013 guidelines for the management of arterial hypertension. J Hypertension 2013; 25: 1105-87.







