Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "Место тиотропиума бромида в лечении больных ХОБЛсогласно новым международным рекомендациям"
Автор: Юдина Л.В. доцент кафедры фтизиатрии и пульмонологии Национальной академии последипломного образования им. П.Л.Шупика, г. Киев, Украина.
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Пульмонология, Семейная медицина/Терапия
Просмотров: 2 900
Дата проведения:
 Хроническая обструктивная болезнь легких (ХОБЛ) относится к числу наиболее распространенных заболеваний человека. Распространенность ХОБЛ, по данным Всемирной организации здравоохранения (ВОЗ), составляет 9,3 на 1 тыс. населения среди мужчин и 7,3 на 1 тыс. населения – среди женщин старше 40 лет.Выделение хронической обструктивной болезни легких (ХОБЛ) в самостоятельную нозологическую единицу произошло относительно недавно и было связано с ростом частоты встречаемости, инвалидизации и, соответственно, затрат на лечение пациентов с этой патологией.ХОБЛ – прогрессирующее заболевание с не полностью обратимой бронхиальной обструкцией, возникающее под воздействием различных повреждающих факторов (главным из которых является курение) [1].
Хроническая обструктивная болезнь легких (ХОБЛ) относится к числу наиболее распространенных заболеваний человека. Распространенность ХОБЛ, по данным Всемирной организации здравоохранения (ВОЗ), составляет 9,3 на 1 тыс. населения среди мужчин и 7,3 на 1 тыс. населения – среди женщин старше 40 лет.Выделение хронической обструктивной болезни легких (ХОБЛ) в самостоятельную нозологическую единицу произошло относительно недавно и было связано с ростом частоты встречаемости, инвалидизации и, соответственно, затрат на лечение пациентов с этой патологией.ХОБЛ – прогрессирующее заболевание с не полностью обратимой бронхиальной обструкцией, возникающее под воздействием различных повреждающих факторов (главным из которых является курение) [1].
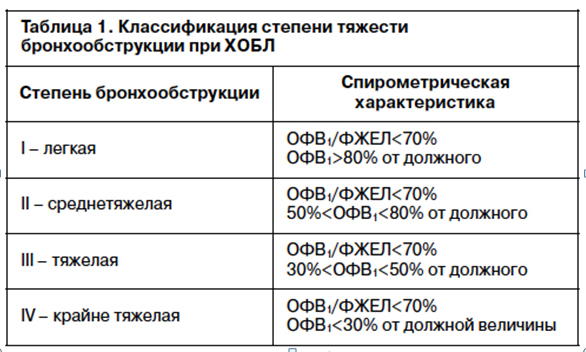
На начальных этапах изучения и разработки лечения ХОБЛ основное внимание уделялось лишь легочным ее проявлениям: необратимому либо не полностью обратимому ограничению скорости воздушного потока, главным показателем которого служил объем форсированного выдоха за первую секунду (ОФВ1). На основании этих данных в 2001 году был опубликован первый доклад в рамках Глобальной инициативы по хронической обструктивной болезни легких – TheGlobalInitiativeforChronicObstructiveLungDisease(GOLD) (1). В зависимости от выраженности бронхообструкции выделялись 4 степени (стадии) тяжести заболевания: легкое течение (I стадия), среднетяжелое (II стадия), тяжелое (III стадия) и крайне тяжелое (IV стадия) течение (табл. 1).
 Неуклонное падение скорости выдоха за 1-ю секунду у пациентов с ХОБЛ долгое время воспринималось как догма. Однако данные многочисленных, хорошо организованных исследований, проведенных в последнее время, заставили в значительной мере пересмотреть данный подход. Одной из таких ключевых работ явилось исследование ECLIPSE, в которое были включены 2163 пациента с ХОБЛ в возрасте от 40 до 75 лет с историей курения более 10 пачко-лет и имевшие постбронходилатационный ОФВ1<80% от должного, а отношение ОФВ1/ФЖЕЛ<0,7. В течение 3 лет измерялись изменения ОФВ1 и было установлено, что 38% пациентов имели падение данного показателя более чем на 40 мл в год, 31% – от 21 до 40 мл в год. При этом было отмечено, что у значительного числа пациентов (23%) не было зафиксировано достоверного падения (изменение ОФВ1 от -20 мл до +20 мл в год), а у 8% и вовсе отмечен рост данного показателя более чем на 20 мл в год, что никоим образом не вписывалось в концепцию необратимого снижения скоростных показателей спирометрии у данных пациентов [11]. В результате было сделано важное заключение, что ХОБЛ не является безусловно прогрессирующим заболеванием. У более чем 1/2 пациентов в данном исследовании уровень падения ОФВ1 не отличался от такового у людей без заболевания легких. Было отмечено, что скорость падения скоростных показателей спирометрии была выше у курящих пациентов, при наличии положительного бронходилатационного ответа – и у пациентов с эмфиземой. К тому же многие клиницисты и на своем опыте отмечали, что ХОБЛ – это комплексное и гетерогенное заболевание и его клинические проявления далеко не всегда коррелируют с изменением ОФВ1, что было подтверждено в ходе клинических исследований [12]. Более того, было продемонстрировано, что есть лишь слабая корреляция между симптомами заболевания, статусом здоровья пациента и спирометрическими показателями [15].
Неуклонное падение скорости выдоха за 1-ю секунду у пациентов с ХОБЛ долгое время воспринималось как догма. Однако данные многочисленных, хорошо организованных исследований, проведенных в последнее время, заставили в значительной мере пересмотреть данный подход. Одной из таких ключевых работ явилось исследование ECLIPSE, в которое были включены 2163 пациента с ХОБЛ в возрасте от 40 до 75 лет с историей курения более 10 пачко-лет и имевшие постбронходилатационный ОФВ1<80% от должного, а отношение ОФВ1/ФЖЕЛ<0,7. В течение 3 лет измерялись изменения ОФВ1 и было установлено, что 38% пациентов имели падение данного показателя более чем на 40 мл в год, 31% – от 21 до 40 мл в год. При этом было отмечено, что у значительного числа пациентов (23%) не было зафиксировано достоверного падения (изменение ОФВ1 от -20 мл до +20 мл в год), а у 8% и вовсе отмечен рост данного показателя более чем на 20 мл в год, что никоим образом не вписывалось в концепцию необратимого снижения скоростных показателей спирометрии у данных пациентов [11]. В результате было сделано важное заключение, что ХОБЛ не является безусловно прогрессирующим заболеванием. У более чем 1/2 пациентов в данном исследовании уровень падения ОФВ1 не отличался от такового у людей без заболевания легких. Было отмечено, что скорость падения скоростных показателей спирометрии была выше у курящих пациентов, при наличии положительного бронходилатационного ответа – и у пациентов с эмфиземой. К тому же многие клиницисты и на своем опыте отмечали, что ХОБЛ – это комплексное и гетерогенное заболевание и его клинические проявления далеко не всегда коррелируют с изменением ОФВ1, что было подтверждено в ходе клинических исследований [12]. Более того, было продемонстрировано, что есть лишь слабая корреляция между симптомами заболевания, статусом здоровья пациента и спирометрическими показателями [15].
При внешней привлекательности и простоте предыдущей классификации, а также при анализе приведенных результатов исследований стало очевидным, что степень ограничения воздушного потока далеко не всегда определяет тяжесть течения ХОБЛ (а, соответственно, и необходимый объем терапии). Поэтому от данной классификации, основанной исключительно на показателях спирометрии, в GOLD пересмотра 2011 года было предложено отказаться.В этом документев 2011 г. (а в дальнейшем в редакции GOLD пересмотра 2013 г.) были внесены значительные изменения, заключающиеся в следующем:
1) отказаться от стадийности ХОБЛ, а разделение по ОФВ1 называть степенями тяжести бронхиальной обструкции;
2) разделить пациентов на четыре группы в зависимости от выраженности симптомов и прогноза обострений в будущем, предлагая медикаментозное лечение для каждой группы;
3) симптомы оценивать по тесту CAT и шкале mMRC;
4) прогноз обострений делать на основании оценки предыдущих обострений и тяжести бронхиальной обструкции.
По данным GOLD пересмотра 2011–2013 гг., для характеристики ХОБЛ предложено: оценивать
- симптоматику заболевания;
- выраженность ограничения воздушного потока;
- риск обострений;
- вклад коморбидных состояний.
Таким образом, оценка ХОБЛ перестала быть линейной, а стала комплексной, как это представлено в табл. 2.
Таблица 2. Новая классификация ХОБЛ.
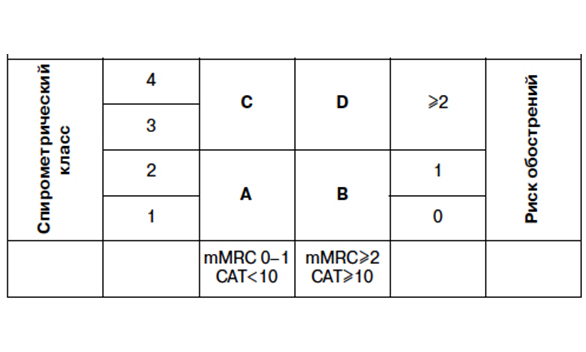
Главную роль в обосновании необходимости пересмотра предыдущей классификации ХОБЛ сыграли проведенные за последние 5 лет рандомизированные исследования, показавшие слабую корреляцию между значением ОФВ1 и симптомами заболевания, ответом на терапию и прогнозом, выявившие также большую гетерогенность среди больных той или иной стадии ХОБЛ [3]. На первый план в определении прогноза прогрессирующего снижения функциональных показателей [4], статуса здоровья [5] и смертности выступают обострения заболевания [6].
Следуя рекомендациям данного пересмотра и делая упор на симптоматике заболевания для разделения по группам и, соответственно, разделяя при этом лечение, врачам непременно надо принимать во внимание субъективность жалоб и их возможное несоответствие функциональным показателям легких. Наконец, при использовании новой классификации необходимо учитывать фенотипы пациентов, так как это напрямую сказывается на выборе лечения.
Одной из основных целей лечения ХОБЛ является воздействие на повышенное бронхиальное сопротивление в результате сужения просвета бронхов, в основе которого лежат воспалительные изменения слизистой дыхательных путей, бронхоконстрикция, как следствие сокращения гладких мышц, присутствие мокроты в просвете дыхательных путей и ремоделированиелегочнойткани.Соответствующая фармакотерапия позволяет уменьшить выраженность симптомов ХОБЛ, снизить частоту и тяжесть обострений и улучшить общее состояние здоровья и переносимость физической нагрузки. Схему фармакотерапии следует подбирать индивидуально в каждом конкретном случае в зависимости от степени выраженности симптомов, риска осложнений, доступности лекарственных препаратов и ответа пациента на проводимое лечение.Среди сегодняшних возможностей в лечении больных ХОБЛ наиболее важной остается бронходилатационная терапия, которая последние годы непрерывно совершенствуется. Появляются новые более удобные медленно высвобождающиеся лекарственные формы, средства доставки ингаляционных продуктов, комбинированные препараты.
В настоящее время согласно международным согласительным документам GOLD, рекомендациям Американского торакального общества/Европейского респираторного общества по диагностике и лечению применение бронхолитиков является терапией первой линии в лечении больных ХОБЛлюбой группы (тал.3).
Таблица 3.Ведение пациентов с ХОЗЛ: фармакологические подходы.
|
Пациент |
Первый выбор |
Второй выбор |
Альтернативный выбор |
|
|
A |
БАКДили М-ХЛКД по треб. |
БАКДиМ-ХЛКД БАДД или М-ХЛДД |
теофиллин |
|
|
B |
БАДД или М-ХЛДД |
БАДД или М-ХЛДД |
теофиллин БАКДилиМ-ХЛКД БАКДиМ-ХЛКД |
|
|
C |
ИКС + БАДД илиМ-ХЛДД |
БАДД или М-ХЛДД |
теофиллин БАКДи/илиМ-ХЛКД ФДЕ4-инг. |
|
|
D |
ИКС + БАДД илиМ-ХЛДД |
ИКС + БАДДи М-ХЛДД ИКС + БАДД и ФДЕ4-инг. М-ХЛДД иФДЕ4-инг. ИКСиМ-ХЛДД БАДД и М-ХЛДД |
теофиллин БАКДи/илиМ-ХЛКД Карбоцистеин |
Примечание: БАГК – бета 2 –агонисты короткого действия
М-ХЛКД – М-холинолитики короткого действия
БАДД – бета – 2 агонисты длительного действия
М-ХЛДД – М-холинолитики длительного действия
ИКС – ингаляционные кортикостероиды
ФДЕ4-инг. – ингибиторы фосфодиэстеразы – 4
Как видно из таблицы, холинолитические препараты присутствуют на всех этапах лечения пациентов ХОБЛ. Тиотропия бромид относится к группе М–холинолитиков.Препарат отличается сверхдлительным (более 24 ч) бронхолитическим эффектом, благодаря которому тиотропий может назначаться 1 раз в сутки. На сегодняшний день тиотропиума бромид является наиболее активным препаратом в ряду холинолитиков:по своей холинолитической активности он в 12 раз превосходит атропин и на 20–30% более активен, чем ипратропиуми аклидиниум бромид.
Все М–холинолитики являются неселективными препаратами, т.е. они блокируют М–холинорецепторы всех подтипов. Приэтом блокада М1– и М3–рецепторов способствует расширениюбронхов и обеспечивает лечебный эффект препаратов, а блокада M2–рецепторов является нежелательной, т.к. этот подвид холинорецепторов отвечает за торможение сигнала в синапсах.Тиотропия бромид отличает очень кратковременная блокадаМ2–рецепторов (Т½ связи с M2–рецепторами у тиотропия всего3,6 ч), в то время как блокада M1 и M3–рецепторов продолжаетсябольше 1 суток. [20].
Основной точкой приложения холинолитиков является их влияние на холинергическую иннервацию бронхов, определяющую бронхомоторный тонус в покое у больных ХОБЛ. Холинергические пути могут быть активированы как внешними раздражителями (табачный дым и загрязняющие вещества окружающей среды), так и медиаторами воспаления. Афферентные сигналы при этой активации передаются от гортани, пищевода и легких, а эфферентные – по блуждающему нерву. Холинергические волокна блуждающего нерва передают сигналы в парасимпатические ганглии, находящиеся в стенках бронхов, вследствие чего постганглионарные пути высвобождают ацетилхолин (АцХ). Высвобождение АцХ в клетки гладкой мускулатуры бронхов и подслизистых желез вызывает сужение просвета бронхов и секрецию слизи [18]. Положительные эффекты холинолитиков объясняются их влиянием на повышенный холинергический тонус дыхательных путей у пациентов ХОБЛ, который приводит к сужению их просвета. Холинергический тонус оказывает большее влияние на сопротивление дыхательных путей и является важным компонентом обратимости бронхиальной обструкции при ХОБЛ, а антихолинергические препараты обладают мощным бронхорасширяющим эффектом.
У больных ХОБЛ основные патологические изменения происходят на уровне мелких периферических дыхательных путей, которые в большей степени повреждаются под воздействием табачного дыма и нейтрофильного воспаления. Эти измененияносят необратимый характер. Но наряду с этим больных ХОБЛ отличает повышенный тонус парасимпатической системы, что приводит к сужению крупных бронхов (общее сопротивление дыхательных путей определяется главным образом центральными бронхами, так как их суммарный просвет – около 2 см2 – значительноменьше общего просвета периферических бронхов) и повышениюобщего сопротивления дыхательных путей [21]. Воздействуя на холинорецепторы центральных бронхов, тиотропиум бромид устраняет влияние парасимпатической нервной системы, крупные бронхи расширяются, а общее сопротивление дыхательных путей – снижается. В итоге уменьшается остаточная емкость легких и увеличивается дыхательный объем. Как следствие, у больных уменьшаетсяодышка, им легче выполнять физические нагрузки [22].После ингаляции тиотропиума бромида величина объема форсированного выдоха за первую секунду (ОФВ1) увеличивается на 150–180 мл (по сравнению с плацебо) или на 103 мл по сравнению сгруппой контроля, получавшей терапию β2–агонистами и ингаляционными ГКС [23]. Еще в большей степени тиотропиум бромидустраняет так называемую «воздушную ловушку», т.е. уменьшаетобъем воздуха, который остается в легких больного после максимального выдоха [24]. В результате препарат увеличивает дыхательный объем, уменьшает выраженность одышки, повышает переносимость физической нагрузки [25] и снижает связанную с нагрузкойконцентрацию катехоламинов в крови [26].
Положительное влияние тиотропия не ограничивается функцией внешнего дыхания – он значимо (на 38–44%) уменьшает число обострений ХОБЛ [27, 28] и на 12–16% – летальность от любыхпричин у больных ХОБЛ [23, 29].
Эффективность бронходилататоров в терапии ХОБЛ доказана результатами многоцентровых двойных слепых плацебо контролируемых исследований. Выбор бронхолитика имеет важное значения для длительной терапии пациентов ХОБЛ. Однако прием бронхорасширяющих препаратов может приводить к возникновению нежелательных эффектов со стороны сердечно-сосудистой системы. Некоторые препараты обладают аритмогенным и положительным хронотропным действием, могут ухудшать кровоснабжение миокарда, провоцируя ишемию. Такие осложнения чаще развиваются на фоне терапии метилксантинами и β2-агонистами. Поэтому особое внимание следует уделять пациентам ХОБЛ с сопутствующей ишемической болезнью сердца, т. к. при сочетании ИБС и ХОБЛ происходит взаимное отягощение течения этих патологий и более быстрое их прогрессирование. Метаанализ ряда рандомизированных плацебо контролируемых исследований, посвященных изучению влияния b2-агонистов при ХОБЛ, показал, что даже однократное применение этих лекарственных препаратов приводит к увеличению частоты сердечных сокращений (ЧСС) в среднем на 9 ударов в минуту. Также установлено, что при длительном приеме β2-агонистов риск возникновения синусовой тахикардии возрастает более чем в три раза. В ряде крупных международных исследований, проведенных в последние годы, в частности, CASS, IVEST показано, что ЧСС является независимым фактором риска как общей, так и кардиоваскулярной смертности. В исследовании BEAUTIFUL проанализирована связь сердечно – сосудистых исходов с базовой ЧСС. Увеличение ЧСС на каждые 5 ударов в минуту приводит к повышению риска смерти от сердечно – сосудистой патологии на 8%, госпитализаций в связи с сердечной недостаточностью на 16%, возникновения инфаркта миокарда на 7% (7). Поэтому ЧСС должна учитываться при выборе оптимальной консервативной терапии у больных с ХОБЛ с сочетанной патологией сердечно-сосудистой системы. Следует помнить, что b2-агонисты как короткого, так и длительного действия могут вызывать не только тахикардию, но и нарушение ритма, особенно при продолжительном применении. Длительный прием пролонгированных β2-агонистов может вызвать развитие гипокалиемии и других метаболических и электрофизиологических изменений, включая удлинение интервала QT. Тем ни менее, продолжительное использование ингаляционных β2 – агонистов длительного действия не сопряжено с ростом смертности.
К неблагоприятным свойствам β2-агонистов относится их селективность, которая зависит от величины принятой дозы, а также возможная потеря чувствительности (десенситизация) β2 – адренорецепторов при их частой повторной стимуляции. Если же воздействие высоких доз β2 – агониста осуществляется регулярно, то возможно стойкое снижение функциональной активности рецепторов (downregulation) преимущественно за счет уменьшения их количества/плотности на мембране миоцита. Способность через снижение плотности адренорецепторов приводить к их десенситизации в той или иной степени присуща всем β2 – агонистам.
В последние годы проводятся интенсивные исследования различных аспектов действия тиотропия, среди которых обострения являются наиболее важным фактором прогрессирования ХОБЛ и в последней редакции GOLD признаны одним из критериев оценки тяжести заболевания [17]. Именно поэтому, обострения являлись одной из важнейших изучаемых конечных точек в крупных исследованиях с использованием тиотропия бромида проведенных в последние годы.В одном из них – исследовании POET (PreventionofExacerbationswithTiotropiumin COPD) с участием 7376 пациентов с ХОБЛ изучалась способность тиотропия бромида предотвращать среднетяжелые и тяжелые обострения в сравнении с другим длительно действующим бронходилататором – салметероломвтечение1года[19].Подавляющее большинство исследований, посвященных тиотропиум бромиду, было выполнено с препаратом Спирива, где в качестве устройства доставки использовался дозированный порошковый ингалятор (ДПИ) ХандиХалер (суточная доза – 1 ингаляция по 18 мкг).Тиотропий показал способность значительно увеличивать время до первого обострения (первичная конечная точка) на 42 дня (187 и 145 дней в первой четверти пациентов) по сравнению с салметеролом. Отмечалось так же достоверное снижение риска развития обострения на 17% при проведении АХЭ терапии по сравнению с салметеролом (HR 0,83; 95% CI 0,77–0,90; p<0,001).
В настоящее время тиотропия бромид относится к базисным препаратам для длительной поддерживающей терапии ХОБЛ. Препарат улучшает функциональные легочные показатели, симптомы, физическую работоспособность, качество жизни больных ХОБЛ, уменьшает число обострений заболевания. В настоящее время только терапия тиотропиум бромидом продемонстрировала те преимущества, которые пока не были показаны при изучении всех других известных β2 – агонистов длительного действия: замедление прогрессирования заболевания, уменьшение летальности больных ХОБЛ, снижение риска сердечно – сосудистых событий и высокая эффективность препарата при всех изученных фенотипах ХОБЛ.Поэтому назначать холинолитики длительного действия пациентам с ХОБЛ сегодня рекомендуется начиная со 2-й стадии (клиническая группа В), когда еще можно предотвратить или существенно замедлить прогрессирование заболевания (34).
Субгрупповые анализы исследования UPLIFT позволили изучить эффективность терапии тиотропия бромида в отдельных фенотипах больных ХОБЛ (8 – 12). Фенотип – это «…характерная черта или комбинация таких черт, которые описывают различия между пациентами ХОБЛ, связанные с клинически значимыми исходами (симптомы, обострения, ответ на терапию, скорость прогрессирования заболевания или смерть)…»(13). Как уже говорилось, прием тиотропия бромида замедлил прогрессирование ХОБЛ у «наивных» больных, т.е. тех, которые ранее не получали этот препарат и у больных моложе 50 лет (9, 10). Кроме того, независимо от фенотипа ХОБЛ («наивные» больные, больные моложе 50 лет, курильщики, бывшие курильщики, мужчины и женщины) терапия тиотропия бромидом приводила к заметному стойкому улучшению показателей ОФВ1 и форсированной жизненной емкости легких, снижению числа обострений и улучшению качества жизни (9 -12).
Согласно современным международным и национальным рекомендациям по лечению ХОБЛ любой из ДДБД – тиотропий, или формотерол, или салметерол – должен назначаться всем больным ХОБЛ, начиная со средней степени тяжести заболевания (II стадия по классификации GOLD) [1]. Однако только терапия тиотропием продемонстрировала те преимущества, которые пока не были показаны при изучении всех других известных ДДБД:
- замедление прогрессирования ХОБЛ;
- уменьшение летальности больных ХОБЛ;
- снижение риска сердечно-сосудистых событий;
- высокая эффективность при всех изученных фенотипах ХОБЛ.
При тяжелом течении ХОБЛ, когда требуется комбинациянескольких препаратов, тиотропий можно эффективно сочетатьс препаратами других фармацевтических групп. В частности,тиотропий выступает как синергист β2–агонистов длительногодействия [30], т.к. на фоне его приема увеличивается чувствительность β–адренорецепторов [31]. В ходе клинических исследований была доказана эффективность комбинации тиотропия срофлумиластом[32] и комбинированными препаратами, в состав которых входят β2–агонисты и ингаляционные ГКС (будесонид/формотерол) [33].
В качестве примера можно рассмотреть клиническую ситуацию, в которой был использован холинолитик длительного действия для базисной терапии ХОБЛ.
Этот клин.случай был опубликован в 2014 году. Показывает, как на фоне Спиривы у пациента с крайне тяжелой степенью обструкции улучшились показатели ФВД, (а не просто замедлилось падение ОФВ1). Его можно и убрать. Пусть решит заказчик.
Клинический случай.Несколько лет назад в нашу клинику обратился больной В., 58 лет с жалобами на выраженную одышку при малейшей физической нагрузке (не мог подняться на второй этаж), кашель с выделением слизисто – гнойной мокроты, слабость, периодически боли в сердце в течение 2 – 3 минут при физической нагрузке (подъем на лестницу, ускоренная ходьба). Больной курил с детства, в последние годы выкуривал по 1 пачке сигарет в сутки. Ежегодно заболевание обострялось 3 – 4 раза в году. Лечился антибиотиками, отхаркивающими препаратами, настоями трав, теофиллином. Ингаляционными бронхолитиками никогда не пользовался. При осмотре больной пониженного питания, отмечался цианоз кожных покровов, акроцианоз. Частота дыхания 22 в 1 минуту, ЧСС -102 в 1 минуту, АД – 160/95 мм рт.ст. Тоны сердца приглушены, небольшой акцент II тона на легочной артерии. Над легкими на фоне ослабленного дыхания выслушивались сухие свистящие хрипы. Живот без особенностей. При рентгенографии органов грудной полости в прямой (рис.1) и боковой проекции (рис.2) выявлена эмфизема легких и усиление легочного рисунка в проекции средней доли справа как следы перенесенной ранее пневмонии, плотная аорта.
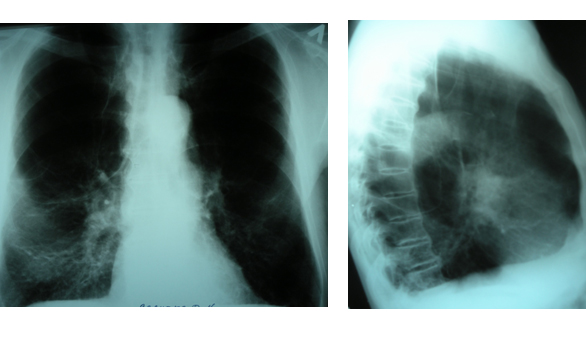
Рис.1 Рис.2
При первичном спирометрическом исследовании ОФВ1 составлял 19,2% от должных величин, что говорило о крайне тяжелой степени тяжести заболевания. При проведении бронхолитической пробы выяснилось, что у пациента отсутствует положительная реакция на β2– агонист короткого действия сальбутамол.
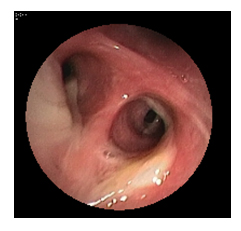
При поступлении в стационар больному В. была произведена лечебно – диагностическая фибробронхоскопия (ФБС), которая выявила диффузный гнойный эндобронхит (рис.3). Данную процедуру мы считаем очень важной и, по возможности, стараемся сделать ее возможно большему числу пациентов с легочными заболеваниями. Во-первых, это позволяет нам определить тип и степень воспаления и при показаниях назначить антибактериальную терапию. Во – вторых, с помощью ФБС мы можем просанировать (очистить) бронхиальное дерево, что совсем не лишнее при наличии обильного количества мокроты, ибо иногда это затрудняет проведение бронхолитического теста (бронхолитик просто не может попасть на слизистую оболочку дыхательных путей), а, следовательно, и дифференциальную диагностику.
Рисунок 3. Эндоскопическая картина больного В.: диффузный гнойный эндобронхит.
После клинико – рентгенологического исследования был выставлен диагноз (новой классификации еще не было): ХОБЛ, крайне тяжелая степень тяжести в фазе обострения. ИБС, стенокардия напряжения, II ФК, гипертоническая болезнь I, НК 0.
В стационаре обострение было снято путем назначения антибиотика (моксифлоксацин) в таблетированной форме, флутиказона 2000мкг и лазолвана 2,0 через небулайзер на протяжении 7 дней. Сальбутамол не назначался в виду отсутствия эффекта при проведении бронхолитического теста. Спирометрическое исследование показало улучшение функции внешнего дыхания (ФВД) (рис.4).
Рисунок 4. Спирометрическое исследование после выписки из стационара.
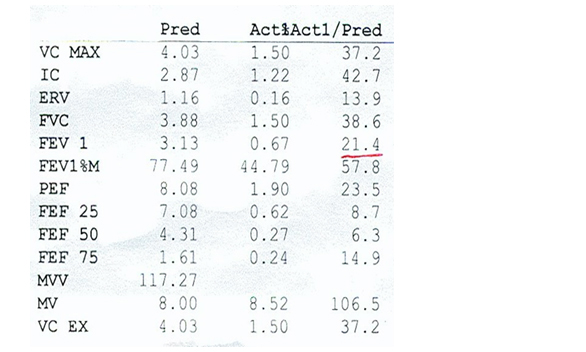
При первичном исследовании ОФВ1 составлял 19,2%, через 10 дней – 21,4% от должных величин. Дальнейшее лечение мы назначили исходя из рекомендаций GOLD и отечественных рекомендаций тех лет, изложенных в приказе МЗ Украины № 128.
ХОБЛ является заболеванием с многокомпонентной патофизиологией. Основу патогенеза ХОБЛ составляет хроническое диффузное, неаллергическое воспалительное поражение дыхательных путей (14,15). Предложенные схемы базисной терапии ХОБЛ предусматривают регулярный прием бронхолитических препаратов, а для борьбы с воспалением рекомендован прием глюкокортикостероидов, которые являются самыми мощными противовоспалительными препаратами. При крайне тяжелой степени ХОБЛ рекомендуется назначение одного или двух бронхолитических препаратов длительного действия разных групп (холинолитик и β2 – агонист) в сочетании с ингаляционным глюкокортикостероидом (ИГКС). В соответствии с рекомендациями GOLDрегулярный прием ИГКС больным ХОБЛ был показан в тех случаях, когда:
- у пациента по данным спирометрии отмечается их положительное влияние,
- у пациентов с объемом форсированного выдоха за первую секунду (ОФВ1) менее 50% и
- повторяющимися обострениями, требующими лечения антибиотиками или системными ГКС.
При современном уровне знаний (GOLD пересмотра 2011, 2013 г.г.) добавление ИГКС к бронхолитикам длительного действия также рекомендуется больным со средне – тяжелой и тяжелой степенью обструкции в клинических группах С и D. Важно учитывать, что лечение ИГКС является местным (топическим). Это обеспечивает выраженные противовоспалительные эффекты непосредственно в бронхиальном дереве при минимальных системных проявлениях. Длительное лечение ИГКС не влияет на долгосрочное прогрессирующее снижение ОФВ1 у пациентов с ХОЗЛ (11), однако в исследовании ISOLDE выявлено, что длительная терапия ИГКС способствует сокращению числа обострений.
Учитывая наличие ИБС, сопровождающейся тахикардией и опасаясь побочного действия β2 – агониста длительного действия, выбор для постоянного применения в качестве базисной терапии был сделан в пользу тиотропия бромида. Спириву назначили в дозе 18 мкг, т.е. 1 вдох 1 раз в день вместе с флутиказоном пропионатом по 500 мкг 2 раза в сутки. Одновременно назначен амлодипин по 5 мг 1 раз в сутки. Был рекомендован контрольный осмотр через 3 месяца.
При повторном осмотре больной чувствовал себя значительно лучше, у него уменьшилась одышка и слабость, легче стало ходить, кашель стал более редким. При контрольном спирометрическом исследовании оказалось, что показатели ФВД еще больше улучшились (рис.5).
Рисунок 5. Спирометрическое исследование больного В. через 3 месяца.

Данные спирометрии показали, что ОФВ1 увеличился до 26,1% (при выписке он составлял 21,1% от должных величин), уменьшилась обструкция на мелких бронхах (до лечения составляла 14,95 от должных, через 3 месяца – 16,7%). Соотношение ОФВ1/ФЖЕЛ, как и бывает у таких пациентов, было ниже 70 (57,1%).
Лечение пациенту оставили без изменений: Спирива 1 вдох в день в сочетании с флутиказоном по 500 мг 2 раза в сутки.
При очередном осмотре через 2 года оказалось, что за это время было только 1 обострение, одышка значительно уменьшилась, может выполнять несложную физическую работу, улучшилось качество жизни, связанное со здоровьем. Показатели внешнего дыхания улучшились (рис.6).
Рисунок 6. Спирометрические показатели больного В. через 2 года.
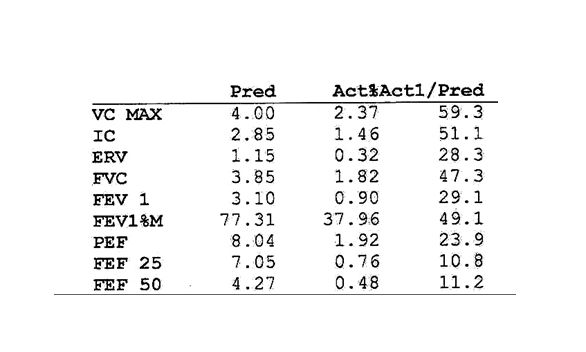 При приеме тиотропия бромида наблюдается замедление падения показателей ФВД, что характерно для больных ХОБЛ. Обращает на себя внимание, что у данного пациента ОФВ1 даже увеличился и составил 29,1% от должных величин, проходимость мелких бронхов также улучшилась (18,8%).
При приеме тиотропия бромида наблюдается замедление падения показателей ФВД, что характерно для больных ХОБЛ. Обращает на себя внимание, что у данного пациента ОФВ1 даже увеличился и составил 29,1% от должных величин, проходимость мелких бронхов также улучшилась (18,8%).
В настоящее время состояние больного удовлетворительное, обострения заболевания стали значительно реже (1 – 2 раза в году), уменьшилась одышка, работает сторожем. Следует отметить, что на протяжении последних пяти лет лечения пациент все – таки продолжает курить.
Как видно на примере данного клинического примера, возможности постоянной терапии бронхолитиками длительного действия (в первую очередь тиотропия бромид как патогенетически обоснованного препарата) в сочетании с ИГКС в лечении ХОБЛ не только ранних, но и поздних стадий, достаточно велики.
Поскольку у пациентов с ХОБЛ отмечается более высокий риск сердечно -сосудистых заболеваний, чем в среднем по популяции, аспект сердечно-сосудистой безопасности при лечении ХОБЛ имеет очень большое значение. Данные анализа 30 рандомизированных двойных слепых плацебо -контролируемых исследований с включением 19545 пациентов с ХОБЛ (тиотропия бромид – 10846, плацебо – 8699) показали отсутствие увеличения риска смерти вообще, или смерти вследствие сердечно – сосудистых осложнений у пациентов, получающих лечение препаратом СПИРИВА®(16).
СПИРИВА® воздействует на основной обратимый механизм бронхообструкции при ХОБЛ – холинергический бронхоспазм. СПИРИВА® – первый ингаляционный антихолинергический препарат пролонгированного действия, применение которого в виде одной дозы в день обеспечивает значительное и длительное улучшение легочных функций, облегчает дыхание пациентам с ХОБЛ, расширяет суженные воздушные пути и сохраняет их открытыми в течение 24 часов. СПИРИВА® позитивно влияет на клиническое течение ХОБЛ, помогая пациентам жить с их заболеванием.
В настоящее время препарат СПИРИВА® рекомендован для длительного применения в клинических группах B, С и D. У пациентов группы B его можно назначать в виде монотерапии или в сочетании с БАДД, а в группах С и D его следует сочетать с ИГКС или с комбинированным препаратом (β2 – агонист длительного действия/ИГКС).
Литература.
- Pauwels R. A., Buist A.S., Calverley P.M. et al. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease (GOLD) Workshop summary// Am J RespirCrit Care Med. 2001; 163: 1256 – 1276/
- Rabe K.F., Hurd S., Anzueto A. et al. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: GOLD executive summary //Am J RespirCrit Care Med. 2007; 176: 532 – 555.
- Agusti A., Calverley P.M., Celli B. et al. Characteristion of COPD heterogeneity in the ECLIPSE cohort //Respir Res. 2010; 11:122.
- Donaldson G.C., Seemungal T.A., Bhowmik A. et al. Relationship between exacerbation frequency and lung function decline in chronic obstructive pulmonary disease //Thorax 2002; 57: 847 – 852.
- Seemungal T.A., Donaldson G.C., Paul E.A. et al. Effect of exacerbation on quality of life in patients with chronic obstructive pulmonary disease // Am J RespirCrit Care Med. 1998; 157; 1418 – 1422.
- Coler-Cataluna J.J., Martinez-Garcia M.A., Roman Sanchez P. et al. Severe acute exacerbation and mortality in patients with chronic obstructive pulmonary disease //Thorax 2005; 60: 925 – 931
- Мостовой Ю.М. с соавт. Хроническое обструктивное заболевание легких и распространенные болезни сердечно-сосудистой системы: в фокусе внимания – кардиобезопасность. «Здоровье Украины», 2009, №9/1,:10 – 11.
8. Авдеев С.Н. Базисный препарат для терапии хронической обструктивной болезни легких. ConsiliumMedicumтом 13 / №3. .http://www.consilium-medicum.com/article/20624
9. Troosters T, Celli B, Lystig T et al. Tiotropium as a first maintenance drug in COPD: secondary analysis of the UPLIFT trial. EurRespir J 2010; 36: 65–73.
10. Morice AH, Celli B, Kesten S et al. COPD in young patients:
A pre-specified analysis of the four-year trial of tiotropium (UPLIFT). Respir Med 2010; 104: 1659–67.
11. Tashkin DP, Celli B, Kesten S et al. Long-term efficacy of tiotropium in relation to smoking status in the UPLIFT trial. EurRespir J 2010; 35: 287–94.
12. Tashkin DP, Celli B, Kesten S et al. Effect of tiotropium in men and women with COPD: Results of the 4-year UPLIFT trial. Respir Med 2010; 104: 1495–504.
13. Han MK, Agusti A, Calverley PM et al. COPD phenotypes: The future of COPD. Am J RespirCrit Care Med 2010; 182: 598–604.
- Global Initiative for Chronic Obstructive Lung Diseases. Global Strategy for the Diagnosis, Management and Prevention of Chronic Obstructive Pulmonary Disease. (Revised 2011). Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких. Пересмотр 2011 г. Перевод с англ. под ред. А. С. Белевского. М.: Российское респираторное общество, 2012.
15. Хроническая обструктивная болезнь легких. Практические рекомендации. Под ред. Чучалина А.Г., М.: Атмосфер, 2003
- Huiart L, Ernst P, Suissa S. Cardiovascular morbidity and mortality in COPD. Chest.2005;128:2640-2646.
- Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. Available from: http://www.goldcopd. org/guidelines-global-strategy-for-diagnosis-management.html. Revised 201.
- Barnes P.J. Managing Chronic Obstructive Pulmonary Disease. London: ScientificPressLimited, 1999.
- Vogelmeier C., Hederer B., Glaab T. et al. Tiotropium versus Salmeterol for the Prevention of Exacerbations of COPD. N Engl J Med. 2011; 364: 1093–103.
- Disse B et al. Life Sci 1993, 52: 537-44.
- Gross NJ, Co E, Skorodin MS. Chest. 1989 Nov;96(5):984-7.
- Buels KS, Fryer AD. HandbExpPharmacol. 2012;(208):317-41.
- Tashkin DP et al. UPLIFT Study Investigators. N Engl J Med 2008;359:1543-54
- Celli B, ZuWallack R, Wang S, Kesten S. Chest. 2003 Nov;124(5):1743-8.
- O’Donnell DE et al. EurRespir J. 2004 Jun;23(6):832-40.
- Yoshimura K et al. Int J Chron Obstruct Pulmon Dis. 2012;7:109-17
- Casaburi R et al. EurRespir J 2002; 19:217-224
- Vincken W et al. EurRespir J 2002; 19:209-216
- Celli В et al. CHEST 2010; 137(1): 20-30
- Van Noord JA, et al. EurRespir J. 2005;26:214-222
- Johnson M. Proc Am Thorac Soc. 2005;2(4):320-5
- Fabbri LM et al. Lancet. 2009;374(9691):695-703
- Aaron CD et al. Ann Intern Med. 2007;146:545-555.
- В.В. Архипов и др. РМЖ, 2013 1-4







