Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "Особенности подхода к диагностике и лечению рецидивирующих инфекций нижних мочевыводящих путей."
Автор: Гаджиева З.К., Аляев Ю.Г.
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Урология
Просмотров: 2 483
Дата проведения: с 27.05.2015 по 27.05.2016
 Актуальность проблемы
Актуальность проблемы
Расстройства мочеиспускания являются причиной ежегодного обращения к врачу около 3000000 женщин в США (Stamm W. E. et al., 1991, Foxman B., 2002). К ведущим причинам дизурии относится цистит, частота которого составляет 15–20 тыс. на 1 млн человек в год (Хайрлиев Г. 3., 1990). Около 30% женщин испытывают по крайней мере один эпизод цистита в течение жизни (Лоран О. Б. с соавт., 1996). Диагноз «рецидивирующий цистит» подразумевает 2 обострения цистита в течение 6 месяцев или 3 обострения в течение года (Guidelines on urological infections, European Association of Urology, 2010). Хронический цистит – заболевание, характеризующееся длительно существующей воспалительной реакцией в ткани мочевого пузыря (Даниленко В.Р.). Воспаление мочевого пузыря превалирует в структуре заболеваний мочевыводящих путей (Даниленко В.Р., 1995, Кан Д. В., 1978, Кан Д. В., 1982, Кузнецова H.H. с соавт., 2001). Проблема стойкой дизурии у женщин остается одной из наиболее актуальных в медицине. Это связано, прежде всего, с большой распространенностью хронического цистита у женщин, который составляет до 30% от всех урологических заболеваний (Ильинская Е.В., 2007). Ежегодно диагноз «цистит» ставят 15–20 тыс. из 1 млн человек, причем в той или иной форме заболевание переносит каждая 4–5-я женщина, а 10% больных страдают рецидивирующим циститом (Лоран О.Б. с соавт., 1998, Naber K.G. et al, 2008). От 40 до 50% женщин хотя бы раз в жизни имели эпизод острого цистита, а в постменопаузе – 8–10% (Perrotta Carla et al., 2008). Расстройства мочеиспускания у женщин, страдающих хроническими рецидивирующими инфекциями нижних мочевыводящих путей (ИНМВП), – серьезная проблема, решения которой, несмотря на большое количество работ, посвященных этой теме, до сих пор не найдено (Беднова В.Н. с соавт., 1993, Chew LD et al., 1999). В России ежегодно регистрируется около 36 млн случаев острого цистита, в то время как заболеваемость острым циститом в среднем составляет 0,5–0,7 эпизода заболевания на 1 женщину в год. Представления о восходящем пути инфицирования у женщин относятся к наиболее распространенным (Даниленко В.Р., 1995). Хронический рецидивирующий цистит охватывает в большинстве своем работоспособное население, может приводить к утрате трудоспособности и развитию неврозоподобного состояния, лишает женщин полноценного ночного сна и привычного образа жизни (Неймарк А.И., 2003). Для данного заболевания характерны возрастные колебания: в детородном возрасте оно встречается у 5% женщин, в период менопаузы – у 10–15%, в пожилом возрасте – у 15–20% (Кан Д.В. с соавт., 1988).
 Особенности диагностики
Особенности диагностики
Важно помнить, что под «маской» цистита могут протекать:
- опущение влагалища и мочевого пузыря;
- камни нижней трети мочеточника;
- опухоль мочевого пузыря;
- туберкулез мочевого пузыря;
- итерстициальный цистит;
- инородное тело мочевого пузыря;
- гиперактивный мочевой пузырь.
Предрасполагающими факторами в развитии цистита являются (Berg E, et al., 1996):
- естественные анатомо-физиологические особенности женского организма (короткий и широкий мочеиспускательный канал, близость к естественным резервуарам инфекции – анусу и влагалищу);
- активная половая жизнь;
- сопутствующие гинекологические заболевания, изменяющие нормальную экосистему влагалища (воспалительные процессы, гормональные нарушения);
- использование контрацептивов, содержащих спермициды;
- ослабление локальных антибактериальных механизмов мочеполовой системы;
- анатомические варианты и аномалии строения уретры;
- нарушения уродинамики нижних мочевых путей;
- низкий уровень гигиены;
- сухость слизистой оболочки в области уретры на фоне эстрогенового дефицита в климактерии.
В подавляющем большинстве случаев возбудителями острого цистита являются кишечная палочка (Escherichia coli), другие грамотрицательные энтеробактерии, а также коагулазонегативные стафилококки (Hooton T., Stamm W., 1997). Говоря о бактериурии, очень важно подчеркнуть, что обнаружение в моче даже первичных уропатогенов не является основанием для постановки окончательного диагноза. Для подтверждения «истинной» бактериурии необходимо доказать, что концентрация бактерий в моче достаточно высока.
Рисунок 1. Распределение основных бактериальных возбудителей инфекции мочевых путей (Л. Страчунский, В. Рафальский, 1999)
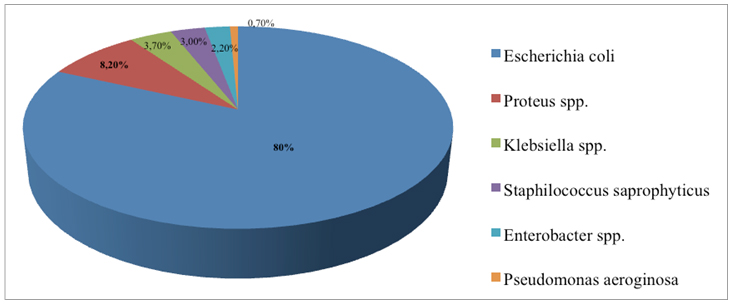
Клинически значимая бактериурия считается в случае выявления:
- монокультур E. coli и S. saprophyticus в титре ≥ 10³ КОЕ/мл;
- монокультур других бактерий в титре ≥ 104 КОЕ/мл;
- смешанных культур двух бактерий – в титре ≥ 105 КОЕ/мл.
Бессимптомная бактериурия является распространенным состоянием. В популяциях пациентов со структурными или функциональными нарушениями мочеполового тракта может наблюдаться очень высокая распространенность бактериурии, но даже и у здоровых лиц из мочи часто выделяются микроорганизмы. Бессимптомная бактериурия редко приводит к неблагоприятным последствиям.
Скрининг или лечение бессимптомной бактериурии не рекомендуется проводить в следующих группах:
- небеременные женщины в пременопаузальном периоде;
- женщины с сахарным диабетом;
- люди старческого возраста, проживающие дома пожилые люди, проживающие в домах престарелых;
- лица с поражением спинного мозга;
- пациенты с постоянным мочевым катетером.
Скрининг и лечение бессимптомной бактериурии рекомендуется проводить только у определенных групп пациентов, для которых были доказаны преимущества такого скрининга и лечения:
- беременные женщины;
- перед проведением трансуретральной резекции предстательной железы (ТУРП) и другими травматичными урологическими вмешательствами.
Антибактериальная терапия должна быть начата до проведения процедуры.
У беременных женщин без симптомов ИМВП бактериурия считается клинически значимой, если в 2-х последовательных образцах мочи, собранных во время самостоятельного мочеиспускания, обнаруживается одинаковый возбудитель в количестве более 105 КОЕ/мл или если в одном образце мочи, взятой катетером, концентрация уропатогена более 105 КОЕ/мл (EAU, 2011).
У беременных женщин с симптомами ИМВП бактериурия считается клинически значимой при концентрации уропатогена в образце мочи, собранном при самостоятельном мочеиспускании или взятом катетером, более 103 КОЕ/мл (EAU, 2011).
Механизмами защиты от инфекции мочевыводящих путей являются:
- кислая реакция мочи;
- механическое удаление бактерий потоком мочи;
- слизь в мочеиспускательном канале;
- клетки и антитела, задерживающие и уничтожающие бактерии.
Основными бактериальными агентами, обнаруживающимися в моче у пациенток, страдающих инфекцией мочевыводящих путей, по данным Л. Страчунского и В. Рафальского (1999) являются Escherihia coli, Proteus spp., Klebsiella spp., Staphilococcus spp. Результаты Международного исследования, выполненного в 252 клиниках 16 стран Европы и Канады – ECO-SENS Project, в котором обследованы 4734 женщины с неосложненной инфекцией мочевыводящих путей, явились практически аналогичными (G. Kahlmeter (2003)
Факторы, определяющие рецидивирование ИМВП (Foxman B., 2002, Hooton T. et al., 1996):
- биологические;
- поведенческие;
- урогенитальные.
Биологические факторы:
- ИМП в анамнезе;
- сахарный диабет 1-го типа;
- дефицит эстрогенов;
- наличие генетической предрасположенности.
Урогенитальные факторы:
- недержание мочи;
- врожденные пороки развития;
- оперативные вмешательства;
- обструкция мочевыводящих путей;
- детрузорно-сфинктерная диссинергия.
Поведенческие факторы:
- половой акт;
- использование в качестве контрацепции спермицидов и/или диафрагм;
- недавний курс антибиотикотерапии.
Важной проблемой является бессимптомная бактериурия у беременных, которая выявляется у 6% (2–11%) беременных (определена зависимость частоты развития бессимптомной бактериурии от социально-экономического положения беременных женщин). При отсутствии лечения у 40% из них развивается острый пиелонефрит. Бессимптомная бактериурия, несмотря на отсутствие клинических проявлений, может приводить к преждевременным родам, анемизации беременной, преэклампсии, гипотрофии новорожденного и внутриутробной смерти плода (Davison J. М., 1998). Риск рождения детей с низкой массой тела и преждевременных родов у беременных женщин с нелеченной бессимптомной бактериурией в 1,5 и 2 раза выше, чем у женщин без нее (Romero R., 1989). Бессимптомная бактериурия наиболее значима в развитии инфекций мочевыводящих путей между 9–17-й неделей беременности. Правильное назначение антибактериальной терапии бактериурии в ранних сроках беременности предотвращает развитие пиелонефрита в 70–80% случаев, а также 5–10% всех случаев недонашивания (Sweet R. L, 1977).
За последнее время, в литературе появились сообщения об увеличении количества пациентов с сохраняющимися расстройствами мочеиспускания, несмотря на нормализацию анализов мочи и прекращение бактериурии (Комяков Б.К. с соавт., 2004). Эффективное этиотропное лечение цистита не во всех случаях приводит к устранению симптомов нарушения мочеиспускания. Поэтому, для уточнения характера мочеиспускания и выбора дальнейшей тактики лечения у данных больных представляется целесообразным проведение уродинамических исследований нижних мочевыводящих путей (Gosling J.A. et al., 1986, Thuroff J. et al., 1991, Зубань О.Н., 2002, Хайрлиев Г.З., 1990, Gogus C. et al., 2000, Tawada T. et al., 1993, Гаджиева З.К., 2009). Выявляемые нарушения касаются как резервуарной, так и эвакуаторной функций мочевого пузыря. Причинами функциональных нарушений нижних мочевыводящих путей могут быть различные процессы, при которых нарушается нервная регуляция их деятельности. Однако значительно чаще встречаются и имеют большее значение расстройства мочеиспускания вследствие хронической мочевой инфекции, вызывающие стойкие изменения нервно-мышечного аппарата детрузора, сфинктеров и тазового дна (Возианов А.Ф. соавт., 1992).
Отсутствие единого системного подхода к оценке симптомов нижних мочевыводящих путей у пациентов, страдающих хроническим циститом, приводит к неправильной трактовке клинических проявлений заболевания и выработке ошибочных направлений лечебной тактики (Забиров К.И., 1997, Кан Д. В., 1986, Левин Е.И., 1991, Лоран О.Б. с соавт., 1997, Gillespie L., 1994). При назначении лечения больным с хроническим циститом часто не учитывается роль вегетативной нервной системы в регуляции сократительной функции мочевого пузыря. Согласно классической концепции нейрофизиологии моторная функция мочевого пузыря обеспечивается антагонистическим взаимодействием симпатического и парасимпатического отделов нервной системы. На сегодняшний день известно немало способов коррекции нарушений функции нижних мочевыводящих путей с применением холинергических и адренергических средств. Однако их системное действие делает их не всегда применимыми (Державин В.М. с соавт., 1977, Andersson K.E., 1988, Andersson K.E., 1993, Biggers R.D., 1986, Cetinel B. et al., 1994, Hinman F.J., 1988, Kinder R.B. et al., 1987, Pang X. et al., 1995, Perez-Marrero R. et al., 1987). По данным некоторых авторов (Неймарк А.Г., 2002), возникновение стойкой дизурии у женщин с хроническим циститом обусловлено развивающимися микроциркуляторными, морфологическими и уродинамическими нарушениями, приводящими к нарушению функции уротелия и повышению его проницаемости. В связи с этим для лечения хронического цистита показано комплексное использование различных групп препаратов. По нашим данным, по результатам выполненного уродинамического исследования у пациенток, страдающих хроническим рецидивирующим циститом, нестабильность уретры выявлена у 45,68% больных, гиперактивность детрузора – у 8,62%, сочетание гиперактивности детрузора и нестабильности уретры – у 22,4%, признаки детрузорно-сфинктерной диссинергии – у 25% (Гаджиева З.К., 2009).
Диагноз острого цистита устанавливается на основании симптомов (жалоб пациентки), анамнеза, лабораторного исследования мочи (микроскопического и культурального). Культуральное исследование (посев) мочи с определением чувствительности возбудителя при впервые возникшем остром неосложненном цистите не показано. Однако при рецидиве заболевания или неэффективности корректно назначенной терапии данное исследование является обязательным (EAU guidelines, 2010).
У женщин с сохраняющимися симптомами, или у женщин, у которых в течение 2-х недель после разрешения симптомов развился рецидив инфекции, следует провести культуральное исследование мочи с определением чувствительности выделенных возбудителей к антибиотикам (EAU).
Информация о профиле чувствительности к антибиотикам возбудителей неосложненных ИМВП должна определять выбор лечения, хотя тенденция к отказу от рутинного проведения культурального исследования мочи при неосложненном цистите, к сожалению, может приводить к потере таких данных. Однако профиль резистентности штаммов E. coli, вызывающих неосложненные ИМВП, может существенно различаться в разных странах и регионах Европы, поэтому не существует единых общих рекомендаций, которые можно было бы применять на территории всей Европы.
При наличии у женщины какого-либо из факторов, позволяющих заподозрить уретрит или вагинит, или при наличии сомнений относительно диагноза, проводится гинекологическое обследование. Гинекологическое обследование должно включать в себя тщательную оценку признаков вагинита, выделений из уретры и поиск герпетических язв; обследование шейки матки для выявления признаков цервицита, а также культуральное исследование материала из шейки матки и уретры на N. gonorrhoeae и C. trachomatis (или другие чувствительные и специфичные анализы с применением в качестве образца первой порции утренней мочи, такие как ПЦР).
Необходимо отметить, что есть категории больных, у которых инфекция мочевыводящих путей априори должна расцениваться как осложненная, и, соответственно, к этим пациентам не применимы диагностические и лечебные действия, показанные при неосложненном остром цистите.
Разделение ИМВП на неосложненные и осложненные является важным, поскольку они отличаются по методам исследования до и после лечения, типу и продолжительности антимикробной терапии и объему обследования мочевыделительной системы. В отличие от неосложненных ИМВП, осложненные ИМВП представляют собой инфекции, развивающиеся на фоне состояний, которые повышают риск развития инфекции или неэффективности терапии. На момент острого начала заболевания, проявляющегося симптомами со стороны мочевыводящих путей, обычно невозможно четко определить, является ли ИМВП у конкретного пациента осложненной или неосложненной. Тем не менее, был установлен ряд факторов, которые являются маркерами потенциальной осложненной ИМВП.
Осложненной инфекция мочевыводящих путей считается у пожилых людей, пациентов мужского пола и беременных. Помимо этого, в соответствии с клиническими рекомендациями EAU инфекция мочевыводящих путей считается осложненной при наличии следующих факторов:
– мужской пол;
– пожилой возраст;
– обструкция мочевыводящих путей (функциональная или органическая);
– камни в мочевыводящих путях;
– аномалии мочевыводящих путей;
– пузырномочеточниковый рефлюкс;
– госпитальная инфекция;
– недавно перенесенное вмешательство на мочевыводящих путях в анамнезе;
– катетер или дренаж в мочевыводящих путях;
– трансплантированная почка;
– азотемия;
– сахарный диабет;
– иммуносупрессивное состояние.
Продолжительность симптомов на момент консультации более 7 дней и неэффективность адекватной антибиотикотерапии более 72 ч также требуют отнесения заболевания к разряду осложненных.
Лечение
На сегодняшний день выделяют два вида антибактериальной терапии. Это этиотропная и эмпирическая. Этиотропная терапия характеризуется применением антибиотиков, направленных на избавление от установленных возбудителей заболеваний. Именно этот метод считается более совершенным и предпочтительным. Однако, как показывает практика, не всегда возможно уточнить бактериологический диагноз. Именно поэтому часто проводится эмпирическая терапия. Это значит, что врачом назначаются препараты, которые учитывают наиболее вероятные возбудители конкретной в данном случае инфекции и имеют наиболее вероятную чувствительность к возбудителю. При использовании антимикробной терапии необходимо основываться на определенных принципах. В первую очередь – это точный диагноз, постановка которого включает в себя установление локализации и степени тяжести инфекции. Также важно определить вид возбудителя. Необходимо проанализировать сведения о предполагаемом или уже установленном возбудителе, его чувствительности к используемым антимикробным препаратам. Важный момент – учитывать сведения о вторичной или приобретенной резистентности.
Согласно рекомендациям Европейской ассоциации урологов (EAU) препаратами выбора для лечения неосложненных инфекций нижних мочевыводящих путей являются:
- TMP-SMX (триметоприм-сульфаметоксазол);
- пивмицеллинам;
- нитрофурантоин;
- фосфомицин;
- фторхинолоны (относятся к группе альтернаивных).
Лечение острого неосложненного цистита преследует 3 основных направления:
- быстрое устранение клинических симптомов;
- эрадикация возбудителя;
- профилактика реинфекций.
Антибактериальный препарат, использующийся в лечении острого цистита, должен:
- как минимум соответствовать спектру антимикробной активности в отношении возбудителей острого цистита;
- характеризоваться фармакокинетикой, позволяющей обеспечить высокие концентрации в моче при приеме препарата 1–2 раза в день;
- иметь высокий профиль безопасности.
Адекватная антибиотикотерапия является краеугольным камнем успешного лечения острого неосложненного цистита. Необходимо помнить, что прием антибактериального препарата нецелесообразен в связи с недостаточной эффективностью при резистентности к нему в популяции более 15–20 % штаммов микроорганизмов.
Локальные данные по антибиотикорезистентности возбудителей внебольничных и нозокомиальных инфекций мочевыводящих путей – решающий фактор при выборе терапии. В России отмечается высокий уровень резистентности уропатогенов к ампициллину и ко-тримоксазолу, вариабельность резистентности к фторхинолонам (рис. 2).
Рисунок 2. Устойчивость E . coli к фторхинолонам, в% ( ARESC )
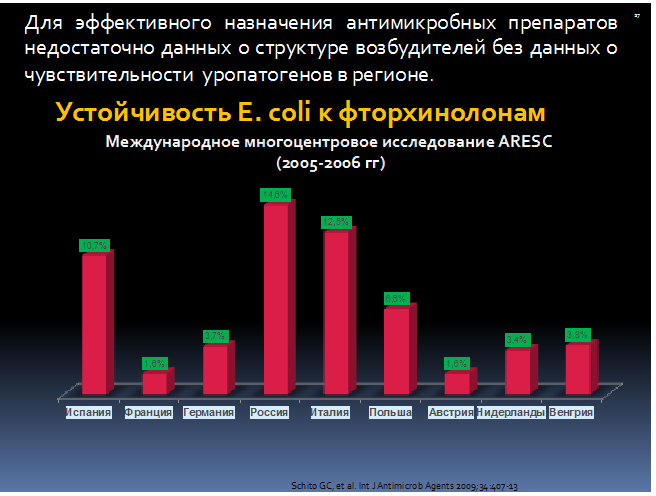
Как когда-то сказал Пауль Эрлих, «…лекарственная резистентность следует за лекарством, как преданная тень».
Нефторированные хинолоны: оксолиновая, налидиксовая, пипемидиновая кислоты в настоящее время потеряли свое лидирующее положение в связи с появлением фторхинолонов и не рекомендуются к применению. Они создают невысокие концентрации в тканях, не активны против грамположительных бактерий, к ним быстро развивается резистентность, особенно если используется неадекватная доза. Более того, они провоцируют развитие резистентности к фторированным хинолонам.
При выборе антибиотиков для лечения неосложненной инфекции нижних мочевыводящих путей необходимо учитывать целый ряд факторов. К ним относятся спектр и чувствительность уропатогенов, эффективность антибиотиков в клинических исследованиях, переносимость препаратов, побочные эффекты, стоимость и доступность препарата. Учитывая очень небольшое количество новых антибиотиков, находящихся на стадии разработки, разумное применение антибиотиков является единственным способом замедлить развитие резистентности (Inge Gyssens, 2009).
Фосфомицин является антибиотиком широкого спектра действия, активным в отношении большинства аэробных грам (-) и грам ( ) бактерий. В исследованиях in vitro показано, что при концентрации, достигаемой фосфомицином в моче, большинство возбудителей инфекций мочевыводящих путей, включая ванкомицин-резистентных энтерококков, чувствительны к фосфомицину (Nicolle L., 2003, Skerk V., Krehen I., Schutnwald S., 2001). В целом частота выделения штаммов уропатогенной E.coli, устойчивой к фосфомицину, составляет 0,7–1,0% с колебаниями между различными регионами от 0 до 1,5% (Рафальский В.В. и соавт., 2004). Фосфомицин является высокоэффективным средством элиминации возбудителей мочевой инфекции за счет следующих механизмов: бактерицидного – вследствие угнетения одного из этапов синтеза клеточной стенки; антиадгезивного, препятствующего взаимодействию уропатогенных штаммов и клеток уротелия (Daza R. И соавт, 2001). К достоинствам препарата также следует отнести отсутствие перекрестной аллергии с антибиотиками других групп. К недостаткам можно отнести высокий процент развития диареи после приема препарата. Препарат назначается в дозе 3 г, при необходимости повторный прием через 24 часа. Возможно его назначение детям и беременным женщинам.
Формирование резистентности штаммов микроорганизмов к наиболее часто применяемым антибиотикам заставляет изменить спектр лекарственных средств для терапии острого цистита. Более того, в том случае, когда у пациентки имеет место хотя бы набольшая опасность вовлечения верхних мочевыводящих путей или уже развившийся восходящий необструктивный пиелонефрит, спектр препаратов должен быть изменен. В данном случае возможно и оправдано использование цефалоспоринов. Цефиксим – цефалоспорин 3-го поколения, обладающий бактерицидным действием в отношении основных уропатогенов, который обладает способностью накапливаться в высоких концентрациях в плазме крови, корковом и мозговом веществе почек даже через 12 часов после приема (Рафальский В.В. и соавт., 2008). Форма солютаб (диспергируемые таблетки) определяет достижение высоких концентраций препарата за меньшее время в сравнении с обычными таблетками. Длительный период полувыведения цефиксима обеспечивает возможность применения 1 раз в сутки. Что немаловажно, препарат могут применять беременные. В экспериментальных исследованиях Halperin-Walega E. (1988), концентрации препарата в тканях плода <1% от концентрации в биологических средах матери, в плазме крови – в 70 раз ниже концентрации, чем в плазме матери. С учетом важности проблемы бессимптомной бактериурии у беременных использование данного препарата является перспективным.
Преимуществами препарата цефиксим являются:
· в условиях роста резистентности уропатогенов к фторхинолонам, цефалоспорины III поколения – препараты выбора;
· высокая активность против внебольничных штаммов E. Coli;
· высокие концентрации в моче и в почечной паренхиме;
· безопасность применения во время беременности;
· минимальная кратность, удобство и многообразие способов приема.
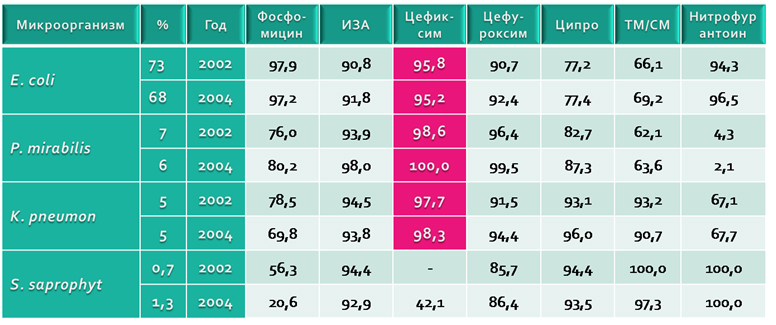
Цефиксим независимо от режима приема (400 мг однократно в день или по 200 мг два раза в сутки) показал высокую бактериологическую и клиническую эффективность в отношении основных уропатогенов (до 98%), превосходя в некоторых исследованиях фосфомицин в отношении чувствительности основных бактериальных возбудителей (рис. 3, табл. 1, 2).
Рисунок 3. Содержание цефиксима в плазме крови и почках при приеме в дозе 400 мг/сутки
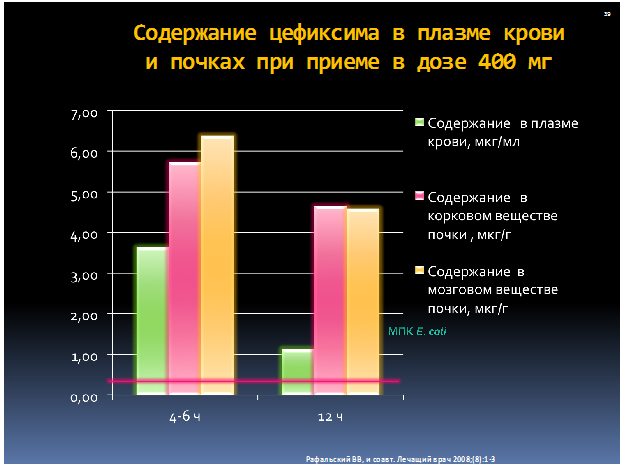
Таблица 1. Данные по эффективности цефиксима при неосложненной инфекции мочевыводящих путей
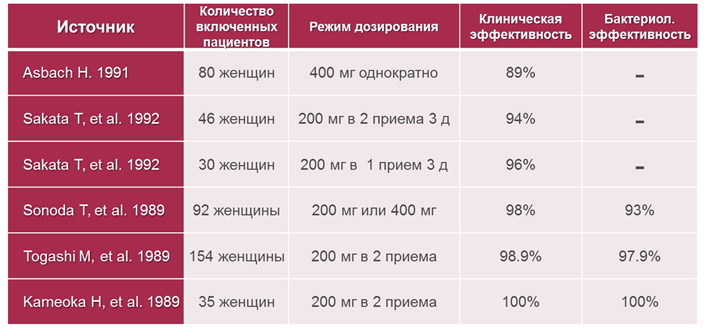
Таблица 2. Чувствительность основных антибиотиков при цистите ( Garcia Garcia MI , et al ., 2007)
В основе воспалительного инфильтрата в слизистой оболочке и подслизистом слое стенки мочевого пузыря лежит повреждение межуточной субстанции соединительной ткани вследствие разных причин как врожденного, так и приобретенного характера. Вне зависимости от этих причин исходом является нарушение физиологической регенерации эпителия мочевого пузыря с нарушением барьерной функции переходного эпителия. Разрушение защитного слоя уротелия происходит по разным причинам: лучевая терапия, частые урогенитальные инфекции, недостаточность женских половых гормонов и т.д. Лечение хронического цистита неэффективно без восстановления внутреннего слоя мочевого пузыря. При патологических процессах снижается концентрация гиалуроновой кислоты в тканях из-за нарушения баланса, замедляется процесс выздоровления. Гиалуроновая кислота – компонент гликозаминогликанового слоя, который находится в высоких концентрациях в субэпителиальном слое стенки мочевого пузыря и предназначен для защиты стенки мочевого пузыря от раздражающих компонентов мочи. Главная задача гликозаминогликанового слоя – защита собственной пластинки (lamina propria) и нервных окончаний от токсического действия мочи и всего, что в ней находится. Кроме того, гиалуроновая кислота связывает свободные радикалы и выступает в качестве иммуномодулятора. Для восстановления защитного внутреннего слоя мочевого пузыря разработаны и выпускаются препараты на основе гиалуроновой кислоты и хондроитинсульфата, главным компонентом которого является гиалуроновая кислота. Разумеется, при лечении рецидивирующих циститов до проведения инстилляций необходимо добиться эрадикации возбудителя. Применение гиалуроновой кислоты стало новым перспективным и патогенетически обоснованным направлением в лечении рецидивирующих циститов, так как в настоящее время это единственный метод, способствующий восстановлению защитного слоя уротелия у этой сложной категории больных.
Профилактика
Профилактика рецидивов хронического цистита является важным вопросом в определении тактики подхода к больным, страдающим данным заболеванием. Множество стратегий предложено для профилактики рецидивов инфекций мочевыводящих путей. Выявление факторов риска у больной позволяет удлинить период ремиссии заболевания.
Согласно рекомендациям Европейской ассоциации урологов, с целью профилактики инфекций мочевыводящих путей возможно применение следующих лекарственных средств:
§ длительная профилактика с использованием низких доз антибиотиков;
§ использование низких доз антибиотиков после полового акта.
Длительная или посткоитальная антибактериальная профилактика рецидивов ИМВП может использоваться только в случае безуспешности профилактических мер, например поведенческих, без использования антибиотиков (Grade of recommendation – A). Лишь немногие антибиотики подходят для антибактериальной профилактики из-за проблем с резистентностью бактерий, комплаенсом, побочными эффектами. Необходима разработка альтернативных стратегий.
Антибактериальная профилактика рецидивирующих ИМВП применяется только после проведения адекватной терапии и эрадикации возбудителя. До начала профилактической антибиотикотерапии необходимо подтвердить эрадикацию предыдущей ИМВП культуральным исследованием мочи через 1–2 нед после лечения.
§ местная заместительная гормонотерапия в климактерии ;
§ пробиотики (GR-1 и RC-14 лактобактерий) (Grade of recommendation – C);
§ неспецифическая профилактика (подкисление мочи, сок клюквы и др.) (Grade of recommendation – C);
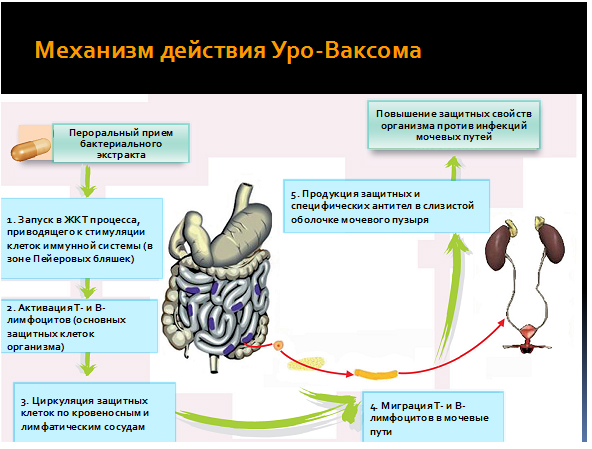
§ иммуноактивная профилактика. Единственным препаратом, рекомендованным для иммунопрофилактики рецидивов инфекции мочевых путей у женщин, является лиофилизированный бактериальный лизат (Grade of recommendation – B). Препарат – капсулы 6 мг, содержащие лиофилизированный бактериальный лизат Escherichia Coli, лизаты 18 штаммов E.coli, наиболее частого возбудителя инфекции мочевыводящих путей. Данный лекарственный препарат является пероральным иммуностимулирующим средством, который активирует механизм иммунной защиты организма через слизистую оболочку основных систем (MALT, GALT и UALT) и поддерживает активность этих механизмов на высоком уровне (рис. 4). Сюда входит гуморальный и клеточный иммунный ответ, в результате чего укрепляется естественная защита организма от инфекции нижних мочевыводящих путей, вызванных различными микроорганизмами. Более того, он может обеспечивать защиту от более широкого спектра патогенов-возбудителей инфекции мочевыводящих путей, а не только от используемых в его составе (Gilbart James, 2011). Препарат обеспечивает иммуноактивную профилактику за счет активизации собственных защитных сил организма, т.е. усиливает реакцию со стороны иммунной системы человека. Концентрация иммуноглобулинов A и G у пациентов, принимающих лиофилизированный бактериальный лизат, в несколько раз превосходит таковые у тех больных, которые не принимают данный препарат (Huberet al., 2000). Препарат хорошо переносится и практически не имеет побочных эффектов. Положительной особенностью препарата является возможность применения Уро-Ваксома как при лечении, так и при профилактике ИМВП. С целью лечения препарат используется совместно с антибиотиком по 1 капсуле в день в течение 10 дней, а для профилактики – по 1 капсуле в день в течение 3-х месяцев. Частота возникновения бактериурии через 3 месяца использования препарата у больных совместно с антибиотиком в 3 раза ниже, чем у тех пациентов, которые принимали только антибиотик (Czerwionka-Szaflarska и Pawlowska, 1996). Лиофилизированный бактериальный лизат сокращает число рецидивирующих инфекций нижних мочевыводящих путей, количество и выраженность симптомов, а также сокращает необходимость применения антибиотиков – по данным мета-анализа Курта Набера (2009) на 13%.
Рисунок 4. Механизм действия лиофилизированного бактериального лизата
Заключение
Подводя итог, необходимо еще раз подчеркнуть, что лечение ИМВП должно быть комплексным и включать помимо антибактериальных и противовоспалительных препаратов средства, влияющие на нормализацию функции НМВП (альфа1-адреноблокаторы, М-холиноблокаторы, антихолинестеразные препараты в зависимости от изменений уродинамики), а также препараты для местной и системной иммунопрофилактики, защиты уротелия от рецидива инфекции, а также местной заместительной гормонотерапии в климактерии.
Список литературы
1. Беднова В. Н., Бакалова Л. А. Лечение фторхинолонами (таривид, ципробай, абактал) инфекций урогенитального тракта. //Вестн. Дерматол. №3. – 1993.
2. Chew LD; Fihn SD Recurrent cystitis in nonpregnant women. West J Med, 1999 may, 170:5, 274-7.
3. Stamm W. E. et al. : Natural history of recurrent urinary tract infections in women. //Rev. Infect. Dis., 13: 77, 1991
4. Foxman B. Epidemiology of urinary tract infections: incidence, morbidity and economic costs // Am. J. Med. 2002. Vol. 113, supp. l S.:5-13.
5. Хайрлиев Г. 3. Изменения мочевого пузыря при дизурии у женщин. Автореф. канд. мед. наук. //М., 1990.
6. Лоран О. Б. Годунов Б. Н. Корсунская И. Л. Эндовезикальный ионофорез в лечении хронического цистита у женщин //Клиническая фармакология и терапия, т. 5. №2. 1996. С. 17-20.
7. Guidelines on urological infections, European Association of Urology, 2010.
8. Даниленко В.Р. Хронический цистит // Урол. и нефрол. 1995. – № 4. – С. 49-53.
9. Кан Д. В. Руководство по акушерской и гинекологической урологии. // М., 1978.-456 с.
10. Кан Д. В. Руководство по акушерской и гинекологической урологии. // М., 1982.-С. 234-235.
11. Кузнецова H.H., Хоменко Н.П., Красильников Г.П., Хорошавина H.A. Системный подход к диагностике и лечению хронических циститов // Сб. науч. тр.: «Актуальные вопросы урологии и андрологии», посв. 100-летию каф. СПбМАПО. СПб, 2001. – С. 188-190.
12. Ильинская Е.В. Патоморфологический анализ и патогенетические особенности лейкоплакии мочевого пузыря у женщин: Диссертация … кандидата медицинских наук: 2007.- 110 с.
13. Hooton T., Stamm W. Diagnosis and treatment of uncomplicated urinary tract infection. – Infect. Dis. Clin. N. Am. – 1997 – 11:551-581.
14. Лоран О.Б., Пушкарь Д.Ю., Тевлин К.П. Применение дриптана (оксибутинина) у больных с императивными формами расстройств мочеиспускания. // Урол. и нефрол. 1998. – № 6. – С. 24-26.
15. Naber K.G., Schito G., Botto H., Palou J. Surveillance study in Europe and Brazil on clinical aspects and antimicrobial resistance epidemiology in females with cystitis (ARESC): implications for empiric therapy // Eur. Urol. 2008. Vol. 54. P. 1164-1178.
16. Perrotta Carla, Aznar Mireya, Mejia Raul et all. Oestrogens for preventing recurrent urinary tract infection in postmenopausal women. Cochrane Database of Systematic Reviews: Reviews 2008, Issue 2.
17. Неймарк А.И., Неймарк Б.А., Кондратьева Ю.С. — Дизурический синдром у женщин. Диагностика и лечение: руководство / М.: ГЭОТАР-Медиа, 2010. — 256 с.
18. Кан Д.В., Лоран О.Б., Левин Е.И. Морфологические изменения мочевого пузыря // Урол. и нефрол. 1988. – N 6. – С. 16-20.
19. Лоран О.Б., Вишневский Е.А., Вишневский А.Е. Лечение расстройств мочеиспускания у больных доброкачественной гиперплазией простаты α-адреноблокаторами. М., 1998. – 123с.
20. Berg E, et al. High prevalence of sexually transmitted diseases in women with urinary infections. //Acad Emerg Med. 1996 Nov. 3(11):1030-4.
21. Комяков Б.К., Новиков А.И., Горелов А.И., Гулиев Б.Г., Кириченко O.A., Прохожев А.Ю., Оде М. Ортотопическая пластика мочевого пузыря сегментом желудка Урология, 2004.-№3.-С.32-35.
22. Gosling J.A., Gilpin S.A., Dixon J.S., Gilpin C.J. Decrease in the autonomic innervation of human detrusor muscle in outflow obstruction // J. Urol.-1986.-Vol.136.-P. 501-503.
23. Thuroff J., Burke B., Ebner A. et al. Randomized double-blined multicentre trial on treatment of freaquency, urgency and incontinence related to detrusor hyperactivity: Oxybutinin vs propanteline vs placebo. //J. Urol. 1991. – Vol. 145.-P. 813.
24. Гаджиева З.К. Уродинамические исследования в диагностике и лечении нарушений мочеиспускания. – М., 2009 – с.114-128.
25. Зубань О.Н. Причины, диагностика и лечение дисфункций мочевого пузыря у больных нефролотуберкулезом: Автореф. дисс. … канд. мед. наук. СПбНИИФ. СПб, 2002. – 24 с.
26. Xайрлиев Г.З. Изменения мочевого пузыря при дизурии у женщин // Автореф. дисс. канд. мед. наук. М., 1990. – 21 с.
27. Gogus C., Turkolmez K., Tulunay O., Gogus O. Eosinophilic cystitis in a case presenting with an initial diagnosis of invasive bladder tumor. // J. Urol. Int. -2000. Vol. 64, № 3. – P. 162-164.
28. Tawada T., Sakakura T., Watanabe H. Clinical evaluation of pressure-flow test to male patient with micturition disturbance // Japanese Journal of J. Urol.-1993,-Vol.84.-P.879-883.
29. Возианов А.Ф., Сеймиевский Д.А., Бекмуратов У. Болезни мочевого пузыря у детей // Киев, Здоров’я, 1992. – 216 с.
30. Забиров К.И. Восходящая инфекция мочевых путей и почек у женщин. // Автореф. дисс. д-ра мед. наук. М., 1997.-24 с.
31. Кан Д. В. Руководство по акушерской и гинекологической урологии. – М., 1986. – 488 с.
32. Левин Е.И. Цистит у женщин: диагностика и лечение: Автореф. дисс. … канд. мед. наук. М., 1991. – 21 с.
33. Лоран О.Б., Каприн А.Д., Давидьянц A.A. Показания к кишечной пластике мочевого пузыря.// В кн.: IX Всероссийский съезд урологов (тезисы докладов). Курск, 1997. – С. 374–375.
34. Gillespie L. Destruction of the vesicoureteric plexus for the treatment of the hypersensitive bladder disorders. // Br J. Urol, 1994. Vol 74. P. 40-43.
35. Державин В.М., Вишневский Е. Л., Гусев Б.С. Экспериментальное изучение незаторможенного нейрогенного мочевого пузыря // Урол. и нефрол. 1977. – № 4. – С. 32-36.
36. Andersson K.E. Current concepts in the treatment of disorders of micturition. // Drugs. 1988. – Vol. 35. – P. 477-494.
37. Andersson K.E. Pharmacology of lower urinary tract smooth muscles and penile erectile tissues. // Pharmacol. Rew. 1993. – Vol. 45. – P. 253, Biggers R.D. Self-administration of dimethyl sulfoxide (DMSO) for interstitial cystitis. //J.Urol., 1986.- Vol.28.- P. 10-11.
38. Cetinel B., Turan T., Talat Z. et al. Update evaluation of benign prostatic hyperplasia: when should we offer prostatectomy? // Br. J. Urol.-1994.-Vol. 74.-566-571.
39. Hinman F.J. Selections of intestinal segments for bladder substitution: Physical and physiological characteristics // J. Urol. 1988. – Vol. 139. – P. 519.
40. Kinder R.B., Mundy A.R. Pathophysiology of idiopathic detrusor instability and detrusor hyperreflexia. An in vitro study of human detrusor muscle. // Br.J.Urol.-1987.-Vol.60.-P. 509-513.
41. Pang X., Marchand J., Sant G.R., Kream R.M., Theoharides T.C. Increased number of substance P positive nerve fibres in interstitial cystitis // Br. J. Urol.- 1995. Vol. 75, № 6. – P. 744-750.
42. Perez-Marrero R., Emerson L., Juma S. Urodynamic studies in interstitial cystitis. //J. Urol. 1987.-suppl.29.- P.27 30.
43. Неймарк А.Г. Роль микроциркуляторных и уродинамических нарушений в генезе стойкой дизурии у женщин. – 2002 – диссер. канд. мед. наук.
44. Nicolle L. Empirical treatment of acute cystitis in women.// Int J Antimicrob Agents. 2003. Jul; 22 (1):1-6.
45. Skerk V., Krehen I., Schutnwald S. Antimicrobal therapy of urinary tract infections.// Lijec Vjesn 2001, Jan-Feb; 123 (1-2): 16-25.
46. Рафальский В.В., Страчунский Л.С., Кречикова О.И., Эйдельштейн И.А. и соавт. Оптимизация антимикробной терапии амбулаторных инфекций мочевыводящих путей по данным многоцентровых микробиологических исследований UTIAP-1, UTIAP-11// Урология. 2004. № 4. С.13-17.
47. Uncomplicated UTIS in adults. //E.A.U.Guidlines on urinary tract and male genital tract infections. P. 9-14.
48. Daza R., Gutierrez J., Piedrola G. Antibiotic susceptibility of bacterial strains isolated from patients with community-acquired urinary tract infections // Int J Antimicrob Agents. 2001. Vol. 18. № 3. P. 211-5.
49. Лоран О.Б., С.Б. Петров, Т.С. Перепанова, Л.А. Синякова, А.З. Винаров, И.В. Косова. Эффективность применения фосфомицина трометамола (Монурала 3 г) в лечении больных хроническим рецидивирующим циститом. – Эффективная фармакотерапия в урологии. – №4 декабрь 2008.
50. Constantinides C., Manousakas T., Nikoiopoulos P., Stanitsas A. Prevention of recurrent bacterial cystitis by intravesical administration of hyaluronic acid: a pilot study // Brit.J.Urol. Intern. 2004. Vol. 93. P.1262-1266.
51. Huberet al., 2000, Int. J. Immunopharmacol. 22; 1103-11
52. Sweet, R. L: Bacteriuria and pyelonephritis during pregnancy. Semin. Perinatol. 1 (1977) 25-40
53. Halperin-Walega E. (Drug Metab Dispos 1988;16(1):130-4)
54. Gilbart James. European Urological Review, 2011; 6(2):114-9
55. Garcia Garcia MI, et al. J Chemother 2007;19(3):263-70
56. Lipovac M, Kurz C, Reithmayr F, Verhoeven HC, Huber JC, Imhof M. Prevention of recurrent bacterial urinary tract infections by intravesical instillation of hyaluronic acid. Int J Gynaecol Obstet 2007; 96:192–5.
57. Хазан П.Л. Современный подход к медикаментозной терапии хронического цистита. Диссертации на соискание ученой степени кандидата медицинских наук. М., 2010 – 216 с.
58. Локшин К. Диагностика и лечение инфекций мочевыводящих путей. Лекция // «Врач», № 6, 2006, с. 18-23.
59. Кудрявцев Ю.В., Кирпатовский В.И., Перепанова Т.С., Хазан П.Л. Применение стабилизатора гликозаминогликанов – гиалуроната цинка, при экспериментальном моделировании острого бактериального и интерстициального цистита. – Экспериментальная и клиническая урология. №1 – 2011, стр. 39-44.







