Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "ОСТЕОАРТРОЗ И МЕТАБОЛИЧЕСКИЙ СИНДРОМ"
Автор: Поворознюк В.В., Григорьева Н.В., Мартынюк Л.П.
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Кардиология, Неврология, Ревматология, Семейная медицина/Терапия
Просмотров: 2 783
Дата проведения: с 01.06.2015 по 01.06.2016
По мере развития цивилизации, преодолевшей на протяжении многовековой истории эпидемии жизненно опасных инфекций, на первое место по актуальности среди всех причин заболеваемости и смертности вышла проблема сердечно-сосудистых заболеваний [Коваленко В.Н., 2004; Митченко Е.И., Корпачев В.В., Путай М.И., 2008; Teichman S.L., Maisel A.S., Storrow A.B., 2015; Cunnington C., Kwok C.S., Satchithananda D.K., 2015]. Этому способствовало изменение образа жизни за счет ограничения физической активности, увеличения калорийности пищевых продуктов, с преобладанием в рационе рафинированных углеводов и животных жиров, роста эмоционально-стрессовых нагрузок. В совокупности поведенческие факторы и генетические изменения способствовали развитию каскада метаболических нарушений. В связи с этим комбинация висцерального ожирения, нарушения липидного и углеводного обменов, артериальная гипертензия (АГ) были выделены в самостоятельный симтомокомплекс, который получил название «метаболический синдром» (МС) [Guh D.P., Zhang W., Bansback N., 2009; Маколкин В.И., 2010; Finucane M.M., Stevens G.A., Cowan M. J., et al., 2011].
Метаболический синдром – комплексное состояние организма, которое, как правило, начинает развиваться после 30 лет, его распространенность увеличивается с возрастом, особенно в средней возрастной группе и достигает максимума у пожилых людей. Согласно данных исследования NHANES III (National Health and Nutritional Examination Survey), в котором принимало участие 8814 мужчин и женщин в возрасте от 20 лет и старше, распространенность МС увеличивалась с 6,7 % в возрасте 20–29 лет до 43,5 % в возрасте 60–69 лет [Ford E.S., Giles W.H., Dietz W.H., 2002]. Соотношение больных в зависимости от пола также изменяется в различные возрастные периоды. Так возрастной группе от 20 до 49 лет МС чаще наблюдается у мужчин, в возрасте 50–69 лет встречается практически одинаково у мужчин и женщин, а в возрасте старше 70 лет – чаще диагностируется у женщин. Последнее, по мнению многих авторов [Насонов Е.Л., 1997; Григорян О.Р., Андреева Е.Н., 2007; Чекальськая Н.А., Корпачев В.В., 2007; Тронько М.Д., Корпачева-Зинич О.В., 2008], обусловлено наступлением менопаузы.
Распространенность МС в два раза превышает распространенность сахарного диабета (СД), и в ближайшие 25 лет ожидается увеличение темпов его роста на 50 %.
На сочетание АГ с дислипидемиями, ожирением, нарушением углеводного обмена клиницисты обратили внимание почти 100 лет назад и данный комплекс метаболических, гормональных и клинических расстройств описывался в литературе неоднократно.
В 1922 году Г.Ф. Ланг обнаружил наличие тесной связи между ожирением, АГ и нарушением углеводного обмена. В 1923 году Kylin, а в 1926 году А.Л. Мясников и Д.М. Гротель указали на частую комбинацию гиперхолестеринемии, гиперурикемии с ожирением и АГ. В 1936 году Himsworth Н. определил, что снижение чувствительности тканей к инсулину является одной из основных составляющих СД. В 1948 году Е.М. Тареев в монографии «Гипертоническая болезнь» акцентировал внимание на том, что представление о гипертонике часто ассоциируется с ожирением и нарушением белкового обмена, накоплением в крови продуктов неполного обмена веществ – холестерина, мочевой кислоты и др. Vague J. (1940) обосновал взаимосвязь абдоминального ожирения и нарушения липидного обмена с сахарным диабетом и сосудистыми расстройствами. В 1966 году Camus J. предложил выделить «метаболический трисиндром», в состав которого входили бы гиперлипидемия, СД и подагра. Mehnert H. и Kuhlmann H. (1968, 1977) описали взаимосвязь факторов, которые приводят к обменным нарушениям при СД и АГ, и ввели понятие «синдрома достатка». Henefeldt M. и Leonard W. (1980, 1981) обозначили случаи сочетания различных метаболических нарушений у человека термином «метаболический синдром».
Концепцию МС впервые на основании собственных наблюдений и обобщений исследований других авторов предложил Gerald M., а Reaven G.M. в 1988 году доказал, что согласно последней сочетание нарушения толерантности к глюкозе с гиперинсулинемией, повышением уровня триглицеридов (ТГ), снижением уровня холестерина (ХС), липопротеидов высокой плотности (ЛПВП) и АГ не является случайным, а развивается в результате единого патогенетического механизма – инсулинорезистентности. Для определения данного симтомокомплекса Reaven G.M. предложил термин «синдром Х». Хотя ожирение не было включено в этот симптомокомплекс, но было отмечено тесную взаимосвязь между увеличением массы тела и инсулинорезистентностью.
Позже Kaplan N.M. (1989) охарактеризовал комбинацию абдоминального ожирения, нарушенной толерантности к глюкозе, артериальной гипертензии и гипертриглицеридемии как «смертельный квартет». DeFronzo R.A., Ferrani I E. (1991), S. Haffner (1992) предложили использовать термин «синдром инсулинорезистентности».
Кроме классического представления о МС Spencer C.и др. (1997) выдвинули концепцию менопаузального метаболического синдрома, в основе которого лежит дефицит эстрогенов. Такое заключение было сделано после анализа работ, посвященных влиянию менопаузы на чувствительность к инсулину, показатели липидного и углеводного обмена, распределение жировой ткани и систему гомеостаза, а также влиянию заместительной гормональной терапии на перечисленные параметры у женщин.
В 1998 году рабочая группа ВОЗ очертила основные симптомы, которые формируют метаболический синдром.
Как видно из вышеописанного, данный симптомокомплекс имеет много различных названий, но термин «метаболический синдром» стал наиболее часто использованным в медицинской литературе. Согласно мнению многих ученых, объединяющей основой всех проявлений МС является первичная инсулинорезистентность [Standl E., 2005] и сопутствующая системная гиперинсулинемия. Это связано с тем, что абдоминальный тип ожирения и увеличение массы жировой ткани с одной стороны приводят к увеличению потребности организма в инсулине и способствуют развитию гиперинсулинемии. С другой стороны в адипоцитах распадаются триглицериды с образованием свободных жирных кислот, количество которых в последующем увеличивается в плазме, что приводит к снижению чувствительности периферических тканей к инсулину, развитию инсулинорезистентности и компенсаторному увеличению гиперинсулинемии.
Даже при нормальных показателях гликемии и отсутствии нарушения толерантности к углеводам инсулинорезистентность и гиперинсулинемия приводят к ряду патологических клинико-лабораторных нарушений.
Повреждающий характер гиперинсулинемии проявляется в увеличении концентрации натрия в крови, усилении активности симпатической нервной системы, что способствует повышению артериального давления, развитию артериальной гипертензии, возникновению метаболических, гемодинамических и органных нарушений, которые в конечном результате приводят к развитию СД 2 типа, ишемической болезни сердца (ИБС), других проявлений атеросклероза.
Избыток свободных жирных кислот в крови кроме блокирования оксигенации и транспорта глюкозы, ухудшения действия инсулина на клетки печени и мышц (то есть развитие инсулинорезистентности), усиливает продукцию в печени липопротеидов очень низкой плотности с последующим повышением концентрации в плазме крови ТГ, аполипопротеина В и снижением уровня антиатерогенных ЛПВП.
Взаимосвязь между нарушениями липидного и углеводного обменов изучена в исследованиях В.Б. Мичка (2008). Доказано, что показатели уровня гликемии натощак и постпрандиальной гликемии тесно достоверно связаны с гиперхолестеринемией и гипертриглицеридемией, а гиперинсулинемия (натощак и постпрандиальная) с высокой степенью достоверности корелирует с гипертриглицеридемией и снижением уровня ХС ЛПВП.
Хотя, МС не имеет собственного кода в МКБ–10 (ВОЗ, 1998) это совсем не свидетельствует о его небольшой значимости.
Так, согласно исследования PAMELA [Mancia G., Bombelli M., Corrao G. et al., 2007] риск смерти, в том числе и от сердечно-сосудистой патологии, независимо от пола в два и три раза выше соответственно у больных с МС и без него. Об исключительной значимости проблемы МС свидетельствуют также данные BOTNIA STUDY. Результаты исследования показали, что смертность от сердечно-сосудистых заболеваний у бальных с МС достигает 12,2 % по сравнению с 2,2 % у пациентов без него [Isomaa D., Almagren P., Tuomi T. еt al., 2001]. В эпидемиологических исследованиях показано, что у больных с повышенной массой тела и МС чаще развиваются заболевания опорно-двигательного аппарата – остеохондроз позвоночника и обменно-дистрофический полиартрит, болезни гепатобиллиарной системы – дискинезии желчного пузыря, хронический холецистит, желчекаменная болезнь, опухоли различных локализаций [Тронько М.Д., Корпачева-Зинич О.В., 2008].
Выделение МС в отдельную патологию имеет большое клиническое значение, потому что соответственная терапия разрешает добиться уменьшения и даже ликвидации основных его проявлений и тем самым предотвратить развитие СД 2 типа и атеросклероза – основных причин заболеваемости и смертности населения.
С целью стандартизации компонентов МС на протяжении последних15 лет было предложено несколько вариантов идентификации МС [Митченко Е.И., Корпачев В.В., Путай М.И. и др., 2008].
Согласно рекомендаций ВОЗ [Albert K.G., Zimmert P.Z., 1998] критериями МС следует считать инсулинорезистентность (которую идентифицируют по наличию СД 2 типа, гипергликемии натощак, нарушению толерантности к глюкозе) в сочетании с двумя из нижеуказанных факторов:
1) наличие АГ (систолическое артериальное давление ≥ 140 мм рт. ст. или диастолическое АД ≥ 90 мм рт. ст.) и/или проведение антигипертензивной терапии;
2) уровень триглицеридов в плазме крови ≥ 1,7 ммоль/л и/или ЛПВП < 0,9 ммоль/л у мужчин и < 1,0 ммоль/л у женщин;
3) индекс массы тела (ИМТ) >30 кг/м2 и/или соотношение окружности талии (ОТ) / окружности бедер (ОБ) > 0,90 у мужчин и > 0,85 у женщин;
4) экскреция альбумина с мочой ≥ 20 мкг/мин и/или соотношение альбумин / креатинин ≥ 30 мг/г.
В рекомендациях ATP III (Аdult Treatment Panel III – Третий отчет группы экспертов по выявлению, оценке и лечению гиперхолестеринемии у взрослых в рамках Национальной образовательной программы США по холестерину) данные критерии были незначительно изменены. Не исключено, что это было связано с публикацией результатов нескольких масштабных проспективных исследований относительно оптимального контроля АД у больных СД. Кроме того, были упрощены антропометрические измерения: считают, что диагностическая ценность определения ОТ и расчета индекса ОТ/ОС аналогичны. Есть также некоторые отличия в уровнях показателей липидного обмена. К критериям МС, предложенным АТР ІІІ, относят:
1) абдоминальное ожирение, выраженное как ОТ >102 см у мужчин и > 88 см у женщин;
2) уровень триглицеридов ≥ 1,7 ммоль/л;
3) уровень ЛПВП < 1,03 ммоль/л у мужчин и < 1,29 ммоль/л у женщин;
4) уровень АД ≥ 130/85 мм рт. ст.;
5) уровень глюкозы в плазме крови натощак ≥ 6,1 ммоль/л.
Новое определение МС было предоставлено в апреле 2005 года на І Международном конгрессе по предиабету и метаболическому синдрому в Берлине, который проводился Международной диабетической федерацией (IDF), и на 75–м конгрессе Европейского общества по атеросклерозу в Праге.
Целью создания консенсуса по МС было определение единого диагностического алгоритма, который бы способствовал выделению популяции пациентов с высоким кардиоваскулярным риском. Проведение профилактических мероприятий, включающих модификацию образа жизни и использование соответственных лекарственных препаратов, у этих пациентов могло бы значительно повлиять на заболеваемость, инвалидность, смертность (поскольку такие макрососудистые осложнения как ИБС, инфаркт миокарда, церебральный инсульт являются главными причинами смерти больных МС и СД).
Принципиально новым стало утверждение абдоминального ожирения, как основного диагностического критерия метаболического синдрома. Также были изменены нормативные параметры ОТ, уровня гликемии натощак.
Несмотря на то, что основной причиной развития МС является инсулинорезистентность, она не входит в рекомендованные для широкого использования критерии его диагностики. Это обусловлено дороговизной и сложностью ее определения, что является существенным ограничением для ее рутинного использования.
Критериями МС, рекомендованными Международной диабетической федерацией (IDF) [Alberti K.G. et al., 2005] является:
1. Наличие абдоминального ожирения, которое определяется как окружность талии в сантиметрах с учетом особенностей различных этнических групп:
– у европейцев – ≥ 94 см у мужчин и ≥ 80 см у женщин;
– в США – ≥ 102 см у мужчин и ≥ 88 см у женщин;
– в Южной Азии – ≥90 см у мужчин и ≥ 80 см у женщин;
– у жителей Китая, Малайзии, азиатско-индийской популяции:
– китайцев – ≥ 90 см у мужчин и ≥ 80 см у женщин;
– японцев – ≥ 85 см у мужчин и ≥ 90 см у женщин;
– у этнических центрально- южноамериканцев предлагается использование рекомендаций для жителей Южной Азии до получения более специфических данных;
– у африканцев, проживающих к югу от Сахары, предлагается использование рекомендаций для европейцев до получения более специфических данных;
– в восточно-средиземноморской и средневосточной (арабы) популяции, предлагается использование рекомендаций для европейцев до получения более специфических данных.
2. Наличие двух факторов из 4-х нижеперечисленных:
1) уровень триглицеридов ≥ 1,7 ммоль/л (150 мг/дл) или проведение специфической гиполипидемической терапии;
3) уровень ЛПВП < 1,03 ммоль/л (40 мг/дл) у мужчин, < 1,29 ммоль/л (50 мг/дл) у женщин или проведение специфической для дислипидемий терапии;
4) уровень АД ≥ 130/85 мм рт. ст. или гипотензивная терапия по поводу ранее диагностированной артериальной гипертензии;
5) уровень глюкозы в плазме крови натощак > 5,6 ммоль/л (100 мг/дл) или ранее диагностированный СД.
Поскольку в результате развития МС возникает риск появления ряда заболеваний, таких как СД, гипертоническая болезнь, ИБС и др. [Хаустова О.О., 2009] проблема диагностики и адекватного лечения МС является актуальной для мировой медицины.
Полный МС формируется на протяжении не менее десятилетия [Жердёва Н.Н., Маньковский Б.Н., 2009]. Так, в возрасте 30-39 лет большинство пациентов имеют абдоминальное ожирение и артериальную гипертензию, к которым присоединяются нарушения липидного и углеводного обмена. Как правило, к моменту первого обращения за медицинской помощью большинство пациентов имеют весь спектр проявлений МС и высокий риск развития сердечно-сосудистых проявлений. Поэтому с целью увеличения длительности и качества жизни, больные нуждаются в лечении, которое должно быть комплексным и, следовательно, наряду с активным изменением образа жизни, включать адекватную медикаментозную терапию [Хаустова О.О., 2009].
На сегодняшний день получены многочисленные данные о взаимосвязи остеоартроза (ОА) с метаболическими нарушениями [Збровский А.Б., Стажаров М.Ю., Мартемьянов В.Ф., 2000; Васильева Л.В., Лахин Д.И., 2010; Masuko K., Murata M., Suematsu N. et al., 2009].
В настоящее время установлено, что метаболические нарушения оказывают значимое влияние на иммунокомпетентные клетки [Алмазов В.А., Шляхто Е.В., Красильникова Е.И., Благосклонная Я.В., 2001], в частности нейтрофилы и моноциты. Инсулинорезистентность, ключевое звено МС, способствуя увеличению продукции гликированных соединений, вызывает повышенное образование кислородных радикалов, провоцирующих эндотелиальную дисфункцию [Ивлева А.Я., 2005]. Повышение образования нейтрофилами кислородных радикалов также выявлено у больных ОА, осложненным синовитом коленного сустава [Kurygin A.G., 2001]. Известно, что повреждения, вызванные свободными радикалами, вносят существенный вклад в развитие как атеросклероза, так и заболеваний суставов. Обнаружена тесная корреляция между содержанием триглицеридов (ТГ) и способностью фагоцитов синтезировать ФНО-α [Доценко Э.А., Юпатов Г.И., Чиркин А.А., 2001], местная продукция которого в очаге воспаления обеспечивает хемотаксис нейтрофилов, усиление фагоцитоза, их дегрануляцию, продукцию и секрецию ими активных форм кислорода. Важную роль инсулинорезистентности в развитии ОА доказывает высокий уровень ТГ у больных с полной утратой хряща по данным артроскопии и его корреляция с циркулирующими иммунными комплексами. Таким образом, наличие признаков МС у больных остеоартрозом ассоциируется с более тяжелым поражением хряща и рецидивирующими синовитами [Bailey C.J., Turner R.C., 1996].
В развитии ОА принимают участие многие факторы, при этом одни играют ведущую роль (физические нагрузки, микротравматизация, гипоксия и ишемия), а другие — предрасполагающую (гормональные, метаболические, инфекционно-аллергические факторы, возраст, гиподинамия).
Ожирение – важнейший фактор риска ОА, в большей степени коленных суставов [Поворознюк В.В., Григорьева Н.В., 2004; Коваленко В.Н., Борткевич О.П., 2004; Васильева Л.В., Лахин Д.И., 2012; Masuko K., Murata M., Suematsu N. et al., 2009; Shin D., 2014]. Клинфордское исследование (Chingford Study) [Hart D.J., Doyle D.V., Spector T.D., 1999] продемонстрировало, у женщин с ожирением (ИМТ > 26,4 усл. ед.) достоверно увеличивается риск развития остеофитов при ОА коленных суставов (отношение шансов (ОШ) составило 2,38, 95 % доверительный интервал (95 % ДИ): 1,29-4,39). Во Фременгеймском исследовании (The Framingham Study) [Felson D.T., Anderson J.J., Naimark A. еt al., 1998] показано, что связь между массой тела и ОА коленного сустава была сильнее выражена у женщин, чем у мужчин. Так, у женщин с избыточной массой тела (самая высокая квантиль) относительный риск ОА составил 2,07 (95 % ДИ: 1,67-2,55), а в следующей квантиле – 1,44 (95 % ДИ: 1,11-1,86). Связь между ожирением и ОА сохранялась после учета показателей уровня мочевой кислоты в сыворотке крови и уровня физической активности, и была наиболее сильной у пациентов с выраженным ОА. По данным этого исследования, ожирение было связано с риском как симптоматического, так и бессимптомного ОА коленных суставов. Также показано, что женщины, снизившие свой вес в среднем на 11 фунтов (1 фунт — 453,59 г), уменьшили риск развития ОА коленных суставов на 50 %.
По данным многих авторов, взаимосвязь между увеличенной массой тела и ОА тазобедренных суставов менее выражена, чем с ОА коленных суставов. При этом одностороннее поражение тазобедренного сустава не связано с избыточным весом в отличие от двухсторонней локализации патологического процесса.
Перегрузка коленных и тазобедренных суставов при ожирении ведет к повреждению хрящевой ткани и нарушениям в связочном аппарате, а также в других поддерживающих структурах [Шостак Н.А., 2003; Поворознюк В.В., Григорьева Н.В., 2004]. При увеличении в массе на 1 фунт общая сила, действующая на коленный сустав в положении стоя на одной нижней конечности, увеличивается на 2-3 фунта. Масса тела, увеличенная в 3-6 раз, передается через коленный сустав во время ходьбы. Для оценки дополнительной силы, переданной на коленный сустав при ходьбе у пациента с избыточной массой, любое увеличение массы тела должно быть умножено на этот коэффициент. Это влияние избыточной нагрузки объясняет в большинстве случаев повышенный риск развития ОА коленных и тазобедренных суставов среди лиц с избыточным весом. В некоторых, однако, не в большинстве исследований сообщено о взаимосвязи между избыточным весом и ОА кистей, при этом высказывается предположение о том, что метаболические нарушения могут выступать в роли посредника (например, диабет или нарушение липидного обмена), однако, в настоящее время поиск такого посредника продолжается.
В настоящее время взаимосвязь между ОА и ожирением не вызывает сомнения. Однако, по некоторым данным, артериальная гипертензия, дислипидемия и повышение уровня глюкозы крови сопутствуют ОА независимо от ожирения [Зотов A.A., Вызова Т.Н., Мороз Н.Г., Теверовская В.В., 1985; Ионов А.Ю., Фишер А.Н., Шубич М.Г., 1990; Koiwa M., Shiga H., Nakamura H., Yoshno S., 1992]. В то же время среди причин вторичного ОА выделяют и эндокринные заболевания, в частности сахарный диабет [Олюнин Ю.А. , 1997; Поворознюк В.В., Григорьева Н.В., 2004; Коваленко В.Н., Борткевич О.П., 2004].
В исследовании Reid J.L. и соавт. (2010) изучено влияние ожирения и других факторов кардиоваскулярного риска на риск развития ОА у 6299 жителей южной Калифорнии старше 35 жителей на протяжении 2002-2006 гг. Остеоартроз был установлен у 16,5 % женщин и 11,5 % мужчин, при этом частота патологии увеличивалась с возрастом, больше у женщин. Наличие болевого синдрома при ОА было связано со степенью ожирения, АГ – с курением больных. В данном исследовании у мужчин не было выявлено связи сахарного диабета с ОА, у женщин сочетание диабета и ОА диагностировали в возрасте от 35 до 54 лет [Reid J.L., Morton D.J., Wingard D.L. et al., 2010].
На сегодняшний день существует много доказательств, что ОА не просто заболевание, связанное с нарушениями морфо-функционального состояния суставов, а нарушение обмена веществ, при котором развиваются метаболические расстройства, способствуют возникновению и прогрессированию системного патологического процесса. Таким образом, развитие ОА связано не только с ожирением и артериальной гипертензией, но и с другими факторами кардиоваскулярного риска – сахарным диабетом, инсулинорезистентностью и дислипидемией.
По данным некоторых исследований у больных ОА существует повышенный риск сердечно-сосудистой патологии, который может увеличиваться при лечении нестероидными противовоспалительными препаратами (НПВП) и при наличии других факторов риска (возраст, ожирение, АГ). По данным И.А. Романовой (2009), у 62 % больных ОА были выявлены АГ и повышение в крови уровня С-реактивного белка, степень которого зависел от факторов риска кардиоваскулярных нарушений, болевого синдрома и стадии заболевания. Также у больных, страдающих на ОА были обнаружены повреждение эндотелия и нарушение его функций – снижение антитромбогенной активности сосудистой стенки, повышение упругости артерий, выраженность которых возрастала с увеличением длительности заболевания.
В исследовании NHANES III (National Health and Nutrition Examination Survey III) при обследовании 7714 пациентов (у 975 из которых установлен ОА) было установлено, что ОА связан с увеличением частоты МС преимущественно в молодом возрасте [Puenpatom R.A., Victor T.W., 2009]. МС был выявлен у 59 % больных с ОА и 23 % пациентов без ОА и включал: артериальную гипертензию (75 и 38 % соответственно), абдоминальное ожирение (63 и 38 % соответственно), гипергликемию (30 и 13 % соответственно), повышенный уровень триглицеридов (47 и 32 % соответственно) и низкий уровень ЛПНП (44 и 38 % соответственно). МС чаще всего диагностировали у пациентов с ОА независимо от пола и расовой принадлежности, при этом более сильная связь между ОА и МС была отмечена у молодых пациентов, и уменьшалась с возрастом.
В исследованини А.Е. Кратнова с соавт. была выявлена взаимосвязь между дислипидемией, окислительным стрессом и эрозивными изменениями в хряще, также установлена связь между МС и более тяжелым поражением суставного хряща по данным артроскопии у пациентов ОА, осложненным вторичным синовитом [Кратнов А.Е., 2006].
В исследовании Leite A.A., Costa A.J. Lima Bde A. (2011) при изучении влияния коморбидности на риск и течение ОА при обследовании 91 пациента (средний возраст 59,3 года, 91,4 % женщины), установлено, что МС выявлялся у 54,9 % больных (82 % у пациентов с OA коленных суставов и 18 % у больных OA суставов ), АГ – у 75,8 %, диспипидемия – у 52,6 %, ожирение – у 57,1 % пациентов.
Вторичный синовиит является частым осложнением ОА и играет важную роль в его прогрессировании, однако пусковые факторы воспаления и механизм его влияния при остеоартрозе продолжают активно изучаться. В последние годы все большая роль в прогрессировании ОА отводится воспалению, в реализации которого процессы выработки и взаимодействия цитокинов могут быть определяющими. Например, интерлейкин-1β (ИЛ-1β) и фактор некроза опухоли α (ФНО-α) стимулируют хондроциты и способствуют синтезу металлопротеиназ и активаторов плазминогена, которые, в свою очередь, разрушают матрицу протеогликанов и коллагена [Moskowitz R.W., 2007]. Другие механизмы повреждения суставов и деградации хряща осуществляются через индукцию синтеза таких провоспалительных цитокинов, как ИЛ-1, ИЛ-6, ИЛ-8 и др. [Bonnet C.S., 2005; McLachlan C.S., 2007; Simon L.S., 2009].
Иммунопатологические реакции у больных ОА также сопряжены с активацией выработки активных форм кислорода нейтрофилами и моноцитами, обладающими мощным флогогенным потенциалом [Белозицкая-Смиян С.И., 1991; Алмазов В.А., Шляхто Е.В., Красильникова Е.И., Благосклонная Я.В., 2001]. При ОА, осложненном синовитом коленного сустава, на начальных этапах антиоксидантная система способна противодействовать активации кислородзависимого метаболизма нейтрофилов, в дальнейшем её потенциал истощается и развиваются комплексные иммунологические изменения, называемые «окислительным стрессом» [Алексеева Л.И., 2002]. Свободные радикалы, являясь высокореактивными соединениями, способны изменять структуру белков, вызывать перекисное окисление липидов, воздействовать на нуклеиновые кислоты, провоцируя развитие мутаций [Лила A.M., 2004]. Воспаление в суставе провоцируется и поддерживается продукцией ферментов и кислородных радикалов фагоцитами.
В последнее время значительно расширились представления о патогенезе ОА. Среди многочисленных воспалительных медиаторов при ОА важную роль отводят не только классу металлопротеиназ, в частности коллагеназ (металлопротеиназы (ММР): ММР-1, ММР-8 и ММР-13 и мембраная MMP-14), но и классам цитокинов (ИЛ-1 [Dingle et al., 1979; Goldring et al., 1988; Pfander et al., 2004]; ИЛ-6 [Kaneko et al,. 2000]; ИЛ-15 [Scanzello et al., 2009]; ИЛ-18 [Olee et al., 1999]; ФНО-α [Saklatvala, 1986]); хемокинов (чемерин [Huss et al., 2010]; ИЛ-8 [Chauffier et al., 2012; Kaneko et al., 2000]; MCP-1 [Vangsness et al., 2011]; MIP-1α [Hsu et al., 2004; Vangsness et al. ,2011]; RANTES [Hsu et al., 2004]; ростовых факторов (трансформирующий фактор роста-β (ТGF-β) [Blaney, Davidson et al., 2007]; VEGF [Haywood et al., 2003]); адипокинов (адипонектин [Conde et al., 2011]; лептин [Dumond et al., 2003]; резистин [Choe et al., 2012]; висфатин [Chen et al., 2010; Gosset et al., 2008]) и простагландинов/лейкотриенов (простагландин E2 [Martel-Pelletier et al., 2003]; лейкотриен LTB4 [Wittenberg et al., 1993]).
Согласно существующим в настоящее время представлениям, в белой жировой ткани синтезируется большое количество сигнальных веществ, а именно, лептин [Чубриева С. Ю., Глухов Н.В., Зайчик А.М., 2008; Косыгина А.В., 2011], ФНО-α [Hotamisligil G.S., Shargill N.S., Spiegelman B.M., 1993], ИЛ-6 [Yudkin J. S., Kumari M., Humphries S. E., 2000], ИЛ-8 [Bruun J. M., Lihn A. S., Madan A. K. et al., 2004], и соответствующие растворимые рецепторы. В последнее время были открыты новые адипоцитокины — оментин [Schaffler A., Neumeier M., Herfarth H. et al., 2005], висфатин [Fukuhara A., Matsuda M., Nihizawa M. et al., 2005] и протеин коллагенового происхождения с молекулярной массой 26 kDa (CORS-26), который также экспрессируется в моноцитах и клетках почек [Weigert J., Neumeier M., Schaffl er A. et al., 2005].
Поскольку жировая ткань широко представлена в организме человека, это означает, что общее количество адипоцитокинов, которые секретируются в ней, может в значительной степени влиять на процессы, происходящие в организме. Кроме того, каждый адипоцит связан с сосудистой сетью, что предполагает тот факт, что адипоцитокины адипоцитов легко и быстро попадают в кровеносное русло и индуцируют каскад воспалительных реакций.
В настоящее время известно, что существует два типа адипоцитокинов [Чубриева С. Ю., Глухов Н.В., Зайчик А.М., 2008; Косыгина А.В., 2011]: специфичные для жировой ткани биологически активные вещества, которые являются истинными адипоцитокинами (лептин, адипонектин и резистин), и другие, которые в изобилии секретируются жировой тканью, но не являются специфическими для жировой ткани (ингибитор-1 активатора плазминогена, ФНО-α и др.).
Лептин представляет собой не только центральный регулятор массы жира в организме, функционирующий путем снижения количества потребляемой пищи и увеличения расхода энергии, помимо этого он может быть вовлечен в индукцию резистентности к инсулину, возможно через периферические механизмы действия [Fruhbeck G., Jebb S.A., Prentice A., 1998]. Предполагается существование комплекса взаимодействий между сигнальными путями лептина и инсулина, которые могут приводить к модификации метаболических эффектов инсулина, осуществляющихся через субстраты инсулинового рецептора (IRS-1 и IRS-2). Лептин может действовать через некоторые компоненты сигнального каскада инсулина, типа IRS-1 и IRS-2, PI-3-киназы и МАР-киназы (митоген-активированной протеинкиназы), и может изменять вызванную инсулином экспрессию генов in vitro. Лептин быстро активизирует пути передачи сигналов непосредственно на уровне чувствительных к инсулину тканей, что накладывается на эффекты инсулина [Kim Y.B., Uotani S., Pierroz D. D. et al., 2000; Szanto I., Kahn C. R., 2000].
Физиологическая роль адипонектина в настоящее время полностью не изучена, однако предполагают, что данный адипоцитокин обладает антиатерогенными [Ouchi N., Kihara S., Arita Y. et al., 2000] и противовоспалительными свойствами [Yokota T., Oritani K., Takahashi I. et al., 2000]. Уровни адипонектина в плазме крови также снижены у пациентов с АГ. Эндотелий-зависимая вазореактивность нарушена у пациентов с гипоадипонектинемией, которую считают причиной АГ и по крайней мере одной из причин ожирения.
Исследования последних лет подтверждают тот факт, что жировая ткань также является важным источником секреции таких регуляторов метаболизма липопротеинов, такие как липопротеинлипаза (LPL), аполипопротеин Е (apoE) и белок-переносчик эфира холестерина (CETP).
Среди постоянно растущего числа вновь открываемых веществ, секретируемых адипоцитами, также можно назвать ангиотензиноген, ангиотензин-II [Engeli S., Sharma A. M., 2000], ингибитор активатора плазминогена-1 (PAI-1) [Sobel B. E, 1996], TGF-β [Samad F., Loskuttof D. J., 1996], адипонектин [Takahashi M., Arita Y., Yamagata K. et al., 2000] и другие.
Из белой жировой ткани крысы была выделена синтетаза оксида азота (NOS), и это указывает на то, что адипоциты являются потенциальным источником оксида азота (NO) [Ribiere C., Jaubert A. M., Gaudiot N. et al., 1996]. Andersson K. и соавт. (1999) была опубликована информация, что NO участвует в липолизе не только у крыс, но и у человека [Andersson K., Gaudiot N., Ribiere C. et al., 1999].
В последнее время большое внимание уделяется изучению роли инсулиноподобного фактора роста-I (IGF-I), глюкокортикоидов и половых стероидов в пролиферации, дифференцировке и распределении жировой ткани. Однако влияние протеина, стимулирующего ацилирование (ASP) [Murray I., Sniderman A. D., Havel P. J., Cianflone K.,1999], адипофилина [Heid H. W., Moll R., Schwetlick I. et al., 1998], резистина [McTernan P. G., McTernan C. L., Chetty R. et al., 200216], протеина агути (agouti) [Manne J., Argeson A.C., Siracusa L.D., 1995], апелина [Bełtowski J., 2006] и факторов, связанных с провоспалительными и иммунными процессами, по-прежнему требует дальнейших исследований [Boone C., Mourot J., Gregoire F. et al., 2000].
Таким образом, жировая ткань обладает ауто-, пара- и эндокринной функциями и может влиять на функцию других органов и систем, секретируя большое количество сигнальных молекул, обладающих различным биологическим действием, которые могут вызывать развитие сопутствующих ожирению осложнений и заболеваний.
В перекрестном исследовании с использованием базы данных корейских пациентов (fifth Korean National Health and Nutrition Examination Survey, 2010) и участием 2363 больных ОА старше 50 лет [ Shin D., 2014] данные мультифакторного регрессионного анализа выявили достоверную взаимосвязь между МС и рентгенологически подтвержденным ОА коленных суставов (ОШ составило 1,49; 95 % ДИ: 1,23-1,79; P < 0,001). Сила этой связи значительно не изменялась после учета других факторов, в том числе и инсулинорезистентности, однако стала не достоверной после поправки на ИМТ. Показатели с учетом возраста, пола и веса (или ИМТ) у пациентов с болевым синдромом в коленных суставах у пациентов с МС были достоверно выше по сравнению с пациентами без него (для тренда Р=0,01 и 0,04 соответственно). Таким образом, авторами сделан вывод о том, что связь между МС и рентгенологически подтвержденным ОА коленного сустава может быть в значительной степени объяснена избыточной массой тела больных, но не резистентностью к инсулину, что является ключевым фактором патофизиологии MС. Учитывая тот факт, что выраженость болевого синдрома у пациентов с ОА и МС больше независимо от ИМТ, само лечение МС может способствовать уменьшению болевого синдрома и улучшению функциональной активности пациентов с ОА.
По данным Гришиной Е.И. и соавт. (2011) у больных ОА и МС уровень провоспалительных цитокинов, таких как ФНО-α, ИЛ-6, ИЛ-8 выше, чем у пациентов с ОА без МС. Это связано с более тяжелым течением ОА у пациентов с МС с клинической точки зрения (худшие показатели индексов Лекена, WOMAC, HAQ, ВАШ боли) и подтверждается наличием позитивной корреляционной зависимости для ФНО-α с индексами Лекена, WOMAC, качеством жизни пациентов, интенсивностью болевого синдрома, для ИЛ-6 — с индексами Лекена, WOMAC, интенсивностью болевого синдрома, а для ИЛ-8 — с индексом Лекена. Полученные результаты свидетельствуют об активном участии провоспалительных цитокинов в реализации патологического процесса при комбинации ОА с МС [Гришина Е.И., Бабинец О.М., Шулика С.А., 2011].
Лечение МС подразумевает под собой выполнение 5 основных задач [Митченко Е.И., Корпачев В.В., Путай М.И. и др., 2008]: нормализацию массы тела, увеличение физической активности и применение антигипертензивных, липидоснижающих, антигипергликемических, а в некоторых случаях – антиагрегантых препаратов [Мамедов М.Н., 2011]. Выбор конкретных соматотропных препаратов наряду с модификацией способа жизни зависит от конкретной клинической ситуации.
Эффективность первоначальных мероприятий направленных на снижение массы тела и нормализацию метаболических нарушений продемонстрирована в ряде крупных многоцентровых исследований, таких как ТОНР-1, TAIM, TOMHS, XENDOS.
Антигипертензивные препараты, применяемые у больных с МС, должны оказывать пролонгированное действие (улучшение суточного контроля АД со снижением как дневного, так ночного уровня), способствовать регрессу поражения органов-мишеней (например, уменьшению гипертрофии левого желудочка), обладать метаболически положительным или нейтральным действием.
Препаратами первой линии коррекции артериального давления у лиц с МС и сахарным диабетом являются ингибиторы ангионтензинпревращающего фермента (ИАПФ), антагонисты рецепторов ангиотензина ІІ и агонисты имидазолиновых рецепторов.
В ряде крупных многоцентровых исследований (UKPDS, ABCD, CAPP, FACET) было доказано метаболически нейтральное (на углеводный и липидный обмен) и органопротективное действие ИАПФ. Целенаправленное выявление микроальбуминурии и адекватная гипотензивная терапия, включающая применение ИАПФ и блокаторов рецепторов ангиотензина ІІ, снижает частоту микро- и макрососудистых нарушений при СД 1-го и 2-го типа, а применение препаратов центрального действия (агонисты имидазолиновых рецепторов) способствует улучшению чувствительности тканей к инсулину, имеет выраженное кардиопротективное действие и способность уменьшать гипертрофию левого желудочка [Митченко Е.И., Корпачев В.В., Путай М.И. и др., 2008].
Целевые уровни АД при МС и сахарном диабете являются довольно жесткими. Часто для достижения этой цели необходима комбинация двух и даже трех групп препаратов. Вполне оправданной является комбинация препаратов первой линий с антагонистами кальция пролонгированного действия, селективными бета-блокаторами, тиазидоподобными диуретиками, индапамидом.
Нарушение липидного обмена является одним из основных компонентов МС и фактором риска развития атеросклеротического повреждения сердечно-сосудистой системы, поэтому у пациентов с данным синдромом следует использовать все возможные первичный и вторичные методы профилактики атеросклероза. Гиполипидемическую терапию назначают при неэффективности диетических мероприятий и при уровне ХСЛНП >3,35 ммоль/л, ТГ >2,3 ммоль/л, а у больных с подтвержденным атеросклерозом при уровне ТГ>1,7 ммоль/л [Перцева Т.О., Черкесова О,Г, Ярова І.Л., 2006].
Препаратами первой линии являются статины и фибраты.
Основной механизм действия статинов [Davidson M., 2002, Ballantyne C.M., Blazing M.A. et al., 2003] направлен на снижение внутриклеточного синтеза холестерина за счет обратимого блокирования фермента, что сопряжено с увеличением числа рецепторов к ЛПНП и повышением скорости удаления холестерина из кровотока. Помимо этого статины имеют противовоспалительный эффект, улучшают локальную функцию эндотелия, стабилизируют атеросклеротические бляшки. Современные статины наряду со снижением уровня ЛПНП (27-40 %) достоверно уменьшают уровень триглицеридов (6-30 %), повышают уровень ЛПВП (6-12 %) в зависимости от исходного уровня этих показателей и дозы препарата, предотвращают развитие сердечно-сосудистых событий на 24-37 % [Бабушкина А.В., 2010, Мамедов М.Н., 2007].
Производные фиброевой кислоты (фибраты) действуют путем расщепления частиц, богатых триглицеридами, снижают синтез свободных жирных кислот и повышают уровень ХС ЛПВП благодаря усиленной транскрипции генов и увеличенному катаболизму частиц ЛПНП [Grundy S.M., Vega G.L., Yuan Z. et al., 2006]. В исследованиях FIELD та DAIS выявлены положительные эффекты фенофибратов на дислипидемию, улучшение инсулиночувствительности, снижение концентрации мочевой кислоты. Фибраты уменьшают риск развития инфарктов, инсультов, смертности от ИБС [Бабушкина А.В., 2010, Rubins H.B., Robins S.J, Collins D. еt al., 1998].
Антигипергликемические препараты улучшают утилизацию глюкозы в периферических тканях и замедляют ее всасывание в кишечнике. К препаратам первой линии относят бигуаниды. При МС антигипергликемические препараты могут применяться на этапе предиабета, если изменение способа жизни не способствовало достижению целевых уровней гликемии натощак и/или через 2 часа после последнего приема пищи.
Нужно отметить, что все группы препаратов, применяемые для коррекции МС, наряду с основным действием на 10 % снижают уровень других компонентов. В отдельности каждый из них способствует снижению риска сердечно-сосудистых осложнений на 30 % [АТР III, 2001, Митченко Е.И., Корпачев В.В., Путай М.И. и др., 2007]. Для достижения целевых уровней основных компонентов МС и максимального снижения сердечно – сосудистых событий необходимо сочетание препаратов с различными механизмами действия. Ранняя диагностика МС у больных позволяет избегать полипрагмазии.
В настоящее время одним из наиболее изученных и эффективных средств для коррекции МС является метформин. Установлено, что препарат обладает гиполипидемическим и антиатерогенным действием [Bailey C.J., Turner R.C., 1996; Daskalopoulou S.S., Mikhailidis D.P., Elisaf M., 2004; Mamputu J.C., Wiernsperger N.F., Renier G.A., 2003], снижает риск тромбообразования [Bailey C.J., Turner R.C., 1996; Kirpichnicov D., McFarlane S.I., Sowers J.R, 2002]. Кроме того, имеются данные, что он способен ингибировать высвобождение провоспалительных цитокинов ИЛ-6, ИЛ-8 [Isoda K., Young J.L., Zirlik A., 2006], способствующих персистированию воспаления, в том числе и в тканях суставов, с развитием хондрита, остеита и синовита [Бадокин В.В., 2005].
При обследовании 68 больных ОА и МС, принимавших комбинированное лечение ОА (НПВП, внутрисуставные инъекции, физиотерапевтические методы) с включением метформина [Васильева Л.В., Лахин Д.И., 2010], показано, что за счет комплексного лечения в стационаре на 7-10-й день у пациентов обеих групп удалость достичь достоверного снижения выраженности болевого синдрома (по индексам ВАШ в покое и при движении, индексу Лекена, WOMAC (р<0,001)). Однако пациенты, получавшие метформин, смогли сохранить достоверность снижения выраженности болевого синдрома по всем показателям через 3, 6 и 12 мес. наблюдения, хотя показатели болевого синдрома и функциональной активности были несколько выше по сравнению с результатами, достигнутыми в стационаре. У пациентов основной группы на фоне лечения удалось уменьшить выраженность болевого синдрома и частоты синовитов через 6 и 12 мес. лечения, в то время как выраженность суставного синдрома у больных контрольной группы не только достоверно не отличалось к концу исследования от первоначальных, но даже наметилась тенденция к ухудшению показателей. Данные факты подтверждают положительное влияние терапии метформином на течение суставного синдрома и позволяют рекомендовать его включение в комплексное лечение больных ОА и МС.
На сегодняшний день оптимальное лечение ОА предусматривает комбинацию немедикаментозных и медикаментозных методов. При лечении OA коленных и тазобедренных суставов (Jordan K.M., Arden N.K., Doherty M. et al. EULAR recommendations, 2003; Zhang W., Doherty M., Arden N. et al., EULAR recommendations, 2005) необходимо учитывать: факторы риска ОА (избыточную массу тела, биомеханические факторы, физическую активность); общие факторы риска (возраст, коморбидность, полипрагмазия); уровень интенсивности болевого синдрома и функциональных нарушений; наличие воспалительного процесса; локализацию и степень структурного повреждения. Немедикаментозная терапия OA должна включать обучение пациента, физические упражнения, использование вспомогательных средств (супинаторы, фиксаторы коленного сустава и др.) и снижение массы тела. Медикаментозная терапия предусматривает использование неопиоидных и опиоидных анальгетиков, кортикостероидов и других лекарственных средств.
Снижение массы тела. Исследование, проведенное с участием 21 мужчин и женщины в старческом возрасте с ОА коленного сустава, рандомизированных в две группы (диета в сочетании с физическими упражнениями или только диета), показало, что пациенты первой группы в большей степени снизили свою массу тела. В обеих группах через 6 мес. отмечены положительные результаты в отношении улучшения физических возможностей, снижения интенсивности и частоты возникновения болевого синдрома в коленном суставе.
Нестероидные противовоспалительные препараты (НПВП) являются наиболее часто назначаемыми средства у пациентов с ОА во всем мире. Механизм их действия обусловлен угнетением превращения арахидоновой кислоты в простагландины путем ингибирования фермента циклооксигеназы (ЦОГ). Выделены два изофермента ЦОГ: ЦОГ-1 и ЦОГ-2. Изоформа ЦОГ-1 была выделена в 1976 году, а изоформа ЦОГ-2 позднее, в 1991 году. ЦОГ-1 существует в организме в норме, катализирует синтез простагландинов (ПГ), участвующих в многочисленных физиологических функциях, включая нормальное функционирование слизистой оболочки ЖКТ и агрегационные свойства тромбоксана 2 в тромбоцитах. ЦОГ-2 синтезируется только при повреждении тканей, индуцирует производство цитокинов и других медиаторов воспаления в ряде тканей, в том числе в эндотелиальных клетках и, считается, играет определенную роль в развитии боли, воспаления и лихорадки [Поворознюк В.В., Григорьева Н.В., 2004; Коваленко В.Н., Борткевич О.П., 2004; Косарев В.В., Бабанов С.А., 2011]. Продукция ЦОГ-2 значительно увеличивается в условиях воспаления. ПГ, образованные под влиянием ЦОГ-2, принимают участие в развитии и прогрессировании острого и хронического воспаления. Таким образом, ПГE2, расширяя артериолы, увеличивает приток крови в область воспаления, а ПГF2a – сужает венулы и затрудняет отток крови, что способствует развитию экссудации. Кроме того, ПГ вызывают гипералгезию и потенцируют действие других медиаторов воспаления.
Центральный механизм действия НПВП связан с угнетением синтеза простагландинов, которые синтезируются в центральной нервной системе и способствуют передаче болевого сигнала. НПВП снижают чувствительность болевых рецепторов, уменьшают отечность тканей в очаге воспаления, ослабляя механическое давление на ноцицепторы.
НПВП представляют разнородную группу препаратов с общими свойствами: анальгетический, противовоспалительный и жаропонижающий эффекты. Препараты могут быть классифицированы в зависимости от различных характеристик, включая ЦОГ-селективность, химические и фармакологические свойства. НПВП, как правило, имеют схожие химические формулы и принадлежат к слабым жирорастворимым кислотам, однако, существуют некоторые клинически значимые различия в фармакокинетических свойствах препаратов.
НПВП, как правило, имеют высокую биодоступность после перорального применения, хорошо абсорбируются из желудочно-кишечного тракта (ЖКТ). Тем не менее, скорость всасывания у различных НПВП варьирует, что может повлиять на кратность приема препарата. НПВП также могут быть классифицированы согласно периоду полураспада, выделяют две группы: с коротким периодом (<6 часов) и длительным периодом полувыведения. Этот показатель определяет рекомендации, касающиеся периодичности приема препарата. Средства с коротким периодом полувыведения (например, ибупрофен) обычно принимают каждые 6-8 часов, а препараты с более длительным периодом (например, напроксен и целекоксиб) вводят один или два раза в день. Скорость всасывания является ценной характеристикой препарата, особенно актуальной в случае острого болевого синдрома, так как именно она обеспечивает время наступления обезболивающего эффекта.
Традиционные неселективные НПВП ассоциируются с более высокой частотой развития серьезных гастроинтестинальных эффектов. Согласно литературным данным распространенность язв желудка и 12-ти перстной кишки у больных с долгосрочным приемом НПВП составляет около 20 %, а ежегодная частота серьезных осложнений от этих язв – 1-4 % [Laporte J., Ibáñez L., Vidal X. et al., 2004; Lanas A., Perez-Aisa M., Feu F. et al., 2005; Lanas A., García-Rodríguez L., Polo-Tomás M. et al., 2009].
У ЦОГ-2 селективных НПВП гастроинтестинальный профиль более благоприятный, что доказано серией клинических исследований, проведенных за последние 15 лет, но существуют данные о большем количестве неблагоприятных сердечно-сосудистых и почечных побочных эффектов. Поэтому, тщательное изучение сопутствующих заболеваний у пациента позволит врачу выбрать препарат, который будет эффективным и безопасным. Основным критерием в выборе препарата является соотношение пользы и риска развития побочных эффектов.
Особенности действия нимесулида. Среди ЦОГ-2 селективных препаратов наиболее исследованным остается нимесулид (4-нитро-2-феноксиметансульфонамид) – уникальный противовоспалительный препарат, отличающийся от большинства НПВП. Нимесулид – первый представитель нового класса селективных ингибиторов ЦОГ-2, представленных на мировом рынке. Он используется в клинической практике с 1985 г., когда впервые появился на фармацевтическом рынке Италии, а в настоящее время это лекарственное средство зарегистрировано более чем в 50 странах мира. Нимесулид наиболее часто назначаемый НПВП в Италии, Португалии, Франции [Mathew S., Devi G., Prasanth V., 2011]. Препарат был разработан в Швейцарии фирмой Helsinn Healthcare в 1980 году, в 1994 году было доказано преобладающее влияние нимесулида на ЦОГ-2, и подтверждено, в дальнейшем, многочисленными исследованиями. Воздействие на ЦОГ-1 осуществляется преимущественно в очаге воспаления, что обеспечивает дополнительный противовоспалительный эффект, а отсутствие влияния на ЦОГ-1 желудка и почек, в свою очередь, обусловливает высокий профиль безопасности [Барскова В.Г., 2011].
Препарат имеет высокую биодоступность, быстро и полностью всасывается из ЖКТ [Барскова В.Г., 2011]. После приема первой дозы в течение 30 мин достигается 25-80 % максимальной концентрации, в это же время, в среднем, наступает его анальгетический эффект. В синовиальной жидкости максимальная концентрация достигается аналогично концентрации в крови. Доказано, что фармакокинетика препарата не зависит от пола и возраста больного.
Механизмы действия нимесулида . Влияние нимесулида обусловлено класс-специфическими механизмами, характерными для большинства НПВП и эффектами именно нимесулида. Как и все представители класса, нимесулид обладает противовоспалительным, обезболивающим и жаропонижающим действием. Препарат снижает концентрацию короткоживущего ПГН2, из которого под действием ПГ-изомеразы образуется ПГЕ2. Уменьшение концентрации ПГЕ2 ведет к снижению степени активации простаноидных рецепторов ЕР-типа, что реализуется в анальгетический и противовоспалительный эффекты. Препарат обратимо подавляет образование ПГЕ2 не только в очаге воспаления, но и в восходящих путях ноцицептивной системы, включая пути проведения болевых импульсов в спинном мозге. На ЦОГ-1 нимесулид действует незначительно и, практически, не препятствует образованию ПГЕ2 из арахидоновой кислоты в физиологических условиях, благодаря чему снижается количество побочных эффектов препарата (рис. 1).
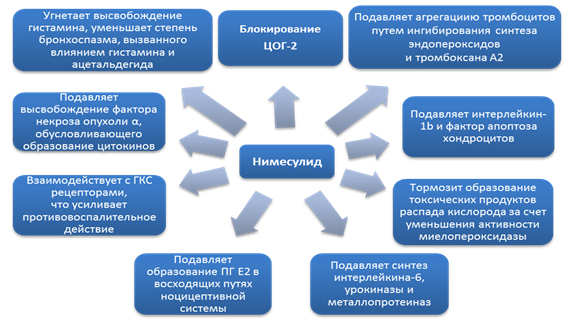
Рис. 1. Механизмы действия нимесулида .
Нимесулид подавляет агрегацию тромбоцитов путем ингибирования синтеза эндопероксидов и тромбоксана А2, подавляет синтез фактора агрегации тромбоцитов, подавляет высвобождение гистамина, а также уменьшает степень бронхоспазма, вызванного воздействием гистамина и ацетальдегида. Нимесулид ингибирует высвобождение фактора некроза опухоли α, который обусловливает образование цитокинов. Показано, что нимесулид способен подавлять синтез интерлейкина-6 и урокиназы, металлопротеиназ (эластазы, коллагеназы), замедляя разрушение протеогликанов и коллагена хрящевой ткани. Кроме того, нимесулид подавляет интерлейкин-1β и фактор апоптоза хондроцитов [Воробьева О.В., 2010].
Нимесулид обладает антиоксидантными свойствами, тормозит образование токсических продуктов распада кислорода за счет уменьшения активности миелопероксидазы, влияет на продукцию и действие окислительных радикалов, а также других компонентов нейтрофильной активации, что усиливает противовоспалительный и анальгетический эффекты и снижает вероятность гастро-интестинальной ульцерогенности. Взаимодействие нимесулида с ГКС рецепторами и активация их путем фосфорилирования усиливает противовоспалительное действие препарата.
Безопасност ь нимесулида. Нимесулид хорошо переносится, что выгодно отличает его от многих других представителей группы НПВП. Большинство побочных эффектов нимесулида являются класс-специфичными и зависят, в определенной степени, от фармакокинетики препарата.
Наиболее частым осложнением для всего класса НПВП является влияние на слизистую оболочку ЖКТ. Изучению этого явления посвящено большое количество исследований. В исследовании F. Bradbury, где проведена оценка частоты осложнений со стороны ЖКТ при применении диклофенака (n = 3553), нимесулида (n = 3807) и ибупрофена (n = 1470) в реальной клинической практике, суммарная частота этой патологии при использовании нимесулида была существенно меньше в сравнении с диклофенаком (12,1 %) и не отличалась от таковой при использовании ибупрофена (8,1 и 8,6 %) [Bradbury F., 2004]. Итальянские исследователи A. Conforti et al. провели анализ 10608 сообщений о серьезных побочных явлениях, связанных с приемом различных НПВП с 1988 по 2000 год. Оказалось, что нимесулид был причиной развития тех или иных осложнений со стороны ЖКТ в 2 раза реже, чем другие НПВП. Таким образом, количество нежелательных явлений при применении нимесулида составило 10,4 %, диклофенака – 21,2 %, кетопрофена – 21,7 %, пироксикама – 18,6 % [Conforti A., Leone R., Moretti U. et al., 2001]. Риск развития желудочно-кишечного кровотечения при использовании нимесулида в реальной клинической практике оценивался в масштабном эпидемиологическом исследовании J. Laporte et al. Согласно полученным результатам, относительный риск кровотечения для нимесулида составил 3,2, для диклофенака – 3,7, мелоксикама – 5,7, а рофекоксиба – 7,2 [28].
Гастроинтестинальная безопасность нимесулида обусловлена отсутствием влияния на ЦОГ-1 и химическими свойствами препарата. Большинство традиционных НПВП по химической структуре – кислоты, которые повышают проницаемость тонкого кишечника. Это является дополнительным, не связанным с угнетением синтеза ПГ, механизмом развития гастропатии. Нимесулид, напротив, имеет слабые кислотные свойства и не накапливается в слизистой оболочке желудка и кишечника. Кроме того, нимесулид снижает продукцию окислительных радикалов и лейкотриенов, а также выброс гистамина из тучных клеток, чем создает дополнительную протекцию слизистой оболочки ЖКТ. В многочисленных клинических исследованиях при различных заболеваниях костно-мышечной системы доказано, что подавляющее большинство побочных реакций для нимесулида со стороны ЖКТ транзиторные, слабо выраженные и слабо коррелируют с ульцерогенным эффектом. Двойное слепое исследование с использованием гастродуоденоскопии показало, что применение нимесулида в дозе 100 или 200 мг в течение 7 дней не приводило к изменениям слизистой оболочки по сравнению с плацебо. Таким образом, можно констатировать, что нимесулид крайне редко вызывает тяжелые гастроинтестинальные осложнения, что особенно важно для лиц старших возрастных групп.
Принципиальное значение для оценки безопасности нимесулида имеет опыт его длительного применения. Так, в работе P. Locker et al. 199 больных с ОА получали нимесулид (200 мг/д) или этодолак (600 мг/д) в течение 3 мес. Терапевтический потенциал нимесулида оказался выше: его действие оценили как «хорошо» или «отлично» 80 % больных, в то время как препарату сравнения аналогичную оценку дали только 68 % больных. При этом, хотя этодолак относится к селективным НПВП и считается препаратом с очень хорошей переносимостью, количество побочных эффектов в обеих группах лечения не отличалось. В масштабном исследовании Huskisson et al. нимесулид (200 мг/д) или диклофенак (150 мг/д) были назначены 279 пациентам с ОА, причем продолжительность терапии составила 6 мес. Эффективность препаратов, которую оценивали по динамике самочувствия больных и функциональному индексу Лекена, оказалась фактически одинаковой. Однако нимесулид существенно превосходил диклофенак по переносимости: появление побочных эффектов со стороны ЖКТ регистрировалось в 36 и 47 % больных соответственно (p<0,05). В настоящее время наиболее длительным и большим рандомизированным двойным слепым исследованием нимесулида остается работа W. Kriegel et al. В этом исследовании определялись эффективность и безопасность нимесулида (200 мг/д) и напроксена (750 мг/д) у 370 больных с ОА в течение 12 мес. Как и в работе Huskisson, эффективность обоих препаратов оказалась сопоставимой. Количество осложнений при использовании нимесулида также оказалось меньшим: суммарно 47,5 % (54,5 % – у пациентов, получавших напроксен). Очень важно, что ни в одной из трех представленных работ не зафиксировано значимого повышения частоты кардиоваскулярных осложнений на фоне длительного приема нимесулида.
Применение нимесулида связано с низкой частотой аллергических реакций. Нимесулид обладает также дополнительными эффектами, которые реализуют его гипоаллергенность, в частности, он подавляет фосфодиэстеразу IV, редуцирует выброс гистамина из базофилов и тучных клеток. Эти дополнительные свойства позволяют рассматривать нимесулид как альтернативный противовоспалительный препарат для пациентов с реакциями гиперчувствительности на традиционные НПВП [Воробьева О.В., 2010].
Обсуждая вопросы безопасности нимесулида, необходимо остановиться на риске гепатотоксических реакций. В последние годы проблема гепатотоксичности НПВП активно обсуждается в мировой литературе. По данным многолетней статистики, тяжелые гепатотоксические осложнения развиваются примерно у 1 из 10 тыс. больных [Каратеев А.Е., 2009]. Что касается нимесулида, то за период 15 летнего применения этого препарата в мировой клинической практике (~ 50 разных стран за период с 1985 по 2000 год) всего отмечено 192 эпизода значимых осложнений со стороны печени. Учитывая, что к 2000 г. нимесулидом было пролечено 280 млн. больных, суммарная частота опасных гепатотоксических реакций, таким образом, составляет менее 0,1 эпизода на 100 тыс. пролеченных больных. Однако, контролирующие органы ряда европейских стран, последней из которых была Ирландия, прекратили использование нимесулида на своей территории, обосновывая свое решение статистическими данными спонтанных сообщений о тяжелых гепатотоксических реакциях. Тем не менее EMEA (European Medicines Agency ) – основной орган Европейского союза, обеспечивающий контроль над оборотом лекарственных препаратов в Европе, после обсуждения сложившейся ситуации не нашел достаточных оснований для прекращения использования нимесулида (пресс-релиз от 21.09.07 г.). Очень важно, что в этом документе, как отметили авторы обзора по нимесулиду Mattia C.C. et. al. (2010), содержится признание того факта, что гепатотоксичность нимесулида не выше гепатотоксичности многих других НПВП, активно применяющихся в Европе [Каратеев А.Е., 2009]. При этом было принято компромиссное решение: рекомендовать использование нимесулида в странах Европы ограниченным курсом (не более 15 дней) в дозе, не превышающей 200 мг/д. Действительно, результаты рандомизированных клинических исследований показывают, что отрицательная динамика изменений лабораторных биохимических показателей, свидетельствующих о повреждении печени, отмечается при использовании нимесулида с такой же частотой, как и на фоне приема других НПВП.
Очередное обсуждение вопроса гепатотоксичности нимесулида было проведено медицинским руководством Евросоюза 23 июня 2011 г. Решение EMEA вновь подтвердило основные положения, обозначенные в пресс-релизе от 21.09.2007 г. Преимущества нимесулида при кратковременном использовании с целью уменьшения острой боли явно превышают его недостатки и оправдывают его дальнейшее использование.
На основании проведенного анализа можно сделать вывод, что краткосрочное применение нимесулида в лечении пациентов с ОА эффективно и оправдано, а вероятность развития нежелательных явлений при применении данного лекарственного средства не превышает риск подобных осложнений при приеме других НПВП.
Таким образом, нимесулид – уникальный представитель класса НПВП, быстро и эффективно уменьшает болевой синдром за счет действия не только на ЦОГ-2, но и непосредственно на элементы ноцицептивной системы. На сегодняшний день применение нимесулида удачно решает проблему легкой и умеренной боли в амбулаторной практике, однако в последнее время при длительном лечении болевого синдрома у больных с ОА все большее предпочтение отдают амтолметин гуацилу, который обладает выраженным противовоспалительным, анальгезирующим, жаропонижающим, десенсибилизирующим действием. Кроме того, отличительной особенностью этого препарата является то, что он – единственный представитель группы НПВП, обладающий и гастропротекторным эффектом.
В настоящее время установлено, что одним из важнейших «передатчиков» биологических сигналов, который принимает участие в регуляции разнообразных физиологических функций является NO (оксид азота). С его действием связывают такие процессы, как замедление агрегации тромбоцитов и миграции нейтрофилов через сосудистую стенку, расслабление гладкомышечных клеток интимы сосудов, неоангиогенез, неонейрогенез и др. Подобно простагландинам, в области воспаления и повреждения ткани NO способен выступать в «негативной» роли медиатора боли, вызывающего сенситизацию и прямую стимуляцию ноцицепторов. Синтез этой маленькой молекулы происходит при помощи фермента NO-синтетазы (NOS). Известны несколько NOS: одни из них являются конститутивными (эндотелиальная, eNOS, и нейрональная, nNOS); синтез же NO в области патологического процесса определяется индуцируемой изоформой данного фермента, iNOS. В слизистой ЖКТ NO выполняет защитную функцию, усиливая кровоток, репарацию эпителиоцитов, препятствуя развитию воспаления (во многом благодаря подавлению хемотаксиса нейтрофилов) и блокируя свободнорадикальные процессы. При этом основное количество этого вещества образуется при участии iNOS, которая экспрессируется в ответ на повреждение эпителиальных клеток, вызванное различными факторами агрессии, такими как H. pylori, НПВП и соляная кислота [Каратеев А.Е., 2009]. По данным проводимых в последние годы исследований, насыщение слизистой оболочки ЖКТ окисью азота «извне» может повысить устойчивость слизистой к повреждению.
Амтолметина гуацил (АМГ) получен путем добавления к молекуле толметина аминокислоты ванилина, что привело к существенному изменению его фармакологических свойств. В отличие от своего предшественника он приобрел гастропротективные свойства, связанные в первую очередь с подавлением активности ингибиторов iNOS, что приводит к существенному повышению концентрации NO в слизистой оболочке ЖКТ. В экспериментальных работах. было показано многократное нарастание активности iNOS в слизистой оболочке ЖКТ лабораторных животных, получавших АМГ; ни плацебо, ни толметин такого эффекта не оказывали [Yuan-Hai Li, Jun Li, Yan Huang et al., 2004; Coruzzi G., Coppelli G, Spaggiari S. еt al., 2004].
В исследовании Tubaro E. и соавт. продемонстрировано дозозависимое подавление стимулированной желудочной секреции АМГ, т. о. установлены его антисекреторные свойства. АМГ значиомо усиливал секрецию бикарбоната, являющегося основой щелочного буфера слизистой оболочки желудка. Кроме того, АМГ снижал повреждающее действие других НПВП. Так, по сравнению с плацебо или толметином, на фоне введения АМГ у лабораторных животных выявлено достоверное дозозависимое уменьшение выраженности ульцерации, вызванной приемом индометацина [Tubaro E., Belogi L., Mezzadri C.M., 2000].
После всасывания АМГ сразу подвергается гидролизу эстеразами плазмы крови с образованием трех метаболитов: MED5, толметин и гвиакол, трансформирующихся до активного метаболита толметина, который проникает в ткани, оказывая фармакологическое действие.
Защитное действие АМГ на слизистую оболочку желудка реализуется путем стимуляции рецепторов капсаицина (также их называют ваниллоидными рецепторами), присутствующих в стенках ЖКТ. Вследствие того, что в составе АМГ присутствует ванилиновая группа, он может стимулировать капсаициновые рецепторы, что в свою очередь вызывает высвобождение пептида, кодируемого геном кальцитонина, и последующее увеличение продукции NO. Оба этих действия создают противовес отрицательному эффекту, вызываемому снижением количества ПГ из-за ингибирования ЦОГ.
Во многочисленных иследованиях показано, что амтолметина гуацил эффективно подавляет провоспалительные факторы, снижает агрегацию тромбоцитов; угнетает ЦОГ-1 и ЦОГ-2, нарушает метаболизм арахидоновой кислоты, уменьшает образование ПГ (в т.ч. в очаге воспаления), подавляет экссудативную и пролиферативную фазы воспаления. Он уменьшает проницаемость капилляров; стабилизирует лизосомальные мембраны; тормозит синтез или инактивирует медиаторы воспаления (ПГ, гистамин, брадикинины, цитокины, факторы комплемента), блокирует взаимодействие брадикинина с тканевыми рецепторами, восстанавливает нарушенную микроциркуляцию и снижает болевую чувствительность в очаге воспаления. Кроме того, он влияет на таламические центры болевой чувствительности; снижает концентрацию биогенных аминов, обладающих альгогенными свойствами; увеличивает порог болевой чувствительности рецепторного апарата, а также устраняет или уменьшает интенсивность болевого синдрома, уменьшает утреннюю скованность и отечность, увеличивает объем движений в пораженных суставах через 4 дня лечения применения.
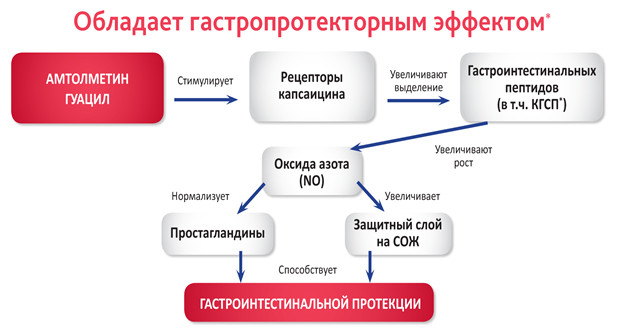
Рис. 2. Механизм гастропротекторного эффекта амтолметина гуацила.
Амтолметин гуацил хорошо переносится пациентами при длительном применении (в течение 6 мес). Всасывание АМГ после перорального приема является быстрым и полным. Препарат, в основном, концентрируется в стенках желудка и кишечника, где в течение 2 ч после приема поддерживается его очень высокая концентрация.
Таким образом, в настоящее время установлено, что остеартроз является важной медико-социальной проблемой, особенно среди пациентов старших возрастных групп. В последнее время отмечено значительное сочетание этой патологии с другими заболеваниями, в том числе формирующими метаболический синдром, что делает проблему коморбидности особенно актуальной. Эффективное и безопасное длительное лечение ОА предполагает прием препаратов, которые не только обладают выраженным анальгетическим и противовоспалительным эффектом, отсутствием разрушающего действия на хрящ, но и обеспечивают хороший профиль их безопасности. В связи с этим применение умеренно селективных препаратов (найз) позволяет уменьшить риск возникновения побочных эффектов со стороны сердечно-сосудистой системы и ЖКТ. При решении вопроса о длительной терапии ОА использование препарата найзилат является методом выбора, в связи не только с доказанной эффективностью в лечении данной группы пациентов, но и выраженным гастропротекторным эффектом.