Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "ПОДХОДЫ К ЛЕЧЕНИЮ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ: СОСТОЯНИЕ ПРОБЛЕМЫ В 2015-2016 ГГ."
Автор: Багрий А.Э., Хоменко М.В.
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Кардиология, Неврология, Ревматология, Семейная медицина/Терапия
Просмотров: 3 375
Дата проведения: с 18.11.2015 по 18.11.2016
 Лечение артериальной гипертензии представляет одну из наиболее актуальных проблем кардиологии. АГ является наиболее важным и наиболее распространенным среди модифицируемых факторов сердечно-сосудистого риска; эксперты полагают, что около 1 миллиарда человек в мире имеют АГ; в развитых странах артериальное давление (АД) повышено у 1/3–1/2 взрослого населения. Важно подчеркнуть, что адекватный контроль АГ с достижением целевых цифр АД позволяет существенно снизить уровни сердечно-сосудистой и сосудисто-мозговой смертности в популяции, значительно замедлить темпы прогрессии хронических заболеваний почек.
Лечение артериальной гипертензии представляет одну из наиболее актуальных проблем кардиологии. АГ является наиболее важным и наиболее распространенным среди модифицируемых факторов сердечно-сосудистого риска; эксперты полагают, что около 1 миллиарда человек в мире имеют АГ; в развитых странах артериальное давление (АД) повышено у 1/3–1/2 взрослого населения. Важно подчеркнуть, что адекватный контроль АГ с достижением целевых цифр АД позволяет существенно снизить уровни сердечно-сосудистой и сосудисто-мозговой смертности в популяции, значительно замедлить темпы прогрессии хронических заболеваний почек.
Настоящий семинар посвящен обсуждению вопросов современной лечебной тактики при АГ (в первую очередь, медикаментозной). С учетом того что общие вопросы АГ, включая ее этиологию, патогенез, классификацию, вопросы диагностики (лабораторной, инструментальной, в т.ч. амбулаторного мониторирования АД) достаточно часто представляются в периодической печати, здесь мы сочли возможным этих аспектов проблемы АГ практически не касаться. Нами будут рассмотрены кратко общие вопросы лечения АГ, применение комбинированной антигипертензивной терапии, представлены данные о различных классах антигипертензивных препаратов. Особое внимание будет уделено вопросам резистентной АГ, а также некоторым симптоматическим АГ (включая почечные, реноваскулярные и так называемые «надпочечниковые»). Отдельно будет рассматриваться возможность применения метаболической терапии (Мельдоний) при АГ.
Общие подходы к лечению АГ
Схематично эти подходы представлены на рисунке 1. Позволим себе лишь кратко их прокомментировать: (1) пациент нуждается в обстоятельном и серьезном разъяснении того, что лечение АГ – важный путь к уменьшению степени его / ее сердечно-сосудистого риска, что лечение АГ должно быть постоянным, требует контроля за уровнями АД (в т.ч. дома), с ведением дневника, регулярных визитов к врачу; лечение АГ – важная и серьезная жизненная задача для пациента; (2) указанные на рисунке 1 целевые уровни АД должны быть также обсуждены с больным, они должны быть письменно указаны в рекомендациях, ему предоставленных; (3) немедикаментозные подходы обычно включают устранение курения, ограничение поваренной соли, снижение массы тела для тучных лиц, умеренные уровни физической активности на воздухе и др.; врачу не следует пренебрегать разъяснением (часто – повторным!) необходимости этих мер; (4) наиболее часто применяемые классы антигипертензивных препаратов указаны на рисунке, чаще они используются не изолированно, но в виде различных комбинаций (см. ниже); (5) если уровень сердечно-сосудистого риска у пациента высокий или очень высокий, то в лечебный режим следует включить статин (например, аторвастатин – 10 мг/сут) и ацетилсалициловую кислоту (последняя – при достижении целевых уровней АД, дозы – 75-100 мг/сут), если нет противопоказаний.

Рисунок 1. Общие подходы к лечению АГ
Примечания: ИАПФ – ингибитор ангиотензин-превращающего фермента; ТПД – тиазидоподобный диуретик; ТД – тиазидный диуретик; БКК – блокатор кальциевых каналов; β-АБ – β-адреноблокатор; АСК – ацетилсалициловая кислота
Комбинированная антигипертензивная терапия
На рисунке 2 представлены подходы к выбору лечебной тактики при АГ, рекомендованные экспертами ESC/ESH в 2013 году. При выборе в качестве начального подхода монотерапии антигипертензивным препаратом предпочтение обычно оказывают блокатору кальциевых каналов либо тиазидному диуретику, при необходимости к ним добавляют либо ингибитор АПФ, либо сартан.
Многим больным уже на начальном этапе лечения может быть назначена комбинированная антигипертензивная терапия двумя препаратами. Эксперты ESC/ESH (2013) рекомендуют следующие комбинации антигипертензивных препаратов (рис. 3). При необходимости используют трехкомпонентную антигипертензивную терапию (как правило, блокатор кальциевых каналов тиазидный диуретик ингибитор АПФ / сартан).
Предлагаем примерный алгоритм выбора тактики антигипертензивной терапии у пациентов с АГ (рис. 4), имеющих различные сопутствующие заболевания, рекомендованный экспертами JNC-8 (2014).
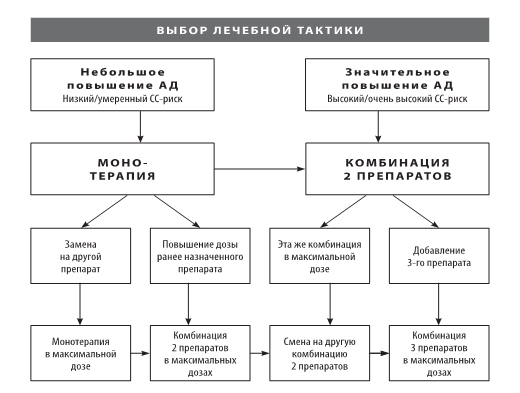
Рисунок 2. Подходы к выбору монотерапии или комбинированной терапии при АГ (адаптировано из Рекомендаций ESC / ESH, 2013)
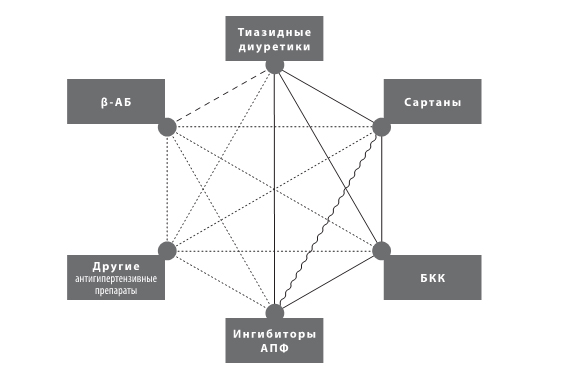
Рисунок 3. Комбинации антигипертензивных препаратов (адаптировано из Рекомендаций ESC / ESH, 2013)
Примечания: сплошная линия – предпочтительные (рациональные) комбинации; штриховая – рациональная комбинация, но с некоторыми ограничениями; пунктирная линия – возможные, но менее изученные комбинации; волнистая – нерекомендованная комбинация.
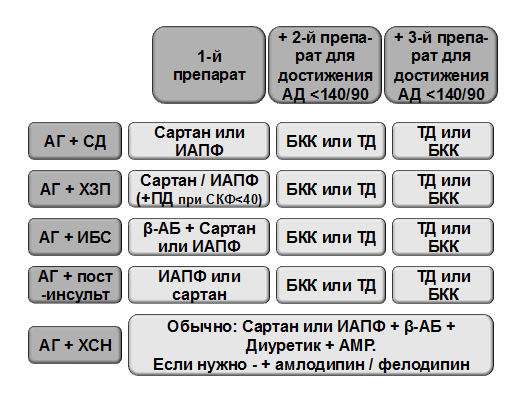
Рисунок 4. Лечение АГ при сопутствующих заболеваниях
Примечания: СД – сахарный диабет, ХЗП – хроническое заболевание почек, ИБС – ишемическая болезнь сердца, ХСН – хроническая сердечная недостаточность, ИАПФ – ингибитор АПФ, БКК – блокатор кальциевых каналов, ТД – тиазидный диуретик, АМР – антагонист минералокортикоидных рецепторов
ХАРАКТЕРИСТИКА КЛАССОВ АНТИ-АГ ПРЕПАРАТОВ
Диуретики
 1. Тиазидовые (гидрохлоротиазид – 12,5-50 мг 1 р/сут) и тиазидоподобные (индапамид – 1,25-2,5 мг 1 р/сут): (1) наиболее часто применяемые для длительного лечения АГ представители класса диуретиков; (2) широко используются в комбинациях с ингибиторами АПФ / сартанами, блокаторами кальциевых каналов, калий-сберегающими диуретиками; (3) нередко представлены в виде фиксированных комбинаций; (4) являются препаратами выбора в лечении АГ у пожилых (в т.ч. при изолированной систолической АГ), у лиц с избыточной массой тела, при наличии сопутствующей сердечной недостаточности, у постинсультных больных, при рецидивирующих кальциевых конкрементах в почках, при резистентной АГ; (5) уменьшают потери кальция, способствуют замедлению развития остеопороза; (6) их эффективность уменьшается при сниженной функции почек, поэтому при скорости клубочковой фильтрации (СКФ) < 60 мл/мин требуется добавление петлевых диуретиков; (7) противопоказаны больным с подагрой; (8) с осторожностью применять у лиц с сахарным диабетом, аортальным стенозом; (9) среди побочных эффектов гипокалиемия, гипомагниемия, дислипидемия, аритмии (в т.ч. жизнеопасные) и др.
1. Тиазидовые (гидрохлоротиазид – 12,5-50 мг 1 р/сут) и тиазидоподобные (индапамид – 1,25-2,5 мг 1 р/сут): (1) наиболее часто применяемые для длительного лечения АГ представители класса диуретиков; (2) широко используются в комбинациях с ингибиторами АПФ / сартанами, блокаторами кальциевых каналов, калий-сберегающими диуретиками; (3) нередко представлены в виде фиксированных комбинаций; (4) являются препаратами выбора в лечении АГ у пожилых (в т.ч. при изолированной систолической АГ), у лиц с избыточной массой тела, при наличии сопутствующей сердечной недостаточности, у постинсультных больных, при рецидивирующих кальциевых конкрементах в почках, при резистентной АГ; (5) уменьшают потери кальция, способствуют замедлению развития остеопороза; (6) их эффективность уменьшается при сниженной функции почек, поэтому при скорости клубочковой фильтрации (СКФ) < 60 мл/мин требуется добавление петлевых диуретиков; (7) противопоказаны больным с подагрой; (8) с осторожностью применять у лиц с сахарным диабетом, аортальным стенозом; (9) среди побочных эффектов гипокалиемия, гипомагниемия, дислипидемия, аритмии (в т.ч. жизнеопасные) и др.
2. Петлевые (фуросемид – по 20–40 мг 1–3 р/сут; торасемид – по 5–10 мг 1 р/сут): (1) для хронического лечения АГ применяются главным образом у лиц со сниженной функцией почек (при СКФ <50-60 мл/мин – обязательный компонент антигипертензивной терапии; фуросемид при этом – обычно 2-3 раза в сутки, его суточная доза может составлять ≥120 мг, торасемида – ≥50 мг); (2) широко используются для контроля задержки жидкости при хронической сердечной недостаточности со сниженной систолической функцией левого желудочка (в т.ч. при наличии у них АГ); (3) парентерально применяются в лечении гипертензивных кризов.
 3. Антагонисты минералокортикоидных рецепторов (спиронолактон – 12,5–50 мг/сут на 1–3 приема; эплеренон 25–100 мг/сут на 1–2 приема): (1) рассматриваются как часто применяемые 4–5 антигипертензивные препараты при резистентной АГ; (2) препараты выбора у лиц с первичным альдостеронизмом; (3) используются для улучшения сердечно-сосудистого прогноза у лиц с острым инфарктом миокарда и у постинфарктных, при хронической сердечной недостаточности; (4) широко используются в комбинированной диуретической терапии ( тиазидовые или петлевые); (5) антигипертензивный эффект выше у спиронолактона, чем у эплеренона; (6) серьезные проблемы для спиронолактона при длительном применении – гинекомастия (также – дисменорея, снижение либидо); (7) для обоих препаратов – возможна гиперкалиемия, особенно при сочетании с ингибитором АПФ / сартаном; требуется контроль уровней калия крови; (8) не применять при СКФ <30–50 мл/мин.
3. Антагонисты минералокортикоидных рецепторов (спиронолактон – 12,5–50 мг/сут на 1–3 приема; эплеренон 25–100 мг/сут на 1–2 приема): (1) рассматриваются как часто применяемые 4–5 антигипертензивные препараты при резистентной АГ; (2) препараты выбора у лиц с первичным альдостеронизмом; (3) используются для улучшения сердечно-сосудистого прогноза у лиц с острым инфарктом миокарда и у постинфарктных, при хронической сердечной недостаточности; (4) широко используются в комбинированной диуретической терапии ( тиазидовые или петлевые); (5) антигипертензивный эффект выше у спиронолактона, чем у эплеренона; (6) серьезные проблемы для спиронолактона при длительном применении – гинекомастия (также – дисменорея, снижение либидо); (7) для обоих препаратов – возможна гиперкалиемия, особенно при сочетании с ингибитором АПФ / сартаном; требуется контроль уровней калия крови; (8) не применять при СКФ <30–50 мл/мин.
4. Калий-сберегающие (амилорид – 5-10 мг 1 р/сут; триамтерен – 100 мг 1 р/сут): (1) сейчас расширяют свое применение как 4–5 препараты в лечении резистентной АГ; (2) применяются главным образом в составе фиксированных комбинаций с гидрохлоротиазидом; (3) из побочных эффектов особое внимание обращаем на гиперкалиемию
Ингибиторы ангиотензин-превращающего фермента (АПФ)
1. Например, зофеноприл – 30–60 мг 1 р/сут; квинаприл – 5–40 мг/сут – на 1–2 приема; лизиноприл – 5–40 мг 1 р/сут; периндоприл – 5–10 мг 1 р/сут; рамиприл – 2,5–10 мг/сут на 1–2 приема; фозиноприл – 10–40 мг 1 р/сут; эналаприл – 5–40 мг/сут на 1–2 приема.
2. Одна из наиболее широко востребованных в современной кардиологии групп лекарственных препаратов. Обладает многочисленными органопротекторными (кардио-, вазо-, ренопротекторными) эффектами, а также доказанным в крупных исследованиях благоприятным влиянием на сердечно-сосудистый прогноз. Наряду с лечением АГ используется как базисная группа у пациентов с острым коронарным синдромом, хронической ишемической болезнью сердца, хронической сердечной недостаточностью, сахарным диабетом, хроническими заболеваниями почек, у постинсультных.
 3. При лечении АГ применяются как изолированно, так и в разнообразных сочетаниях с другими антигипертензивными препаратами (наиболее часто – с диуретиками и/или блокаторами кальциевых каналов). Ингибиторы АПФ не следует сочетать с сартанами.
3. При лечении АГ применяются как изолированно, так и в разнообразных сочетаниях с другими антигипертензивными препаратами (наиболее часто – с диуретиками и/или блокаторами кальциевых каналов). Ингибиторы АПФ не следует сочетать с сартанами.
4. Обычно хорошо переносятся. Среди побочных эффектов – кашель (у 10–15% лиц белокожей популяции и до 20–30% – у лиц азиатского происхождения; более часто – у женщин и у пожилых; при его развитии обычно следует заменить ингибитор АПФ на сартан).
5. Другие побочные эффекты – гиперкалиемия, снижение функции почек (особенно у лиц, исходно имевших сниженную функцию почек, принимающих нестероидные противовоспалительные препараты, имеющие стенозирование почечных артерий), гипотензия.
6. Ингибиторы АПФ противопоказаны при беременности (особенно во 2 и 3 триместрах), так как их применение может нарушить нормальное развитие плода.
Сартаны (антагонисты рецепторов ангиотензина II )
1. Например, азилсартан 40–80 мг 1 р/сут; валсартан – 80–320 мг/сут на 1-2 приема; ирбесартан – 150–300 мг 1 р/сут; кандесартан – 4–32 мг 1 р/сут; лосартан 50–100 мг/сут на 1-2 приема; олмесартан – 10–40 мг 1 р/сут; телмисартан – 40–80 мг 1 р/сут.
2. Как и ингибиторы АПФ, представляет один из наиболее употребляемых в лечении АГ классов лекарственных препаратов. Обладает широким набором органопротекторных свойств, а также серьезными доказательствами благоприятного действия на сердечно-сосудистый прогноз.
3. В силу сравнимого с ингибиторами АПФ спектра благоприятных эффектов в сочетании со значительно лучшей переносимостью (для сартанов практически не характерен кашель) они при АГ применяются все более широко (обычно сейчас – не при непереносимости ингибиторов АПФ, как это было ранее, но чаще всего – как первое назначение). Обратим внимание читателя на рисунок 4, где при перечислении пары «сартан или ингибитор АПФ» на первом месте даже при различных сопутствующих состояниях указан именно сартан (в англоязычном подлиннике так, хотя если бы группы перечислялись по алфавиту, то сначала бы указывались ингибиторы АПФ – ACE Inhibitors, а затем уже сартаны – ARBs)
 4. Наряду с АГ находят применение в лечении пациентов с острым коронарным синдромом, хронической ишемической болезнью сердца, хронической сердечной недостаточностью со сниженной систолической функцией левого желудочка, сахарным диабетом, хроническими заболеваниями почек, постинсультных. Кандесартан и валсартан могут улучшать когнитивную функцию у пожилых лиц. Сартаны, как и ингибиторы АПФ, могут уменьшать толерантность к органическим нитратам.
4. Наряду с АГ находят применение в лечении пациентов с острым коронарным синдромом, хронической ишемической болезнью сердца, хронической сердечной недостаточностью со сниженной систолической функцией левого желудочка, сахарным диабетом, хроническими заболеваниями почек, постинсультных. Кандесартан и валсартан могут улучшать когнитивную функцию у пожилых лиц. Сартаны, как и ингибиторы АПФ, могут уменьшать толерантность к органическим нитратам.
5. Используются нередко в комбинациях с другими антигипертензивными препаратами, в том числе в фиксированных комбинациях (с диуретиками и/или блокаторами кальциевых каналов). Не рекомендовано сочетание их с ингибиторами АПФ.
6. Среди побочных эффектов – гиперкалиемия, снижение функции почек (как и для ингибиторов АПФ – чаще у лиц с исходно нарушенной функцией почек, а также у одновременно принимающих нестероидные противовоспалительные препараты). Сартаны противопоказаны при беременности.
Блокаторы кальциевых каналов
1. Дигидропиридиновые (например, амлодипин – 2,5–10 мг 1 р/сут; лерканидипин – 10–40 мг 1 р/сут; нифедипин продленного действия – 20–90 мг/сут на 1–2 приема; фелодипин – 2,5–10 мг/сут на 1-2 приема): (1) широко применяются в лечении различных категорий пациентов с АГ, в том числе у пожилых, при сопутствующих сахарном диабете, ожирении, метаболическом синдроме, хронической ишемической болезни сердца, у лиц с перенесенными мозговыми инсультами, с периферическими сосудистыми поражениями ( синдромом Рейно); (2) обычно являются компонентом стандартных комбинаций из трех антигипертензивных препаратов (т.е. ингибитор АПФ блокатор кальциевых каналов диуретик); наиболее часто применяется амлодипин; (3) нифедипин короткого действия практически вышел из употребления в лечении АГ, в том числе при купировании гипертензивных кризов (кроме беременных); (4) могут применяться у лиц со сниженной функцией почек; (5) среди побочных эффектов – головная боль, приливы, отеки голеней (при отеках – сочетать с ингибитором АПФ или сартаном, может быть заменить дигидропиридиновый препарат на недигидропиридиновый; диуретики неэффективны); (6) левовращающий амлодипин изучен недостаточно, в этой связи у лиц с высоким / очень высоким сердечно-сосудистым риском следует применять рацемат амлодипина; (7) при сниженной систолической функции левого желудочка безопасны амлодипин и фелодипин.
2. Недигидропиридиновые (верапамил – 120–480 мг/сут на 1–2 приема; дилтиазем – 120–360 мг/сут на 1-2 приема): (1) в лечении АГ применяются реже, чем дигидропиридиновые; (2) предпочтительны у лиц с хроническими заболеваниями почек с протеинурией (имеют более выраженную ренопротекцию, чем дигидропиридиновые), при снижении функции почек не требуют коррекции дозы; (3) применяются у лиц со склонностью к тахикардии (в том числе при ишемической болезни сердца); являются противоаритмическими препаратами 4 класса; могут назначаться для контроля частоты желудочкового ритма при фибрилляции предсердий у лиц, которые не переносят бета-адреноблокаторы; (4) не используются при сниженной систолической функции левого желудочка; (5) из побочных эффектов – брадикардия, нарушения атриоветрикулярной проводимости; (6) при резистентной АГ в качестве одного из вариантов лечебной тактики может быть применена комбинация недигидропиридинового препарата с дигидропиридиновым.
Бета-адреноблокаторы (β-АБ)
1. Например, бетаксолол – 5–20 мг, 1 р/сут; бисопролол – 5–10 мг, 1 р/сут; карведилол – по 3,125–25 мг 2 р/сут; метопролола сукцинат – 25–100 мг, 1 р/сут; метопролола тартрат – по 25–100 мг 2 р/сут; небиволол – 2,5–10 мг 1 р/сут.
2. Обладают антигипертензивной эффективностью, сравнимой с другими основными классами антигипертензивных препаратов. В настоящее время при неосложненной АГ используются реже прочих основных классов (в том чсиле у лиц пожилого возраста, а также у молодых). Поскольку β-АБ улучшают прогноз у лиц с острым коронарным синдромом, у перенесших инфаркт миокарда и у имеющих хроническую сердечную недостаточность со сниженной систолической функцией левого желудочка, они являются препаратами выбора и в лечении АГ именно у этих категорий больных.
3. β-АБ – эффективные антиангинальные лекарственные средства, они также – противоаритмические препараты II класса (находят широкое применение в лечении наджелудочковых и желудочковых аритмий).
4. β-АБ III поколения (с вазодилатирующей активностью – карведилол, небиволол) благоприятно влияют на центральное аортальное давление, как и ингибиторы АПФ, сартаны, блокаторы кальциевых каналов (эти же препараты являются предпочтительными β-АБ для кардиопротекции у лиц с сахарным диабетом вне декомпенсации и с хроническим обструктивным заболеванием легких без выраженной бронхообструкции и вне приема бронходилататоров).
5. Среди побочных эффектов: негативные эффекты на метаболизм глюкозы и липидов (меньше у представителей III поколения), брадикардия, нарушения атриовентрикулярной проводимости, снижение эректильной функции, слабость, бронхообструкция, усиление периферических сосудистых нарушений (у лиц, уже имеющих таковые).
6. Во избежание развития «синдрома отмены» резко отменять β-АБ не следует.
Прочие антигипертензивные препараты
1. Альфа-1-адреноблокаторы: (1) доксазозин – 1–16 мг 1 р/сут; празозин – 1–10 мг/сут на 2–3 приема; теразозин – 1–2 мг 1 р/сут; урапидил – 60–180 мг/сут на 2 приема; (2) в лечении АГ используются в качестве компонента комбинированной терапии; (3) находят применение в лечении резистентной АГ; (4) могут применяться в лечении АГ при сниженной функции почек, при этом не требуют коррекции дозы; (5) могут быть предпочтительным антигипертензивным препаратом у пожилых мужчин с доброкачественной аденомой предстательной железы; (6) частый побочный эффект – ортостатическая гипотензия (обязательно инструктировать больного о недопустимости быстрого вставания!); (8) урапидил часто применяется в лечении гипертензивных кризов.
2. Препараты центрального действия: (1) клонидин – 0,075–0,9 мг/сут на 2–4 приема; метилдопа – 250–2000 мг/сут на 2 приема; моксонидин – 0,2–0,6 мг 1 р/сут; (2) обычно – в качестве компонента комбинированной антигипертензивной терапии; (3) метилдопа – антигипертензивный препарат выбора при беременности; (4) моксонидин – находит применение в лечении АГ у лиц с сахарным диабетом, метаболическим синдромом, хроническими заболеваниями почек; его не следует применять при тяжелой сердечной недостаточности со сниженной систолической функцией левого желудочка (функциональных классов III-IV); (5) применение клонидина ограничивают его известные побочные эффекты, в первую очередь, сухость во рту и сонливость.
3. Прямые вазодилататоры: (1) гидралазин – 50–200 мг/сут на 2–4 приема; изосорбида динитрат – 20–120 мг/сут на 1–2 приема; (2) гидралазин сейчас применяется нечасто, может использоваться в лечении хронической АГ при беременности; (3) нитраты могут использоваться в комбинированном лечении АГ при остром коронарном синдроме, хронической ишемической болезни сердца, изолированной систолической АГ, резистентной АГ, АГ при сниженной функции почек, у пожилых; внутривенно нитраты – при гипертензивных кризах, в том числе в сочетании с кардиальной астмой, отеком легких, при беременности; (4) длительное применение нитратов может сопровождаться развитием нитратной толерантности (для ее предупреждения следует в режиме приема использовать адекватный по продолжительности нитратосвободный промежуток, возможно также сочетать нитраты с ингибиторами АПФ, карведилолом, аторвастатином).
Резистентная АГ и симптоматические АГ
Отсутствие удовлетворительного контроля АД на фоне стандартного лечения представляет собой частую и весьма актуальную проблему. При ее обсуждении сошлемся на опубликованную в 2015 г. серьезную обзорную работу Ghofrani H et al («Резистентная АГ (РАГ): медикаментозное лечение и альтернативные подходы»), основные положения которой мы сочли возможным привести в таблице 1 и на рисунке 5.
Представляет интерес выделение авторами следующих типов АГ:
- РАГ – невозможность достижения АД<140/90 мм рт.ст. на 3 антигипертензивных препаратах в максимально переносимых дозах, один из которых – диуретик ( изменения образа жизни – поваренная соль, жидкость и др.).
- Контролируемая РАГ – те пациенты с РАГ, у которых целевое АД достигнуто на ≥ 4 антигипертензивных препаратах.
- Рефрактерная АГ – невозможность достижения АД<140/90 мм рт.ст. на ≥ 4 антигипертензивных препаратах в максимально переносимых дозах.
- Псевдорезистентная АГ – лица с отсутствием целевого АД, не имеющие РАГ (например, не придерживающиеся рекомендаций по изменению образа жизни, не приверженные к медикаментозному лечению).
- АГ «белого халата» – лица с уровнем АД выше целевого при ≥ 3 визитах к врачу, но имеющие нормальное АД при ≥ 2 измерениях дома при отсутствии поражений органов-мишеней.
- Маскированная АГ – лица с нормальным АД при измерении в кабинете врача, если уровень АД повышен по данным его амбулаторного мониторирования.
Как видно из таблицы 1 и рисунка 5, распространенность неадекватного контроля АД при АГ несмотря на адекватное изменение образа жизни и прием ≥ 3 антигипертензивных препаратов – очень высока. Даже в рандомизированных контролируемых исследованиях она составляет 20–35%, а в условиях реальной клинической практики – еще выше. Обратим особое внимание врача на то, что для достижения контроля АД могут иметь большое значение (1) существенное ограничение поваренной соли в рационе больного; (2) уменьшение приема или отмена нестероидных противовоспалительных препаратов и иных указанных в таблице 1 средств, способствующих повышению АД; (3) жесткий контроль приверженности пациента к лечению; (4) учет того, что причиной до 10–30% случаев РАГ является первичный альдостеронизм (латентный), а это мотивирует более частое применение при РАГ спиронолактона (25–50 мг/сут, возможно – и более), если нет противопоказаний; (5) адекватный выбор сочетаний из 3, 4 и 5 антигипертензивных препаратов (см. табл.1).

Рисунок 5. Основные подходы при резистентной АГ
Примечание: * – чаще на начальном этапе используется комбинация из сартана или ингибитора АПФ блокатор кальциевых каналов диуретик.
Таблица 1. Резистентная АГ (РАГ): определение и лечебная тактика
|
Неадекватный контроль АД – основная причина >60% случаев цереброваскулярных катастроф и почти 50% случаев острого коронарного синдрома, а также большинства случаев прогрессии хронических заболеваний почек (ХЗП). Даже в условиях рандомизированных контролируемых исследований до 20-35% больных с АГ не достигают целевого контроля уровней АД несмотря на прием ≥ 3 антигипертензивных препаратов |
|
Частые особенности больных с плохо контролируемой АГ включают: пожилой возраст, ожирение, курение, избыточное употребление соли, наличие ХЗП, сахарного диабета, женский пол, избыточное употребление алкоголя. Резистентности АГ способствует прием препаратов: нестероидных противо-воспалительных, симпатомиметиков, глюкокортикоидов, эритропоэтина и др. |
|
Важнейшей причиной плохого контроля уровней АД является низкая приверженность больных к лечению (ее частота при АГ достигает 50–60%). Ведущими причинами считают: низкий уровень информированности больного (информировать, разъяснять, убеждать!), нигилизм и инертность врача, сложный режим дозирования, высокую стоимость, побочные эффекты |
|
Частой причиной РАГ являются симптоматические АГ (их суммарная частота составляет до 10% всех случаев АГ). Наиболее частые причины РАГ среди симптоматических АГ – первичный альдостеронизм (10–30% всех случаев РАГ), ХЗП, реноваскулярные АГ, гипер / гипотиреоз, синдром обструктивного апноэ во сне, синдром Кушинга, феохромоцитома, коарктация аорты |
|
РАГ нередко связана с использованием неадекватных комбинаций и субоптимального дозирования антигипертензивных препаратов. Обычно большинство больных с РАГ должны получать комбинацию ингибитора АПФ или сартана с блокатором кальциевых каналов и диуретиком, желательно в «полных» дозах, в адекватное время. Чаще следует использовать фиксированные комбинации (это явно повышает приверженность!) |
|
4-м препаратомк вышеперечисленным при скорости клубочковой фильтрации (СКФ) < 60 мл/мин обычно являетсяпетлевой диуретик (фуросемид – на 2-3 приема/сут или торасемид – на 1-2 приема/сут). При СКФ > 30–50 мл/мин 4-м препаратом чаще является АМР (спиронолактон), особенно при ожирении и синдроме обструктивного апноэ во сне. Вместо АМР также возможны не-АМР калийсберегающие диуретики: амилорид или триамтерен |
|
В качестве 5-го препарата можно выбирать: бета-адреноблокатор, препарат центрального действия, альфа-адреноблокатор, нитрат |
|
Среди немедикаментозных подходов: · Стимуляция каротидных барорецепторов каротидного синуса устройством, имплантируемым под кожу (повышение парасимпатического тонуса, вазодилатация, натрийурез, снижение ЧСС и АД). В исследованиях систолическое АД (САД) снижается на 26–30 мм рт.ст. (нужны дополнительные данные) · Катетерная радиочастотная аблация симпатических нервных ганглиев в стенке почечных артерий с 2 сторон. В исследованиях (в т.ч. Symplicity HTN-3) – противоречивые данные (снижение САД на 22-32 или плацебо-подобное) |
Примечание: АМР – антагонист минералокортикоидных рецепторов.
При обсуждении вопросов РАГ мы уже упоминали о том, что одной из частых причин резистентности АГ к лечению являются симптоматические АГ, перечень наиболее частых причин которых приводился выше. Обсуждение вопросов диагностики и лечебной тактики при симптоматических АГ часто оказывается за рамками обсуждаемых в учебных семинарах вопросов. С учетом этого, мы сочли возможным здесь хотя бы кратко представить данные по некоторым вариантам симптоматической АГ. Далее нами рассматриваются почечные и почечно-сосудистые варианты симптоматических АГ; также мы обсуждаем «надпочечниковые» причины АГ (первичный альдостеронизм, синдром Кушинга и феохромоцитома). Разумеется, материал здесь, в силу необходимости, представлен весьма сжато; для более полного знакомства с проблемой заинтересованному читателю следует обратиться к соответствующим источникам (например, Дядык А.И., Багрий А.Э. Артериальные гипертензии в современной клинической практике. – Киев, 2014. 206 с.).
АГ при хронических заболеваниях почек (ХЗП)
Термин ХЗП является в настоящее время общепринятым. Под ХЗП понимают нарушение структуры и/или функции почек, присутствующее в течение >3 месяцев (табл. 2). ХЗП – это собирательное понятие, объединяющее гетерогенные заболевания, которые (1) нарушают структуру и/или функцию почек; (2) имеют различные клинические особенности; (3) неоднородны по этиологии, степени тяжести и темпу прогрессирования. На ранних этапах становления и развития ХЗП часто протекают бессимптомно; их диагностика при этом обычно происходит в ходе скрининговых или случайных исследований, а также при обследовании по поводу сопутствующих заболеваний. При быстропрогрессирующем характере течения некоторых вариантов ХЗП развитие значимого снижения функции почек возможно уже в течение нескольких недель–месяцев, однако во многих случаях темп прогрессирования значительно меньше (годы–десятилетия). На рисунке 6 и в таблице 2 представлены некоторые наиболее существенные для врача-интерниста подходы к диагностике и лечению ХЗП. Особенно отметим крайнюю важность для диагностики ХЗП регулярной оценки уровней креатинина крови с подсчетом скорости клубочковой фильтрации.

Рисунок 6. Общий взгляд на тактику врача при АГ у лиц с ХЗП
Примечание: СКФ – скорость клубочковой фильтрации; ТД – тиазидный диуретик; БКК – блокатор кальциевых каналов; * – ОПП – острое поражение почек (этот термин сейчас широко применяют вместо устаревшего – ОПН, т.е. острой почечной недостаточности).
Таблица 2. АГ при ХЗП – вопросы диагностики и лечения
|
Под ХЗП понимают присутствующие в течение > 3 месяцев (1) протеину-рию >150 мг/сут и/ или (2) изменения осадка мочи (гематурия, эритроцитарные / зернистые / лейкоцитарные цилиндры) и/или (3) СКФ<60 мл/мин; (4) также к ХЗП относят наличие структурных нарушений, выявленных при инструментальном исследовании (поликистоз, дисплазия, гидронефроз и др) |
|
Основные категории ХЗП: (1) гломерулярные заболевания (гломерулонефриты, диабетическая нефропатия и др.); (2) тубуло-интерстициальные (инфекции мочевой системы, в т.ч. с обструкцией и др.); (3) сосудистые (при АГ, атеросклерозе и др.); (4) кистозные и врожденные (поликистоз, дисплазии и др.) |
|
Всем больным с АГ необходимо оценивать уровни креатинина сыворотки крови и подсчитывать скорость клубочковой фильтрации (СКФ):
Классификация ХЗП по уровню СКФ (мл/мин): 1 стадия – СКФ >90; 2 стадия – 60–89; 3 стадия – 30–59; 4 стадия – 15–29; 5 стадия – <15 |
|
Распространенность АГ при хроническом гломерулонефрите – 35–80%, при диабетической нефропатии – 70–100%, хроническом пиелонефрите – 50–75%, поликистозе почек – 50–60%. Развитие АГ нередко – на этапе снижения функции почек. АГ ассоциирована с увеличением темпа прогрессии почечных поражений, а также увеличением риска сердечно-сосудистых осложнений |
|
Лечение АГ при ХЗП: (1) целевые уровни АД – обычно 130–139 / 80–89 мм рт.ст., ближе к нижней из этих границ, а при протеинурии > 0,15 г/сут – ≤ 130 / 80 мм рт.ст.; (2) среди антигипертензивных препаратах во многих случаях предпочтение отдают ингибиторам АПФ либо сартанам (с учетом уровней СКФ); (3) к ним нередко добавляют блокаторы кальциевых каналов, тиазидные / тиазидоподобные диуретики, возможно – иные классы препаратов; (4) при СКФ <50 мл/мин неотъемлемым компонентом лечебной тактики являются петлевые диуретики; (5) многим пациентам требуется назначение 4-, 5-компонентной антигипертензивной терапии; (6) чаще следует использовать фиксированные комбинации лекарственных средств |
|
Иные кардио / ренопротекторные лечебные подходы при ХЗП: (1) сейчас при ХЗП широко применяют статины (снижают как степень сердечно-сосудистого риска, так и темп прогрессии ХЗП); (2) коррекция анемии (препараты эритропоэтина, железа); (3) коррекция гипергликемии (целевой уровень гликозилированного гемоглобина – обычно <7,0 ммоль/л); (4) коррекция фосфорно-кальциевого баланса; (5) отказ от курения; (6) сведение к минимуму влияния нефротоксичных факторов (в т.ч. приема нестероидных противовоспалительных препаратов) |
Реноваскулярные АГ
Подходы к диагностике и лечению реноваскулярных АГ представлены на рисунке 7 и в таблице 3. При их обсуждении сначала укажем, что предполагать наличие реноваскулярной АГ следует преимущественно у лиц, имеющих необычные варианты течения АГ (начало ее в молодом возрасте, начало тяжелой АГ в пожилом возрасте, резкое утяжеление характера ранее стабильной АГ и т.д.). При обследовании нужно обращать внимание на выслушивание проекций почечных артерий, наличие тяжелой гипертензивной ретинопатии, снижение функции почек, возможно – наличие умеренной протеинурии, разницы в размерах почек >1,5 см при ультрасонографии, кортикальной атрофии при КТ-ангиографии. В основе лечения лиц с фибромышечной дисплазией и АГ лежит эффективная антигипертензивная терапия (следует соблюдать особую осторожность при использовании ингибиторов АПФ / сартанов); в части случаев выполняется баллонная ангиопластика. При атеросклеротическом поражении почечных артерий – антигипертензивная терапия; статины в высоких дозах; контроль факторов сердечно-сосудистого риска. Реваскуляризация при атеросклеротических поражениях почечных артерий резервируется лишь для отдельных, наиболее тяжелых, категорий таких больных.

Рисунок 7. Общий взгляд на тактику врача при реноваскулярной АГ
Примечание: ДАД – диастолическое АД; РАГ – резистентная АГ; ФМД – фибромышечная дисплазия; ПА – почечная артерия; АСК – ацетилсалициловая кислота.
Таблица 3. Реноваскулярные АГ – вопросы диагностики и лечения
|
Реноваскулярные АГ (АГ у лиц со стенозирующими процессами в почечных артериях – ПА) составляет около 1% среди всех случаев АГ; среди лиц с диастолическим АД ≥ 125 мм рт.ст. – до 30% имеют реноваскулярные АГ |
|
Наиболее частые причины: (1) фибромышечная дисплазия (ФМД) ПА; (2) атеросклеротическое поражение ПА |
|
ФМД: (1) патологическое состояние неизвестной этиологии с фиброзированием и/или избыточной пролиферацией клеток артериальной стенки; (2) наиболее часто вовлечены ПА (у 75%), но также – сонные, позвоночные и др.; (3) клиническая картина вариабельна и зависит от локализации поражения (ПА – АГ, шум над проекцией этих артерий; сонные и позвоночные – головная боль, ишемические инсульты, шумы над проекцией соответствующих артерий; мезентериальные – абдоминальная боль после еды, похудание и др.); (3) средний возраст установления диагноза (США) – 50 лет, но часто – у молодых; (4) стеноз чаще – в средних и дистальных отделах ПА |
|
Атеросклероз: (1) составляет до 90% всех случаев стенозирования ПА; (2) выявляется у 30% лиц, которым проводится катетеризация сердца; (3) типично поражение проксимальной трети ПА и прилегающих участков брюшной аорты; (4) наряду с АГ часто имеется снижение функции почек |
|
Обследование для выявления возможного стенозирования ПА показано, в первую очередь больным с: (1) началом АГ в возрасте до 30 лет; (2) началом тяжелой АГ (>160 / >110 мм рт. ст.) в возрасте > 55 лет; (3) внезапным и устойчивым ухудшением ранее достаточно хорошо контролировавшейся АГ; (4) РАГ; (5) ухудшением функции почек на фоне применения ингибитора АПФ или сартана; (6) наличием уменьшения размера почки (атрофия), а также с различиями в размере почек, превышающими 1,5 см; (7) эпизодом внезапно развившегося необъяснимого отека легких (особенно у больного со сниженной функцией почек) |
|
Методы обследования: (1) дуплексная ультрасонография ПА; (2) КТ-ангиография; (3) МРТ-ангиография; (4) катетерная ангиография |
|
Лечение при ФМД: (1) бессимптомное течение и отсутствие АГ – только инструментальный контроль, без лечения; (2) при АГ – ингибитор АПФ или сартан (осторожно (!) при билатеральном поражении ПА, унилатеральном поражении высокой степени, скорости клубочковой фильтрации <30 мл/мин) блокатор кальциевых каналов диуретик; (3) при отсутствии эффекта – чрескожная баллонная ангиопластика (обычно без стентирования); (4) при достижении контроля АД – ацетилсалициловая кислота 75–100 мг/сут |
|
Лечение при атеросклерозе ПА: (1) настойчивая анти-АГ терапия (те же классы и предосторожности, что и для ФМД); (2) высокие дозы мощных статинов (целевой уровень липопротеидов низкой плотности <1,8 ммоль/л); (3) прекращение курения; (4) тщательный контроль гликемии; (5) ацетилсалициловая кислота 75–100 мг/сут (при достижении контроля АД); (6) реваскуляризация ПА (стент) – только для лиц с рецидивирующей и необъяснимой иными причинами острого отека легких, рецидивирующей нестабильной стенокардией, прогрессирующим снижением функции почек |
Надпочечниковые АГ. «Инциденталома» надпочечника
В начале нашего обсуждения «надпочечниковых» АГ отметим важность дифференциальной диагностики так называемой «инциденталомы» (т.е. случайно выявленного при компьютерно-томографическом (КТ) или магнитно-резонансно-томографическом (МРТ) исследовании); частота такого выявления при КТ / МРТ достигает 5–8% всех случаев этих исследований. В 85–90% такие «инциденталомы» представляют собой доброкачественные и гормонально-неактивные образования. Однако в 10–15% эти образования гормонально активны и/или малигнантны, что требует проведения соответствующих дифференциально-диагностических мероприятий (рис. 8, табл. 4).

Рисунок 8. Общий взгляд на тактику врача при «инциденталоме» надпочечника
Примечание: * – см в таблицах 5–7.
Таблица 4. «Инциденталома» надпочечника (от англ. incidental – cлучайный) – вопросы диагностики и лечения
|
Инциденталома – образование надпочечника, обычно имеющее размер ≥1 см, выявленное случайно в ходе КТ или МРТ, выполненных по не-надпочечниковым показаниям. До 10–15% случаев инциденталом оказываются злокачественными и/или гормонально активными образованиями |
|
Требуется исключить злокачественный характер выявленного образования. Значение имеют определяемые при КТ / МРТ размеры (при злокачественной природе – чаще > 4 см); форма (чаще – неправильная); структура (чаще – негомогенная); плотность (чаще – высокая); темп роста (чаще – быстрый); наличие метастазирования) |
|
Необходимо установление гормональной активности образования надпочечника. Среди 3868 случаев инциденталом: субклинический синдром Кушинга – 8%; феохромоцитома – 5%; первичный альдостеронизм – 1%.
|
|
При подозрении на гормональную активность образования проводят подтверждающие тесты. Если она подтверждена, а также если не исключена злокачественная природа образования – хирургическое вмешательство. Если нет – КТ / МРТ в динамике (1 раз в 6 месяцев), контроль гормональной активности (1 раз в год – первые 4 года) |
Первичный альдостеронизм
На рисунке 9 и в таблице 5 представлены основные подходы к диагностике и лечению первичного альдостеронизма (ПА). Практикующему врачу следует помнить, что это – одна из ведущих причин симптоматических АГ, частая основа для развития резистентной / рефрактерной АГ. Наиболее доступным методом исследования, позволяющим заподозрить ПА, является оценка уровней электролитов сыворотки крови. Скрининговые тесты (табл. 5) следует проводить лицам с АД > 160 / 100, а особенно – с АД > 180 / 110 мм рт.ст., при РАГ, при гипокалиемии, при «инциденталоме» надпочечника. Важно иметь в виду, что гипокалиемия часто имеет место при ПА, однако у некоторых пациентов ее может не быть. При положительных результатах скрининговых и верифицирующих лабораторных тестов необходимо уточнение особенностей поражения надпочечников (аденома – чаще односторонняя или билатеральная гиперплазия). Медикаментозный контроль АД обычно осуществляется с использованием антагонистов минералокортикоидных рецепторов – спиронолактона или эплеренона, нередко в сочетании с тиазидным диуретиком, возможно – с блокаторами кальциевых каналов (последние обладают умеренной антиальдостероновой активностью).

Рисунок 9. Общий взгляд: первичный альдостеронизм (ПА)
Примечание: * – см. табл. 5; ** – АМР – антагонисты минералокортикоидных рецепторов – селективный – эплеренон (лучше, т.к. ниже риск побочных эффектов) или неселективный спиронолактон; ТД – тиазидные диуретики; БКК – блокаторы кальциевых каналов (например, амлодипин, имеет умеренные свойства АМР)
Таблица 5. Первичный альдостеронизм (ПА) – вопросы диагностики и лечения
|
ПА (синдром Конна) – синдром, обусловленный автономной (независимой от ренин-ангиотензиновой системы – РАС) гиперсекрецией альдостерона в корковом веществе надпочечников |
|
Наиболее частые причины ПА: (1) альдостерон-продуцирующая аденома надпочечника; (2) билатеральная гиперплазия надпочечников. Реже – унилатеральная гиперплазия, карцинома, семейный гиперальдостеронизм |
|
Большинство случаев альдостеронизма (повышение уровней альдостерона в крови) вторичны по отношению к гиперактивности РАС (при стенозе почечной артерии и др.). Для диагностики – определение активности ренина плазмы (при ПА – снижена, при вторичном альдостеронизме – повышена) |
|
АГ имеется практически у всех больных с ПА |
|
ПА сейчас рассматривается как одна из самых частых (если не самая частая) среди причин развития симптоматических АГ. Доля лиц с ПА среди лиц с АГ в целом может составлять 3–10%, с АГ 3 степени – до 40%. Возраст – любой (типично – 30–50 лет), более часто у женщин |
|
Классические клинические проявления ПА: АГ (часто РАГ), гипокалиемия (не всегда!), чрезмерное выведение калия почками, гипернатриемия, метаболический алкалоз. Всем лицам с АГ – исследовать электролиты крови! |
|
Скрининговые тесты: (1) лицам с АД > 180 / 110, с РАГ, с гипокалиемией, с «инциденталомой» надпочечника – оценка экскреции калия и натрия с мочой (за 24 ч, перед этим – не менее 3 дней без любых диуретиков); (2) оценка альдостерон-ренинового соотношения (после коррекции гипокалиемии не менее 4-6 недель без калийсберегающих диуретиков) |
|
Верифицирующие тесты (при повышенных уровнях альдостерон-ренинового соотношения): (1) с физраствором (оценка уровней альдостерона плазмы до и после 4-часовой инфузии 2 л физраствора – при ПА нет снижения альдостерона); (2) с каптоприлом (оценка альдостерона до и после приема внутрь каптоприла 1 мг/кг м тела – при ПА нет снижения альдостерона) |
|
Оценка типа поражения надпочечника (КТ более информативна, чем МРТ): (1) аденома (чаще односторонняя) – 40% случаев ПА; (2) билатеральная гиперплазия – 60% случаев ПА |
|
Хирургическое лечение (чаще – лапароскопия) – при аденоме надпочечника (на фоне 3–5 недельного лечения спиронолактоном) |
|
Медикаментозное лечение (при билатеральной гиперплазии, невозможности хирургического лечения, сохранении АГ после операции): (1) спиронолактон или эплеренон (сначала 50–100 мг/сут, затем 25–50 мг/сут); (2) при их непереносимости – амилорид; (3) часто гидрохлоротиазид; (4) нередко амлодипин; (5) при необходимости – другие классы анти-АГ препаратов |
Синдром Кушинга (Иценко-Кушинга, гиперкортицизм)
На рисунке 10 и в таблице 6 представлены подходы к диагностике и лечению при втором из вариантов «надпочечниковых» симптоматических АГ, которые нами здесь рассматриваются, а именно – при синдроме / болезни Кушинга. Как видно из рисунка и таблицы, настороженности в отношении наличия этого синдрома требуют лица, у которых АГ (нередко носящая характер РАГ) сочетается с абдоминальным ожирением, сахарным диабетом, слабостью и кожными широкими пурпурными стриями. Эта клиническая картина достаточно известна клиницисту. Здесь следует иметь в виду, что такие признаки гиперкортицизма могут быть вторичными по отношению к приему глюкокортикоидов (ятрогенный синдром Кушинга), либо являться проявлениями «псевдосиндрома Кушинга» – см. табл. 6.
Подобным пациентам может потребоваться выполнение соответствующих скрининговых и верифицирующих методов исследования. Следует иметь в виду возможность локализации опухолевого процесса в гипофизе (АКТГ-продуцирующая аденома), надпочечниках, а также в иных органах. Контроль АГ осуществляется с использованием любых классов антигипертензивных препаратов, приоритет отдается диуретикам и антагонистам минералокортикоидных рецепторов. При выявлении опухоли обычно рекомендуют оперативное лечение.

Рисунок 10. Общий взгляд на тактику врача при синдроме Кушинга
Примечание: * -АМР – антагонист минералокортикоидных рецепторов (спиронолактон или эплеренон.
Таблица 6. Синдром Кушинга – вопросы диагностики и лечения
|
Синдром Кушинга – комплекс проявлений, связанных с длительной экспозицией чрезмерно высоких концентраций гормона кортизола (гидрокортизона – глюкокортикоида, продуцируемого корой надпочечников). Он может быть связан с: (1) опухолью коры надпочечников (добро- или злокачественной); (2) аденомой гипофиза (гиперпродукция адренокортикотропного гормона – АКТГ); (3) т.н. кортикотропиномами – опухолями, продуцирующими кортикотропин-релизинг гормон (могут локализоваться в гипоталамусе, бронхах, яичках, яичниках); (4) приемом глюкокортикоидов (ятрогения, самая частая причина синдрома Кушинга) |
|
Болезнь Кушинга : ситуация с избыточной продукцией АКТГ, что стимулирует гиперпродукцию кортизола в надпочечниках |
|
Среди неятрогенных причин синдрома Кушинга: опухоли гипофиза – 70%, эктопическая гиперсекреция АКТГ – 10%, эктопическая гиперпродукция кортикотропин-релизинг гормона – 1%, аденома надпочечника – 10%, карцинома надпочечника – 7%, гиперплазия надпочечника – 2% |
|
Выделяют также «псевдосиндром Кушинга», когда нарушений гипоталамо-гипофизарно-надпочечниковой оси нет, но повышен кортизол и есть кушингоид (при ожирении, алкоголизме, беременности). Дифференциальная диагностика с истинным синдромом Кушинга может быть затруднена |
|
АГ имеется у 75–90% больных с синдромом / болезнью Кушинга; часто РАГ |
|
Клинические проявления (наиболее характерные): абдоминальное ожирение, АГ, широкие пурпурные стрии, угревая сыпь, нарушения памяти и внимания, дисменорея, снижение потенции / либидо, слабость вследствие миопатии, сахарный диабет |
|
Скрининг: (1) оценка уровней кортизола в сыворотке крови или слюне (забор образцов – лучше поздно ночью, с учетом суточного ритма секреции гормона); уровень > 8,6 ммоль/л – повышен; (2) при высокой вероятности синдрома Кушинга – оценка свободного кортизола в суточной моче (норма – до 1,4 ммоль/л; диагностический уровень – в 4 раза выше); (3) при невысокой вероятности синдрома Кушинга (например, у лиц с диабетом, ожирением, РАГ) – низкодозовый тест с дексаметазоном (1 мг внутрь перед сном; утром – забор крови (диагностический – > 48,6 ммоль/л); (4) осмотр окулиста, оценка полей зрения (гемианопсия при сдавлении chiasma opticum при аденоме гипофиза?) |
|
Верификация причины: (1) оценка АКТГ в плазме; (2) КТ / МРТ надпочечников; (3) МРТ гипофиза |
|
Лечение: · Контроль АГ: (1) можно использовать все классы антигипертензивных препаратов; (2) т.к. важна перегрузка объемом в развитии АГ при гиперкортицизме, препараты выбора – диуретики спиронолактон / эплеренон
· Если кортизол-продуцирующая опухоль надпочечника (доброкачественная или злокачественная – хирургическое удаление) · После операции – контроль кортизола, тщательное и длительное наблюдение (нередки рецидивы в течение ближайших 5 лет после операции) |
Феохромоцитома
Основные принципы диагностики и лечения пациентов с феохромоцитомой представлены на рисунке 11 и в таблице 7. Комментируя их, нужно отметить, что феохромоцитома в структуре симптоматических АГ является нечастым состоянием. В силу этого, скрининг (в первую очередь, биохимический, эталоном которого в настоящее время признано определение уровней метанефринов в плазме / моче) следует проводить не большим группам пациентов с АГ, но лишь отдельным пациентам, имеющим указанные на рисунке 11 и в таблице 7 особенности. Важно подчеркнуть, что относительно хорошо известные врачу из литературы гиперадренергические пароксизмы доминируют в клинической картине лишь у небольшой части больных; чаще же симптоматика значительно менее типична и представлена стабильной АГ с эпизодами гипертензивных кризов. Лечебная тактика у лиц с установленной при МРТ / КТ локализацией катехоламин-секретирующей опухоли обычно предусматривает ее удаление в условиях эффективной α- и β-адреноблокады. При неоперабельности опухоли возможно длительное лечение α-АБ, к которым добавляют β-АБ, возможно также – блокаторы кальциевых каналов, а при необходимости – и иные классы антигипертензивных препаратов.

Рисунок 11. Общий взгляд на тактику врача при феохромоцитоме
Таблица 7. Феохромоцитома – вопросы диагностики и лечения
|
Феохромоцитома – катехоламинсекретирующая опухоль, происходящая из хромаффинных клеток надпочечников. Параганглиома – вненадпочечниковая опухоль из клеток симпатических или парасимпатических ганглиев |
|
Среди лиц с АГ феохромоцитома – у 0,2% |
|
Классический вариант клинической картины – гиперадренергические пароксизмы (гипертензивный криз интенсивная головная боль интенсивное диффузное потоотделение сердцебиение побледнение /покраснение лица). Эти эпизоды могут провоцироваться механическим воздействием на опухоль, приемом ряда препаратов (β-адреноблокаторов, анестетиков и др.) |
|
Иные частые проявления:сердцебиение, тревога, нервозность, дрожь, гипергликемия натощак, слабость, тахипноэ. У большинства больных имеется стабильная АГ с эпизодами гипертензивных кризов |
|
Правило 10%: среди всех феохромоцитом ≈ 10% – вненадпочечниковые (т.е. параганглиомы); 10% имеют место у детей; 10% – двусторонние 10% – рецидивируют; 10% – злокачественные; 10% – обнаруживают случайно, 10% – семейные. В США сейчас до 50% – обнаруживают случайно |
|
Скрининг для выявления феохромоцитомы показан не всем с АГ, но лишь лицам с гиперадренергическими кризами, с РАГ, с повышением АД в ответ на анестезию, с началом АГ в возрасте до 20 лет, с АГ в сочетании с дилатационной кардиомиопатией, с инциденталомой надпочечника |
|
Биохимическая диагностика: (1) безусловный стандарт – оценка уровней метанефринов в плазме и/или моме (например, нормы свободного норметанефрина плазмы <0,9 нмоль/л; свободного метанефрина плазмы < 0,5 нмоль/л; повышение в ≥ 4 раза – 100% диагностика катехоламин-продуцирующей опухоли); (2) значительно менее чувствительна оценка катехоламинов плазмы / мочи; ванилилминдальную кислоту уже не используют |
|
Установление локализации опухоли: (1) МРТ (лучше) или КТ живота и таза (80% опухолей – в надпочечниках, 98% – в структурах живота и таза); (2) I131-MIBG (метилиодбензилгуанидин) – сканирование |
|
При выявлении опухоли – хирургическое удаление. Большинство феохромоцитом доброкачественные и могут быть удалены радикально. Обязательна периоперационная эффективная α- и β-адреноблокада (α-АБ и β-АБ). После вмешательства – ежегодный контроль метанефринов крови / мочи; при необходимости – МРТ / КТ |
|
При неоперируемых опухолях: (1) α-АБ (доксазозин, празозин, теразозин); (2) через 4–7 дней можно β-АБ (нельзя без предварительной α-АБ!) – дозу с малой постепенно титровать; целевая ЧСС сидя – 60–70 /мин; стоя – 70–80 /мин; (3) возможно блокатор кальциевых каналов; (4) возможно ингибитор синтеза катехоламинов (метирозин) |
ВОЗМОЖНОСТИ ПРИМЕНЕНИЯ ПРЕПАРАТОВ С МЕТАБОЛИЧЕСКИМ ДЕЙСТВИЕМ (Мельдоний) В ЛЕЧЕНИИ ПАЦИЕНТОВ С АГ
Современные Рекомендации не включают препараты с метаболическим действием в число стандартных лечебных подходов при АГ. Тем не менее, возможности для их рационального использования у достаточно широких контингентов больных АГ имеются. В ранее опубликованных нами семинарах по лечению ишемической болезни сердца (ИБС) и хронической сердечной недостаточности (ХСН) уже подробно обсуждались механизм действия и позитивные эффекты Мельдония при этих состояниях. С учетом представленных там данных, использование Мельдония у лиц с ИБС (включая как острый коронарный синдром, так и хронические формы ИБС) и с ХСН с систолической дисфункцией ЛЖ выглядит вполне оправданным (включая, разумеется, и тех из них, кто имеет АГ).
Далее рассмотрим возможности использования Мельдония у лиц с АГ без сопутствующих ИБС / ХСН. Мельдоний характеризуется исследователями как препарат с представительным органопротекторным потенциалом (антигипоксант, ангиопротектор, миокардиальный цитопротектор). При его использовании улучшается функция эндотелия сосудов, снижаются оксидативный стресс и инсулинорезистентность, улучшается функция тромбоцитов.
Интерес к применению метаболических препаратов (в частности, Мельдония) в комплексном лечении больных с АГ базируется на следующих соображениях (Дзерве В.Я., Калвиньш И.Я.; Михина В.П. и соавт.; Стаценко М.Е. и соавт.; Хайшева Л.А. и соавт.; Хлебодаровой Ф.Е. и соавт. и др.): (1) благоприятные эффекты Мельдония на функцию эндотелиальных (и, возможно, гладкомышечных) клеток сосудистой стенки могут способствовать повышению эффективности традиционных антигипертензивных препаратов, улучшению таким образом контроля АД; (2) комплекс присущих Мельдонию цитопротекторных действий (ангиопротекция, миокардиальная цитопротекция) может ослабить негативные эффекты АГ на эти органы-мишени и, тем самым, снизить имеющийся у больного уровень сердечно-сосудистого риска.
На рисунке 12 представлены возможности использования Мельдония у больных с АГ по данным ряда работ отечественных специалистов. Как видно из рисунка, авторами действительно отмечен комплекс ценных при АГ эффектов на сосудистую стенку и миокард (улучшение функции эндотелия, регрессия гипертрофии миокарда, улучшение диастолического наполнения левого желудочка и др.); здесь следует отметить, что эти эффекты были отмечены при добавлении препарата к стандартно применяемым антигипертензивным лекарственным средствам. Важным является выявленное дополнительное снижение уровней АД и улучшение его суточного профиля, что в ряде случаев позволяло уменьшить дозу антигипертензивных препаратов и, тем самым, снизить риск развития их дозозависимых побочных эффектов. Следует отметить, что позитивные эффекты Мельдония могут быть особенно значимы для лиц с сахарным диабетом и метаболическим синдромом (вследствие уменьшения инсулинорезистентности), а также у пожилых (улучшение когнитивной функции). При обсуждении вопросов тактики назначения препарата при АГ отметим, что в рассматриваемых работах его использовали в дозе 500–750 мг/сут на протяжении 2–3 месяцев, однако Дзерве В.Я., Калвиньш И.Я. полагают, что в полной мере позитивные эффекты Милдроната при АГ могли бы реализоваться при его применении в более высокой дозе (например, 1000 мг/сут – несколько месяцев). Мы полагаем, что в составе комплексной терапии Мельдоний мог бы оказаться полезным и при иных вариантах АГ, например, при рассмотренных нами в рамках этого семинара РАГ и АГ при ХЗП.

Рисунок 12. Возможности применения Милдроната в комплексном лечении больных с АГ
Примечания: стрелка вниз – снижение; стрелка вверх – увеличение; ПОЛ – перекисное окисление липидов; СД – сахарный диабет; МС – метаболический синдром; анти-АГ – антигипертензивный; ЛЖ – левый желудочек
Завершая обсуждение вопросов современной лечебной тактики при АГ, подчеркнем, что многие из них достаточно подробно регламентированы действующими сейчас отечественными и зарубежными рекомендациями; знание их и следование им – серьезная задача для практикующего врача. Обязательным компонентом лечения является реализация рекомендаций по изменению образа жизни. Следует нацелить больного на определенные целевые уровни АД. Чаще необходимо применять комбинированную антигипертензивную терапию, в том числе фиксированные комбинации. Лицам с резистентной АГ и симптоматическими АГ необходимо проведение соответствующих диагностических и лечебных мероприятий. Ряду больных с АГ может быть полезно применение в составе комплексной терапии препарата с метаболическим эффектом – Мельдония, который может обеспечить им дополнительную ангио- и кардиопротекцию.







