Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "Роль устройства Респимат в лечении ХОБЛ и бронхиальной астмы"
Автор: Козлова И.Ю.
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Пульмонология, Семейная медицина/Терапия
Просмотров: 2 920
Дата проведения: с 22.06.2015 по 22.06.2016
 Хроническая обструктивная болезнь легких (ХОБЛ) – обычно предотвратимое и курабельное заболевание, которое можно предупредить и лечить, характеризующееся персистирующим ограничением скорости воздушного потока, которое обычно прогрессирует и связано с выраженным хроническим воспалительным ответом легких на действие патогенных частиц или газов. На общую тяжесть ХОБЛ оказывают влияние обострения и сопутствующие заболевания (GOLD 2014).
Хроническая обструктивная болезнь легких (ХОБЛ) – обычно предотвратимое и курабельное заболевание, которое можно предупредить и лечить, характеризующееся персистирующим ограничением скорости воздушного потока, которое обычно прогрессирует и связано с выраженным хроническим воспалительным ответом легких на действие патогенных частиц или газов. На общую тяжесть ХОБЛ оказывают влияние обострения и сопутствующие заболевания (GOLD 2014).
Смертность от ХОБЛ постоянно растет. Согласно данным ВОЗ, в 2012 г. в общемировой статистике смертность от ХОБЛ заняла 3-4-е место наряду с респираторными инфекциями, уступая только ишемической болезни сердца и инсульту. Ежегодно от ХОБЛ в мире умирает около 2,75 млн человек
В последние годы изменены подходы к классификации ХОБЛ, определены возможности выделения групп пациентов с высокими рисками летальности, пересмотрены и дополнены схемы базисной терапии, направленной на снижение риска обострений и смертности пациентов.
Выживаемость больных ХОБЛ напрямую зависит от частоты обострений. Чем больше обострений переносит пациент с ХОБЛ, тем хуже прогноз. Достаточно высок уровень летальности вследствие дыхательной недостаточности, развивающейся в период тяжелых обострений заболевания. Тяжелым последствием для больных ХОБЛ является снижение функциональных показателей за один год. Так, даже после одного обострения объем форсированного выдоха за первую секунду (ОФВ1) уменьшается почти в два раза.
Внесение дополнений в классификацию ХОБЛ наряду с выделением групп (A, B, C, D) предусматривает существование таких фенотипов ХОБЛ, как «с частыми обострениями и эмфиземой», «с частыми обострениями и хроническим бронхитом», без обострений и фенотип сочетанного течения ХОБЛ и бронхиальной астмы (ACOS) (на основании GOLD 2014).
В современных условиях целью оптимальной терапии ХОБЛ является улучшение контроля и снижение будущих рисков, особенно в плане предотвращения последующих обострений.
 Мировые и казахстанские клинические рекомендации по диагностике и лечению ХОБЛ основаны на данных программы GOLD. Большим преимуществом классификации ABCD стало расширение возможностей применения различных групп препаратов при разных типах ХОБЛ. Бронхолитики длительного действия теперь рекомендованы при всех стадиях ХОБЛ. При выборе базисной терапии пациенты всех групп (A, B, C, D) получают бета-2-агонисты короткого действия (КДБА), бета-2-агонисты длительного действия (ДДБА), комбинации с ингаляционными глюкокортикостероидами (иГКС), тройные комбинации. Возможно сочетание ДДБА и короткодействующего антихолинергического препарата (таблица 1).
Мировые и казахстанские клинические рекомендации по диагностике и лечению ХОБЛ основаны на данных программы GOLD. Большим преимуществом классификации ABCD стало расширение возможностей применения различных групп препаратов при разных типах ХОБЛ. Бронхолитики длительного действия теперь рекомендованы при всех стадиях ХОБЛ. При выборе базисной терапии пациенты всех групп (A, B, C, D) получают бета-2-агонисты короткого действия (КДБА), бета-2-агонисты длительного действия (ДДБА), комбинации с ингаляционными глюкокортикостероидами (иГКС), тройные комбинации. Возможно сочетание ДДБА и короткодействующего антихолинергического препарата (таблица 1).
Перечень препаратов, применяемых при ХОБЛ, расширяется. За последние 40 лет лечение бронхообструктивной патологии претерпело изменения от системной терапии адреналином, атропином, эуфиллином, преднизолоном до высокодисперсных селективных ингаляционных препаратов. Теофиллин сохраняет свое значение как препарат третьей линии лишь при недостаточной эффективности лекарств других групп. Более 30 лет в практической медицине сохраняет устойчивую позицию фиксированная комбинация бронхолитиков короткого действия – фенотерола и ипратропия бромида, как в виде дозирующего аэрозоля, так и виде раствора для ингаляций.
Последнее десятилетие комбинации ИГКС и ДДБА (будесонид/формотерол, флутиказон/сальметерол) занимают прочное положение при тяжелом и крайне тяжелом течении ХОБЛ. Наряду с появлением новых молекул совершенствуются способы доставки уже известных субстанций.
В базисной терапии ХОБЛ на первое место выходят длительно действующие бронходилататоры, среди которых наиболее изученным и применяемым является антихолинергический препарат тиотропия бромид.
Совокупный анализ ряда исследований (INLIGHT2, INVOLVE, INCHANCE) показал, что и современные препараты группы ДДБА значимо снижают частоту обострений.
Однако максимальное уменьшение числа обострений наблюдается на фоне приема длительнодействующего антихолинергического препарата (ДДАХ). В большинстве работ по изучению эффективности тиотропия бромида продемонстрировано снижение частоты среднетяжелых и тяжелых обострений ХОБЛ (INVIGORATE).
Появление тиотропия бромида – первого 24-часового избирательного холиноблокатора открыло новую эпоху бронхолитической терапии, названную «фармакологическим стентированием». Препарат сразу же занял свою нишу, а переход на ABCD-классификацию позволил использовать его при всех типах ХОБЛ (таблица 1).
Таблица 1. Новый клинический алгоритм терапии ХОБЛ (GOLD 2014-2015)
|
Группа больных ХОБЛ |
Препарат выбора |
Альтернативные препараты |
Другие препараты |
|
ХОБЛ легкого и среднетяжелого течения (ОФВ1 ≥ 50% от д.в.) с редкими обострениями и невыразительными симптомами (группа А) |
1-я схема: КДАХ по требованию 2-я схема: КДБА по требованию |
1-я схема: ДДАХ 2-я схема: ДДБА 3-я схема: КДБА в сочетании с КДАХ |
Теофиллины |
|
ХОБЛ легкого и среднетяжелого течения (ОФВ1 ≥ 50% от д.в.) с редкими обострениями и выраженными симптомами (группа В) |
1-я схема: ДДАХ 2-я схема: ДДБА |
1-я схема: ДДАХ в сочетании с ДДБА |
КДАХ и/или КДБА Теофиллины |
|
ХОБЛ тяжелого и крайне тяжелого течения (ОФВ1<50%д.в.) с частыми обострениями и невыраженными симптомами (группа С) |
1-я схема: ДДБА/иГКС 2-я схема: ДДАХ |
1-я схема: ДДАХ в сочетании с ДДБА 2-я схема: ДДАХ в сочетании с ингибитором ФДЭ-4 3-я схема: ДДБА в сочетании с ингибитором ФДЭ-4 |
КДАХ и/или КДБА Теофиллины |
|
ХОБЛ тяжелого и крайне тяжелого течения (ОФВ1<50% д.в.) с частыми обострениями и выраженными симптомами (группа D) |
1-я схема: ДДБА/иГКС 2-я схема: ДДАХ дополнительно к лекарственным препаратам 1-й схемы 3-я схема: ДДАХ |
1-я схема: ДДБА/иГКС в сочетании с ДДАХ 2-я схема: ДДБА/иГКС в сочетании с ингибитором ФДЭ-4 3-я схема: ДДАХ в сочетании с ДДБА 4-я схема: ДДАХ в сочетании с ингибитором ФДЭ-4 |
Карбоцистеин, NAC КДАХ и/или КДБА Теофиллины |
|
Примечание: КДАХ – короткодействующие антихолинергики, ДДАХ – длительнодействующие антихолинергики, ДДБА – бета-2-агонисты длительного действия, КДБА – бета-2-агонисты короткого действия, ФДЭ – фосфодиэстераза, иГКС – ингаляционные глюкокортикостероиды, NAC – N-ацетил-цистеин |
|||
Последующие схемы эффективной терапии – тройная комбинация в виде одновременного применения тиотропия, будесонида и формотерола оказались значимо эффективнее как моно-, так и двойной терапии.
Современные схемы лечения характеризуются конкурентными работами по применению при ХОБЛ комбинаций как ИГКС ДДБА, так и ДДАХ ДДБА. В работе H. Magnussen и соавт. показано, что у пациентов с ХОБЛ тяжелого течения, получающих совместно тиотропия и сальметерол, риск развития среднетяжелых и тяжелых обострений не зависел от того, принимались ли ИГКС.
Особое место для назначения кортикостероидов отведено лечению ХОБЛ с фенотипом ACOS (сочетание ХОБЛ с бронхиальной астмой). Эффективность стероидной терапии (как ингаляционной, так и системной) в данном случае выше, чем при ХОБЛ других фенотипов, особенно при ХОБЛ с бронхоэктазами и инфекционными обострениями, где показания к стероидной терапии весьма ограничены.
Доказанными достоинствами тиотропия бромида являются его селективность к М1- и М3-рецепторам, а также длительность действия. Препарат обеспечивает бронхолитический эффект в течение 24 часов, что позволяет использовать его 1 раз в сутки, что повышает приверженность больных к лечению.
Прирост функциональных легочных показателей на фоне приема тиотропия бромидом во всех исследованиях превышал таковой в группах препаратов сравнения (ипратропий, сальметерол и др.), данное улучшение не снижалось на протяжении всего периода исследования. Тиотропия бромид – первый препарат, уменьшающий легочную гиперинфляцию наряду с улучшением переносимости физических нагрузок. На фоне приема тиотропия наблюдалось также уменьшение частоты госпитализаций, числа обострений и увеличение периода до первого обострения.
В глобальном исследовании UPLIFT (Understanding Potential Long-term impacts on Function with Tiotropium) были получены доказательства снижения летальности пациентов с ХОБЛ на фоне приема тиотропия. Прием тиотропия продемонстрировал уменьшение частоты эпизодов дыхательной недостаточности (ОР 0,69; 95% ДИ 0,52–0,92).
Большая часть исследований эффективности тиотропия бромида проведено с применением порошкового доставочного устройства ХандиХалер (1 ингаляция по 18 мкг в сутки), рис. 1.
Позже было разработано устройство Респимат, получившее теперь регистрацию и в Казахстане.
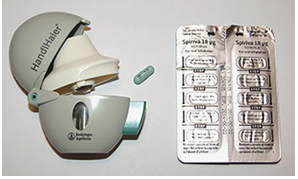
Рисунок 1 – Тиотропия бромид в устройстве ХандиХалер
Известно, что успех ингаляционной терапии определяется как свойствами субстанции, так и наличием оптимальной системы доставки. Идеальное ингаляционное устройство должно обеспечивать хорошую депозицию препарата в легочной ткани, быть простым и доступным для применения в любом возрасте и при любой тяжести заболевания. В этом плане ингаляционное устройство Респимат сделало революционный шаг в ингаляционной терапии.
В основе ингалятора Респимат (Respimat soft mist inhaler) лежит форсированное прохождение раствора лекарственного препарата через каналы, которые сходятся к двум выпускным соплам (рис. 2 и 3). Для активации устройства основание поворачивают на 180 градусов до щелчка, это приводит к сжатию пружины и продвижению капиллярной трубки картриджа с раствором. Так жидкость поступает в дозирующую камеру (рис. 2). При нажатии на кнопку пружина освобождается и проталкивает капиллярную трубку к униблоку (рис. 2 и 3), закрывая клапан и тем самым продвигая раствор через униблок.
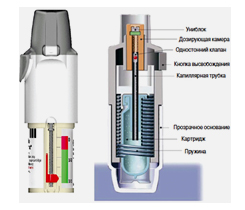
Рисунок 2 – Респимат: внешний вид и схема устройства
Далее раствор проталкивается через микроканалы, которые сходятся к двум зеркальным выпускным отверстиям – соплам (рис. 3).
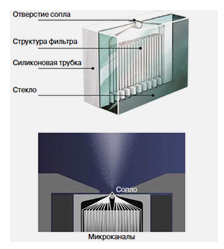
Рисунок 3 – Устройство униблока в ингаляторе Респимат
При выходе из сопла жидкостные струи сталкиваются между собой под определенным углом, в результате чего образуется аэрозоль лекарственного препарата (рис. 4).
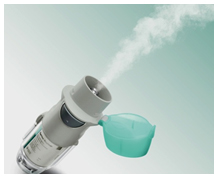
Рисунок 4 – Распыление лекарственного препарата через ингалятор Респимат
Ингалятор Респимат имеет цифровой счетчик доз (рис. 2). Стрелка счетчика подходит к красной зоне, когда остается несколько доз препарата (на 5-7 дней). После использования всех доз (в Спирива Респимат 60 доз) механизм блокируется и применение ингалятора становится невозможным, что позволяет пациенту точно определиться с отсутствием лекарства и необходимостью смены катриджа.
Для эффективной ингаляции определен оптимальный аэродинамический диаметр частиц аэрозоля, составляющий от 1 до 5 мкм. Частицы диаметром менее 1 мкм не оседают в дыхательных путях и выходят при выдохе, а частицы размером более 5 мкм в основном оседают в верхних отделах и ротоглотке.
Большая часть аэрозольных частиц (более 75%), генерируемых Респиматом, имеют диаметр менее 5 мкм.
Эффективность ингаляционной терапии зависит также от депозиции субстанции в ингаляционном устройстве и в ротоглотке, что зависит от скорости и времени существования аэрозольного облака, а также его турбулентной дисперсности. Один из механизмов улучшения доставки лекарственного препарата в нижние отделы дыхательной системы – это разработка аэрозольного облака с более длительным временем существования.
При измерении скорости струи аэрозоля на расстоянии 10 см от выхода из различных ингаляционных устройств было определено, что самая низкая скорость распыления аэрозоля (0,8 м/сек) наблюдается у Респимата, в то время как у дозированного аэрозольного ингалятора (ДАИ) от 2,4 до 5,6 м/сек. Длительность существования облака аэрозоля при использовании Респимата составила 1,45 сек, ДАИ – от 0,15 до 0,21 сек (рис. 5).
Это позволяет определить Респимат как ингалятор с созданием медленного аэрозольного облака с длительностью существования в 7–10 раз больше, чем при использовании ДАИ. Низкая скорость аэрозоля, создаваемая Респиматом, увеличивает доставку препарата в нижние респираторные отделы и уменьшает депозицию лекарственной субстанции в ротоглоке. Данное обстоятельство сопровождается увеличением эффективности ингаляционной терапии с уменьшением риска побочных эффектов.
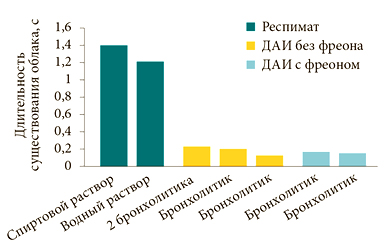
Рисунок 5 – Длительность существования аэрозольного облака при использовании Респимата и ДАИ
Проведение сцинтиграфии также подтвердило меньшую ротоглоточную и более высокую легочную депозицию препарата при использовании Респимата в сравнении с ДАИ со спейсером (рис. 6).
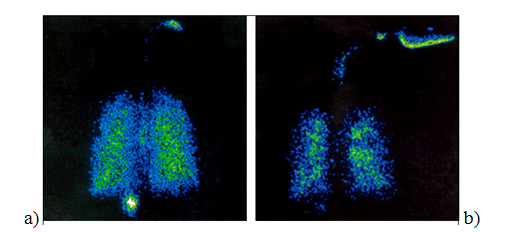
Рисунок 6 – Сцинтиграфическое распределение лекарственного препарата при использовании Респимата (a) и ДАИ со спейсером (b)
Ингалятор Респимат продемонстрировал более высокую эффективность с меньшим числом ожидаемых побочных эффектов, что позволило пересмотреть дозы ингаляционного препарата, применяемого через Респимат.
В частности, была определена рекомендуемая эффективная доза тиотропия бромида в Респимате, составив 5 мкг, что по прогнозируемым эффектам соответствует 18 мкг тиотропия, применяемого через ХандиХалер.
Опубликованные результаты рандомизированных клинических исследований по изучению тиотропия бромида в устройстве Респимат в течение не менее 12 недель показали, что Спирива Респимат в дозах 5 и 10 мкг превосходил плацебо и был сопоставим по бронхолитическому эффекту с ипратропием в первые часы после ингаляции. Обе дозы тиотропия приводили к и клинически достоверному улучшению функциональных показателей, уменьшению выраженности одышки и повышению качества жизни пациентов с ХОБЛ (табл. 2).

Таблица 2 – Сравнение тиотропия Респимат и плацебо: первичные конечные точки
Применение тиотропия бромид в устройстве Респимат сопровождалось уменьшением числа обострений ХОБЛ на 31%, в том числе тяжелых обострений, требующих госпитализации – на 27%.
Резюмируя вышесказанное, можно заключить, что применение тиотропиума бромида в ингаляторе Респимат достоверно улучшает легочную функцию, уменьшает одышку, повышает качество жизни пациентов, а также снижает частоту обострений, в том требующих госпитализации. Все это позволило включить форму Респимат как одно из наиболее оптимальных устройств для ингаляции тиотропиума бромида (GOLD 2014-2015).
Тиотропия бромид, наряду с другими представителями группы АХП, рассматривается как один из наиболее безопасных бронхолитиков для терапии ХОБЛ.
Благоприятный профиль безопасности тиотропия в устройстве ХандиХалер доказан ранее в многочисленных исследованиях. Тиотропия бромид в Респимате может демонстрировать еще большую безопасность, так как содержит меньшую дозу препарата и минимальную ротоглоточную депозицию, что ожидаемо сопровождается меньшей системной биодоступностью.
Анализ частых нежелательных явлений, выявленных у Спиривы Респимат продемонстрировал возникновение сухости во рту, специфического побочного эффекта всех АХП (табл. 3). Этот побочный эффект наблюдался в 2 раза реже при использовании устройства Респимат, чем ХандиХалера, что объясняется меньшей депозицией препарата в ротоглотке.
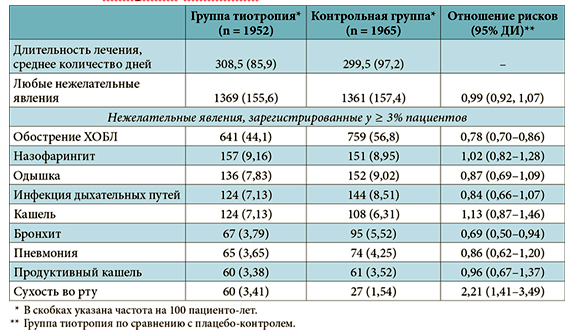
Таблица 3 – Наиболее распространенные нежелательные явления при использовании Спиривы Респимат
При оценке частоты побочных эффектов на фоне приема высоких доз тиотропиума бромида в Респимате (до 32 мкг/сут) были отмечены лишь легкие антихолинергические эффекты (сухость слизистых оболочек). Закапывание раствора тиотропия в глаза не сопровождалось изменением диаметра зрачка, внутриглазного давления, аккомодации, что подтверждает безопасность тиотропиума в Респимате в случае попадания препарата в глаза.
Достоверные сведения об эффективности и безопасности Спиривы Респимат представлены в крупнейшем к данному времени исследовании ХОБЛ – рандомизированном двойном слепом исследовании TIOSPIR (The Tiotropium Safety and Performance in Respimat Trial). В исследование TIOSPIR было включено 17135 пациентов с ХОБЛ (средний возраст 65 лет, средний ОФВ1 48%), которые на протяжении в среднем 2,3 года принимали Спириву Респимат в дозе 2,5 или 5 мкг или Спириву ХандиХалер в дозе 18 мкг в сутки. Первичными конечными точками были риск летального исхода и риск развития первого обострения заболевания. Оценивалась также сердечно-сосудистая безопасность тиотропиума бромида в разных формах и разных дозировках. Необходимо отметить, что часть пациентов, включенных в исследование имели стабильные сердечно-сосудистые заболевания: у 15,2% – ИБС, у 6% – постинфарктный кардиосклероз, у 10,6% – аритмии.
Результаты исследования TIOSPIR показали, что по риску летальных исходов длительная терапия Спиривой Респимат не отличается от Спиривы ХандиХалер (для тиотропия 5 мкг ОР 0,96; 95% ДИ 0,84–1,09; для тиотропия 2,5 мкг ОР 1,00; 95% ДИ 0,87–1,14) и по риску развития первого обострения (для тиотропия 5 мкг ОР 0,98; 95% ДИ 0,93–1,03) (рис. 7 и 8, табл. 4). Частота летальных исходов и сердечно-сосудистых событий во всех группах лечения тиотропием были сходными.
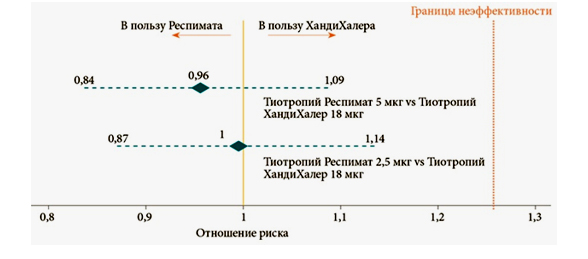
Рисунок 7 – Летальность от любых причин у пациентов с ХОБЛ при лечении препаратами тиотропия бромида в разных устройствах
Таблица 4 – Летальность от всех причин при терапии препаратами тиотропия
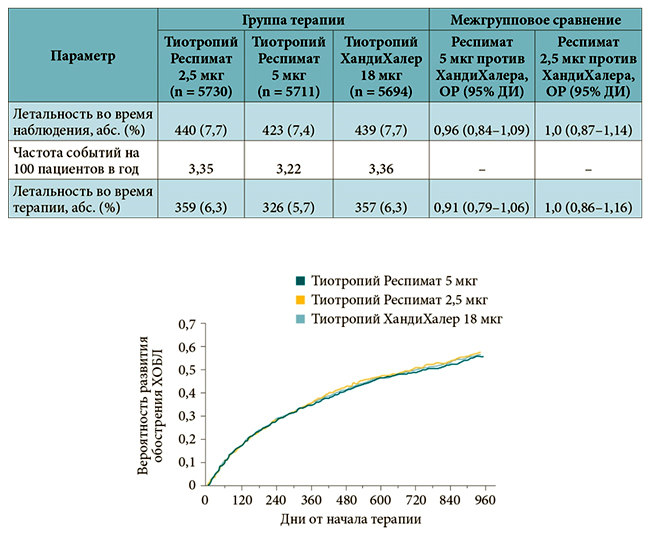
Рисунок 8 – Время до развития первого обострения ХОБЛ при лечении препаратами тиотропия
Таким образом, итоги глобального исследования TIOSPIR разрешили палемику о сердечно-сосудистых рисках применения Спиривы Респимат, показав, что тиотропия бромид в Респимате демонстрирует как высокую эффективность, так и обладает хорошим профилем безопасности.
Спирива Респимат в лечении бронхиальной астмы
При бронхиальной астме (БА) в ряде случаев применение средних доз ингаляционных глюкокортикостероидов (ИГКС) не дает возможности достижения полного контроля над астмой. В подобных ситуациях, согласно GINA (update 2015), рекомендуется увеличение объема базисной терапии в виде увеличения дозы ИГКС, назначение бета-2-агонистов длительного действия (ДДБА) в форме фиксированных комбинаций ИГКС/ДДБА, а также дополнения антагонистами рецепторов лейкотриенов.
Эффективность тиотропия бромида при БА изучалась в ряде исследований. S.P. Peters и соавт. в двойном слепом перекрестном рандомизированном исследовании TALC (Tiotropium bromide as an Alternative to increased inhaled glucocorticoid in patients inadequately controlled on a Lower dose of inhaled Corticosteroid) сравнивали дополнительную терапию тиотропием с удвоением дозы ИГКС и дополнительной терапией ДДБА при плохо контролируемой астме на фоне монотерапиий ИГКС. Было показано, что при недостаточном контроле БА на фоне монотерапии ИГКС добавление тиотропия бромида было более эффективным, чем удвоение дозы ИГКС. Это сопровождалось улучшением легочной функции, уменьшением частоты и выраженности симптомов БА и увеличением числа дней полного контроля заболевания.
В последующем были получены данные о роли тиотропия бромида при плохо контролируемой БА. В двух сходных исследованиях изучена эффективность дополнительной терапии тиотропием (в дозе 5 мкг в сутки через Респимат) при БА, на фоне уже проводимого лечения ИГКС и ДДБА. Эффективность лечения оценивалась по функциональным легочным параметрам и частоте развития обострений. Длительность исследования составила 48 недель. Перед включением в исследование у пациентов отмечались симптомы заболевания, снижение ОФВ1 менее 80% д.в., наличие не менее одного обострения БА за последний год. Всего в исследовании включено 912 пациентов с БА (средний возраст 53 года, ОФВ1 в среднем 62%). Уже через 24 недели от начала лечения изменение ОФВ1 в сравнении с исходным было большим в группе пациентов с добавлением тиотропия бромида. Дополнительная терапия тиотропием сопровождалась уменьшением частоты тяжелых обострений БА на 21% (ОР 0,79; р = 0,03) и увеличению времени до первого обострения (282 против 226 дней). Нежелательные явления и серьезные побочные эффекты наблюдались с одинаковой частотой в группах сравнения. Сухость во рту, как наиболее характерный побочный эффект АХП, отмечена менее чем у 2% пациентов.
Эффекты от добавления тиотропия к стандартной терапии астмы сравнивались с более принятой терапией БА в виде добавление антагонистов рецепторов лейкотриенов и ксантинов к ИГКС/ДДБА. Данные схемы не сопровождались значительными положительными результатами, а лечение с использованием системных стероидов сопровождается тяжелыми побочными эффектами.
Выбор оптимального ингаляционного устройства
При выборе ингаляционного устройства врачом учитывается множество факторов, таких как субстанция лекарственного вещества, имеющаяся доказанная клиническая эффективность препарата, простота техники применения ингаляционного устройства, стоимость и доступность препарата в конкретном ингаляционном устройстве. Наряду с указанными факторами, значимые позиции при определении типа ингалятора должно занимать отношение и комплайнс пациента к устройству.
Преимуществом ингалятора Респимат в первую очередь является простота техники ингаляции. Адекватная техника ингаляции при использовании устройства Респимата при непродолжительном обучении может быть достигнута в 96–98% случаев. Положительным моментом применения Респимата также является хорошая координация «пациент- ингалятор», что позволяет достичь высокой легочной депозиции препарата даже без предшествующего обучения пациента (до 37%) с возрастанием дозы лекарственного препарата в нижних отделах дыхательной системы до 53% после обучения больных (рис. 9). В сравнении с Респиматом наибольшие цифры легочной депозиции при ингаляции через ДАИ составили лишь 21%.
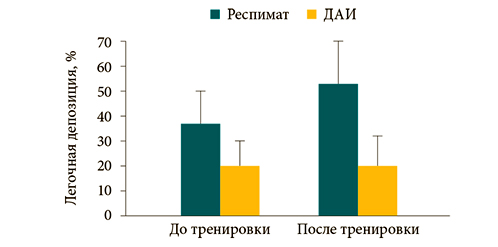
Рисунок 9 – Влияние обучения на легочную депозицию при использовании ингаляционных устройств Респимат и ДАИ
Применение валидизированных опросников по удовлетворенности и предпочтению пациента (Patient Satisfaction and Preference Questionnaire – PASAPQ) в качестве инструмента по выяснению отношения пациента к ингаляционную устройству показало, что большая часть опрошенных пациентов (81%) предпочли устройство Респимат для дальнейшего применения.
При сравнении отношения пациентов с ХОБЛ и БА к ингалятору Респимата и дозированных порошковых ингаляторов (ДПИ) в виде мультидиска и турбухалера) предпочтение Респимату отдали 74% больных, Турбухалеру – 17%, Мультидиску – 34% (рис. 10).
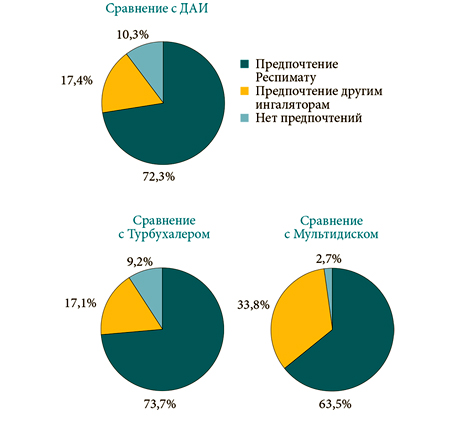
Рисунок 10 – Предпочтения пациентов при использовании разных ингаляторов
Анализируя вышеизложенное, можно резюмировать, что ингаляционное устройство Респимат отличается простотой техники ингаляции, создает хороший комплайнс проводимой терапии и обепечивает адекватную координацию «пациент-ингалятор», что подтверждается опросом самих пациентов.
Базисная терапия препаратом тиотропия бромид в устройстве Респимат при ХОБЛ достоверно улучшает легочную функцию, снижает выраженность одышки, увеличивает качество жизни, уменьшает частоту обострений, в том числе требующих госпитализации.
Сведения о побочных эффектах лечения тиотропиумом через Респимат аналогичны с ранее описанными нежелательными явлениями тиотропия в ХандиХалере, что подтверждено в исследовании TIOSPIR.
Дополнительное показание использования тиотропия Респимат – плохо контролируемая БА на фоне терапии ИГКС и ДДБА. Тиотропия Респимат показано у взрослых пациентов с неконтролируемой БА, перенесших не менее одного обострения заболевания за предшествующий год. ТиотропияРеспимат как дополнительный компонент базисной терпаии БА позволяет значимо снизить выраженность бронхиальной обструкции и минимизировать риск развития тяжелых обострений заболевания.
Приложение 1
Техника применения ингаляционного устройства Респимат

 1. При закрытом колпачке нажмите стопорную кнопку (Е) и одновременно снимите прозрачную гильзу (G) потянув ее вниз.
1. При закрытом колпачке нажмите стопорную кнопку (Е) и одновременно снимите прозрачную гильзу (G) потянув ее вниз.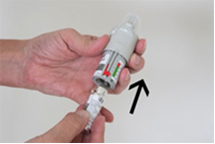 2. Выньте картридж (H) из упаковки. Вставьте его узким концом в ингалятор до фиксации.
2. Выньте картридж (H) из упаковки. Вставьте его узким концом в ингалятор до фиксации.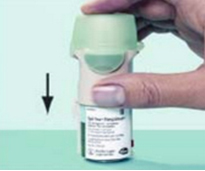 3. Чтобы убедиться в том, что картридж полностью вставлен, следует cильно надавить картриджем на твердую поверхность. При этом дно картриджа не должно быть на одном уровне с нижним краем ингалятора, нижняя часть картриджа серебрянного цвета должна быть видна.
3. Чтобы убедиться в том, что картридж полностью вставлен, следует cильно надавить картриджем на твердую поверхность. При этом дно картриджа не должно быть на одном уровне с нижним краем ингалятора, нижняя часть картриджа серебрянного цвета должна быть видна.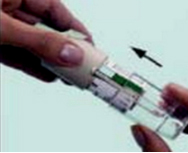 4. Оденьте снова прозрачную гильзу (G).
4. Оденьте снова прозрачную гильзу (G).После этого гильза не должна больше сниматься.
 5. Держите ингалятор СПИРИВА РЕСПИМАТ вертикально с одетым колпачком (A). Поверните прозрачную гильзу (G) в направлении красных стрелок, указанных на этикетке, до щелчка (пол-оборота).
5. Держите ингалятор СПИРИВА РЕСПИМАТ вертикально с одетым колпачком (A). Поверните прозрачную гильзу (G) в направлении красных стрелок, указанных на этикетке, до щелчка (пол-оборота).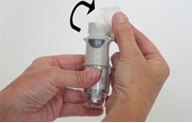 6. Снимите колпачок (A)
6. Снимите колпачок (A) 7. Направьте ингалятор СПИРИВА РЕСПИМАТ вниз. Нажмите кнопку подачи дозы (D). Закройте колпачок.
7. Направьте ингалятор СПИРИВА РЕСПИМАТ вниз. Нажмите кнопку подачи дозы (D). Закройте колпачок.
Повторите этапы 4, 5 и 6 до появления аэрозольного облачка. Теперь ингалятор СПИРИВА РЕСПИМАТ готов к применению. Осуществление этих этапов не уменьшает число доз препарата. После подготовки ингалятор СПИРИВА РЕСПИМАТ позволяет высвободить 30 доз лекарства (60 ингаляций).
Ингалятор используется только ОДИН РАЗ В ДЕНЬ. Каждый раз делается ДВЕ ИНГАЛЯЦИИ
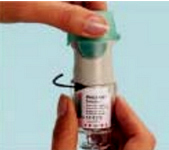 Держите ингалятор СПИРИВА РЕСПИМАТ вертикально с одетым колпачком (A), чтобы предотвратить случайное высвобождение лекарства. Поверните прозрачную гильзу (G) по направлению красных стрелок, указанных на этикетке, до щелчка (пол-оборота).
Держите ингалятор СПИРИВА РЕСПИМАТ вертикально с одетым колпачком (A), чтобы предотвратить случайное высвобождение лекарства. Поверните прозрачную гильзу (G) по направлению красных стрелок, указанных на этикетке, до щелчка (пол-оборота).
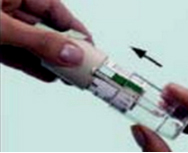 Снимите колпачок (A) Выдохните медленно и глубоко. Охватите плотно губами конец мундштука.
Снимите колпачок (A) Выдохните медленно и глубоко. Охватите плотно губами конец мундштука.
Воздушное отверстие ингалятора (C) должно быть при этом свободно. Направьте ингалятор СПИРИВА РЕСПИМАТ к задней части горла. Во время медленного и глубокого вдоха через рот нажмите кнопку подачи дозы (D) и продолжайте вдох как можно дольше. Задержите дыхание на 10 секунд или так долго, как вам удобно. Повторите этапы I и II, чтобы получить полную дозу.
Список литературы:
1. Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких (пересмотр 2011 г.): пер. с англ. / под ред. А.С. Белевского. – М.: Российское респираторное общество, 2012.- 80 с.: ил.
2. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease (GOLD), Updated, 2015. (http://www.goldcopd.org/uploads/users/files/GOLD_Report_2015_Feb18.pdf)
3. http://www.who.int/mediacentre/factsheets/fs310/en/index.htm
4. Soler-Cataluña J.J., Martínez-García M.A., Román Sánchez P. et al. Severe acute exacerbations and mortality in patients with chronic obstructive pulmonary disease // Тhorax. 2005. Vol. 60. № 11. P. 925–931.
5. Postma D., Anzueto A., Calverley P. et al. A new perspective on optimal care for patients with COPD // Prim. Care Respir. J. 2011. Vol. 20. № 2. P. 205–209.
6. Чучалин А.Г., Авдеев С.Н., Айсанов З.Р. и др. Российское респираторное общество. Федеральные клинические рекомендации по диагностике и лечению хронической обструктивной болезни легких // Пульмонология. 2014. № 3. С. 15–54.
7. Wedzicha J., Buhl R., Lawrence D., McBryan D. Indacaterol once daily reduces the risk of COPD exacerbations over 6 months of treatment: a pooled analysis. Poster presented at COPD 8 Congress 2012, Birmingham.
8. Decramer M.L., Chapman K.R., Dahl R. et al. Once-daily indacaterol versus tiotropium for patients with severe chronic obstructive pulmonary disease (INVIGORATE): a randomised, blinded, parallel-group study // Lancet. Respir. Med. 2013. Vol. 1. № 7. P. 524–533.
9. Welte, T. Efficacy and tolerability of budesonide/formoterol added to tiotropium in patients with chronic obstructive pulmonary disease / T. Welte, M. Miravitlles, P. Hernandez [et al.] // Am. J. Respir. Crit. Care Med. — 2009. – Vol. 180(8). — P.741—750.
10. Magnussen, H. WISDOM Investigators. Withdrawal of inhaled glucocorticoids and exacerbations of COPD / H. Magnussen, B. Disse, R. Rodriguez-Roisin [et al.] // N. Engl. J. Med. — 2014. — Vol. 371(14). — P.1285-1294.
11. Kew, K.M. Long-acting inhaled therapy (beta-agonists, anticholinergics and steroids) for COPD: a network metaanalysis / K.M. Kew, S. Dias, C.J. Cates // Cochrane Database Syst. Rev. — 2014. — Vol. 26, № 3. – CD010844.
12. Panning C.A., DeBisschop M. Tiotropium: an inhaled, long-acting anticholinergic drug for chronic obstructive pulmonary disease // Pharmacotherapy. 2003. Vol. 23. № 2. P. 183–189.
13. Yohannes A.M., Connolly M.J., Hanania N.A. Ten years of tiotropium: clinical impact and patient perspectives // Int. J. Chron. Obstruct. Pulmon. Dis. 2013. Vol. 8. P. 117–125.
14. Tashkin D.P. Long-acting anticholinergic use in chronic obstructive pulmonary disease: efficacy and safety // Curr. Opin. Pulm. Med. 2010. Vol. 16. № 2. P. 97–105.
15. Donohue J.F., van Noord J.A., Bateman E.D. et al. A 6-month, placebo-controlled study comparing lung function and health status changes in COPD patients treated with tiotropium or salmeterol // Chest. 2002. Vol. 122. № 1. P. 47–55.
16. Vincken W., van Noord J.A., Greefhorst A.P. et al. Improved health outcomes in patients with COPD during 1 yr›s treatment with tiotropium // Eur. Respir. J. 2002. Vol. 19. № 2. P. 209–216.
17. Tashkin D.P., Celli B., Senn S. et al. A 4-year trial of tiotropium in chronic obstructive pulmonary disease // N. Engl. J. Med. 2008. Vol. 359. № 15. P. 1543–1554.
18. Decramer M., Celli B., Kesten S. et al. Effect of tiotropium on outcomes in patients with moderate chronic obstructive pulmonary disease (UPLIFT): a prespecified subgroup analysis of a randomised controlled trial // Lancet. 2009. Vol. 374. № 9696. P. 1171–1178.
19. Troosters T., Celli B., Lystig T. et al. Tiotropium as a first maintenance drug in COPD: secondary analysis of the UPLIFT trial // Eur. Respir. J. 2010. Vol. 36. № 1. P. 65–73.
20. Panos R.J. Efficacy and safety of eco-friendly inhalers: focus on combination ipratropium bromide and albuterol in chronic obstructive pulmonary disease // Int. J. Chron. Obstruct. Pulmon. Dis. 2013. Vol. 8. P. 221–230.
21. Dalby R.N., Eicher J., Zierenberg B. Development of Respimat(®) Soft Mist™ Inhaler and its clinical utility in respiratory disorders // Med. Devices (Auckl.). 2011. Vol. 4. P. 145–155.
22. Stein S.W., Gabrio B.J. Understanding throat deposition during cascade impactor testing // Respiratory drug delivery. VII / Ed. by R.N. Dalby, P.R. Byron, S.J. Farr, J. Peart. Raleigh, NC: Serentec Press, 2000. P. 573–576.
23. Longest P.W., Hindle M., Das Choudhuri S., Byron P.R. Numerical simulations of capillary aerosol generation: CFD model development and comparisons with experimental data // Aerosol. Sci. Technol. 2007. Vol. 41. P. 952–973.
24. Longest P.W., Hindle M., Das Choudhuri S., Xi J. Comparison of ambient and spray aerosol deposition in a standard induction port and more realistic mouth–throat geometry // J. Aerosol. Sci. 2008. Vol. 39. P. 572–591.
25. Newman S.P. Aerosol deposition considerations in inhalation therapy // Chest. 1985. Vol. 88. № 2. Suppl. P. 152S–160S.
26. Longest P.W., Hindle M. Quantitative analysis and design of a spray aerosol inhaler. Part 1: effects of dilution air inlets and flow paths // J. Aerosol. Med. Pulm. Drug Deliv. 2009. Vol. 22. № 3. P. 271–283.
27. Hochrainer D., Hölz H., Kreher C. et al. Comparison of the aerosol velocity and spray duration of Respimat Soft Mist inhaler and pressurized metered dose inhalers // J. Aerosol. Med. 2005. Vol. 18. № 3. P. 273–282.
28. Newman S.P., Brown J., Steed K.P. et al. Lung deposition of fenoterol and flunisolide delivered using a novel device for inhaled medicines: comparison of RESPIMAT with conventional metered-dose inhalers with and without spacer devices // Chest. 1998. Vol. 113. № 4. P. 957–963.
29. Pitcairn G., Reader S., Pavia D., Newman S. Deposition of corticosteroid aerosol in the human lung by Respimat Soft Mist inhaler compared to deposition by metered dose inhaler or by Turbuhaler dry powder inhaler // J. Aerosol. Med. 2005. Vol. 18. № 3. P. 264–272.
30. Caillaud D., Le Merre C., Martinat Y. et al. A dose-ranging study of tiotropium delivered via Respimat Soft Mist Inhaler or HandiHaler in COPD patients // Int. J. Chron. Obstruct. Pulmon. Dis. 2007. Vol. 2. № 4. P. 559–565.
31. Bateman E., Singh D., Smith D. et al. Efficacy and safety of tiotropium Respimat SMI in COPD in two 1-year randomized studies // Int. J. Chron. Obstruct. Pulmon. Dis. 2010. Vol. 5. P. 197–208.
32. Bateman E.D., Tashkin D., Siafakas N. et al. A one-year trial of tiotropium Respimat plus usual therapy in COPD patients // Respir. Med. 2010. Vol. 104. №
33. Rau-Berger H., Mitfessel H., Glaab T. Tiotropium Respimat® improves physical functioning in chronic obstructive pulmonary disease // Int. J. Chron. Obstruct. Pulmon. Dis. 2010. Vol. 5. P. 367–373.
34. Asakura Y., Nishimura N., Maezawa K. et al. Effect of switching tiotropium HandiHaler® to Respimat® Soft Mist™ Inhaler in patients with COPD: the difference of adverse events and usability between inhaler devices // J. Aerosol. Med. Pulm. Drug Deliv. 2013. Vol. 26. № 1. P. 41–45 10. P. 1460–1472.
35. Feifel U., Wallenstein G., Rominger K.L. et al. Pharmacokinetics and tolerability (Study 1) with particular reference to ocular safety (Study 2) of tiotropium Respimat soft mist inhaler: findings from two dose-ranging studies in healthy men // Int. J. Chron. Obstruct. Pulmon. Dis. 2008. Vol. 3. № 3. P. 397–403.
36. Wise R.A., Anzueto A., Cotton D. et al. Tiotropium Respimat inhaler and the risk of death in COPD // N. Engl. J. Med. 2013. Vol. 369. № 16. P. 1491–1501.
37. http://www.ginasthma.org/local/uploads/files/GINA_Report_2015.
38. Peters S.P., Kunselman S.J., Icitovic N. et al. Tiotropium bromide step-up therapy for adults with uncontrolled asthma // N. Engl. J. Med. 2010. Vol. 363. № 18. P. 1715–1726.
39. Kerstjens H.A., Engel M., Dahl R. et al. Tiotropium in asthma poorly controlled with standard combination therapy // N. Engl. J. Med. 2012. Vol. 367. № 13. P. 1198–1207.
40. Schürmann W., Schmidtmann S., Moroni P. et al. Respimat Soft Mist inhaler versus hydrofluoroalkane metered dose inhaler: patient preference and satisfaction // Treat. Respir. Med. 2005. Vol. 4. № 1. P. 53–61
41. Hodder R., Price D. Patient preferences for inhaler devices in chronic obstructive pulmonary disease: experience with Respimat Soft Mist inhaler // Int. J. Chron. Obstruct. Pulmon. Dis. 2009. Vol. 4. P. 381–390.
42. Brand P., Hederer B., Austen G. et al. Higher lung deposition with Respimat Soft Mist inhaler than HFA-MDI in COPD patients with poor technique // Int. J. Chron. Obstruct. Pulmon. Dis. 2008. Vol. 3. № 4. P. 763–770.
43. Kozma C.M., Slaton T.L., Monz B.U. et al. Development and validation of a patient satisfaction and preference questionnaire for inhalation devices // Treat. Respir. Med. 2005. Vol. 4. № 1. P. 41–52.
44. Hodder R., Reese P.R., Slaton T. Asthma patients prefer Respimat Soft Mist Inhaler to Turbuhaler // Int. J. Chron. Obstruct. Pulmon. Dis. 2009. Vol. 4. P. 225–232.
45. Freytag F., Rau-Berger H., Glaab T., Wolf K. Respimat® Soft Mist™ Inhaler preferred to Diskus by patients with COPD and/or asthma // Am. J. Respir. Crit. Care Med. 2007. Vol. 175. P. A639







