Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "Применение тиотропия бромида при хронических бронхолегочных заболеваниях"
Автор: И.Г. Березняков Харьковская медицинская академия последипломного образования
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Пульмонология, Семейная медицина/Терапия
Просмотров: 3 067
Дата проведения: с 22.06.2015 по 22.06.2016
Бронходилататоры (антихолинергические средства и β2-агонисты) занимают ключевую позицию в терапии хронической обструктивной болезни легких (ХОБЛ). В настоящей работе с позиций доказательной медицины будут рассмотрены эффективность и безопасность длительно действующего антихолинергического препарата тиотропия бромида у больных ХОБЛ и перспективы его использования для лечения бронхиальной астмы (БА). Отличительной особенностью препарата является наличие различных доставочных устройств (порошкового и жидкостного ингаляторов).
Патофизиологические механизмы
В перибронхиальных нервных узлах (ганглиях) преганглионарные парасимпатические волокна блуждающего нерва формируют синапсы с постганглионарными нейронами, от которых отходят постганглионарные волокна, иннервирующие дыхательные пути. Парасимпатическая активность опосредуется мускариновыми (М-) рецепторами. Среди них наибольшее значение придается первым трем подтипам. М1-рецепторы расположены на парасимпатических ганглиях и отвечают за передачу холинергических стимулов. Напротив, М2-рецепторы располагаются возле постганглионарных окончаний и по механизму обратной связи тормозят дальнейшее выделение ацетилхолина. М3-рецепторы, расположенные в гладких мышцах воздухоносных путей и подслизистых железах, обеспечивают контроль над тонусом гладких мышц (и, следовательно, просветом воздухоносных путей) и секрецией слизи.
Холинергическая иннервация в легких наиболее широко представлена в крупных воздухоносных путях и количественно уменьшается на уровне средних и особенно мелких бронхов и бронхиол. Соответственно, эффекты стимуляции холинергических нервов наиболее выражены в трахее и крупных бронхах и слабее реализуются на периферии бронхиального дерева.
Ранние антихолинергические средства для ингаляционного введения (ипратропиума бромид и др.) были неселективными антагонистами трех указанных подтипов рецепторов и характеризовались непродолжительным периодом действия. Первый длительно действующий антихолинергический препарат – тиотропия бромид – отличается большей селективностью в отношении М1- и М3-рецепторов и применяется 1 раз в сутки. Со времени своего внедрения в клиническую практику в начале нынешнего тысячелетия препарат нашел широкое применение для лечения больных ХОБЛ, для которого характерно необратимое или не полностью обратимое сужение воздухоносных путей. При хроническом обструктивном бронхите оно связано с сочетанием фиброза, прежде всего в периферических бронхах, и гиперплазии слизистой оболочки, в то время как при эмфиземе легких имеет место обтурация воздухоносных путей с потерей эластических элементов и утолщением альвеолярной стенки. В физиологических условиях бронхомоторный тонус, обусловленный активностью блуждающего нерва, оказывает определенное, но незначительное влияние на просвет воздухоносных путей. Однако при их сужении при ХОБЛ, из-за особенностей «геометрии» просвета бронхов, воздействие этого тонуса на динамику дыхания существенно возрастает. В подобных условиях применение антихолинергических препаратов вызывает существенно больший бронхорасширяющий эффект.
 Механизм действия антихолинергических препаратов при ХОБЛ не исчерпывается влиянием на тонус гладкой мускулатуры. Прямая или опосредованная холинергическая стимуляция (например, за счет воздействия табачного дыма, газов с резким запахом или других раздражителей на холинергические окончания в слизистой оболочке воздухоносных путей) вызывает отчетливую активацию подслизистых желез и секреторной функции бокаловидных клеток, что усиливает бронхиальную обструкцию при ХОБЛ. Поэтому ингаляция антихолинергических средств, ограничивающая секрецию бронхиальной слизи, может способствовать улучшению проходимости в периферических отделах бронхолегочной системы.
Механизм действия антихолинергических препаратов при ХОБЛ не исчерпывается влиянием на тонус гладкой мускулатуры. Прямая или опосредованная холинергическая стимуляция (например, за счет воздействия табачного дыма, газов с резким запахом или других раздражителей на холинергические окончания в слизистой оболочке воздухоносных путей) вызывает отчетливую активацию подслизистых желез и секреторной функции бокаловидных клеток, что усиливает бронхиальную обструкцию при ХОБЛ. Поэтому ингаляция антихолинергических средств, ограничивающая секрецию бронхиальной слизи, может способствовать улучшению проходимости в периферических отделах бронхолегочной системы.
Эффективность тиотропия бромида при ХОБЛ
1. Сравнение с плацебо
У больных ХОБЛ тиотропия бромид по сравнению с плацебо оказывает положительное влияние на качество жизни и значительно снижает риск обострений, том числе нуждающихся в лечении в условиях госпиталя. Как свидетельствуют результаты недавнего Кокрановского обзора, для предупреждения 1 обострения необходимо пролечить тиотропия бромидом 16 больных ХОБЛ на протяжении 1 г. Различия в госпитализации по любому поводу и в смертности между сравниваемыми группами отсутствовали [1]. Авторы обзора отметили, что больные, получавшие тиотропия бромид, существенно реже (примерно на одну треть) прекращали прием препарата, нежели пациенты из группы плацебо. Кроме того, ко времени завершения исследований у лечившихся тиотропия бромидом отмечалось улучшение функции легких, на что указывает увеличение объема форсированного выдоха за 1-ю секунду (ОФВ1) по сравнению с группой плацебо почти на 119 мл.
Всего проанализированы результаты 22 исследований длительностью от 3-х мес. до 4-х лет, в которых приняло участие более 23 тыс. пациентов. Полученные данные свидетельствуют о превосходстве тиотропия бромида над плацебо и разумности включения препарата в современные схемы лечения больных ХОБЛ.
2. Сравнение с ипратропиума бромидом
В 2013 г. авторы Кокрановского сотрудничества проанализировали влияние ипратропиума бромида и тиотропия бромида на качество жизни, обострения, симптомы, функцию легких и переносимость у больных ХОБЛ [2]. Длительность вмешательств колебалась от 12 недель до 1 года, общее количество включенных больных составило 1073 человека в возрасте 40 лет и старше со стажем курения не менее 10 пачко-лет, исходный ОФВ1 – в среднем 40% от должного. В качестве первичных исходов для анализа были выбраны величина ОФВ1 через 3 мес. от начала лечения и тяжелые несмертельные побочные эффекты (как любого генеза, так и специфичные для ХОБЛ). Причем побочные эффекты любого генеза были добавлены к болезнь-специфичным из-за высокого риска ошибок при объяснении причин возникновения того или иного нежелательного лекарственного явления.
Через 3 мес. ОФВ1 в группе больных, получавших тиотропия бромид, увеличился на 109 мл по сравнению с пациентами, получавшими ипратропиума бромид (95%-ный доверительный интервал (ДИ) 81–137 мл). Следует оговориться, что минимальная разница в величине ОФВ1, имеющая клиническое значение, составляет 150 мл. Риск развития тяжелых несмертельных побочных эффектов в группе лечения тиотропия бромидом был в 2 раза ниже (рис. 1). Лучшая переносимость тиотропия бромида документировалась также меньшим риском возникновения тяжелых несмертельных болезнь-специфичных нежелательных лекарственных явлений и отказов от продолжения лечения.
Другие исходы (госпитализации, общая смертность, качество жизни и т.д.) рассматривались как вторичные. Риск обострений ХОБЛ, нуждающихся в курсовом лечении кортикостероидами, антибиотиками, либо их комбинацией (рис. 1) и риск госпитализации по любому поводу также были ниже в группе в группе лиц, лечившихся тиотропия бромидом. Однако риск смертности от любой причины в группах сравнения оказался сопоставимым (рис. 2).
Рис. 1.
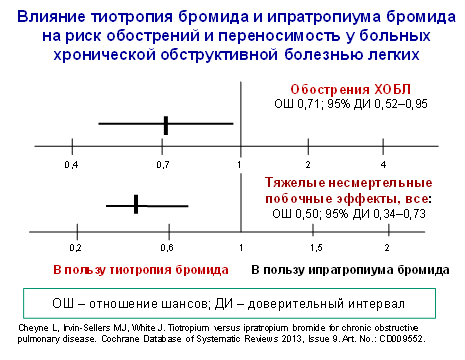
Рис. 2.
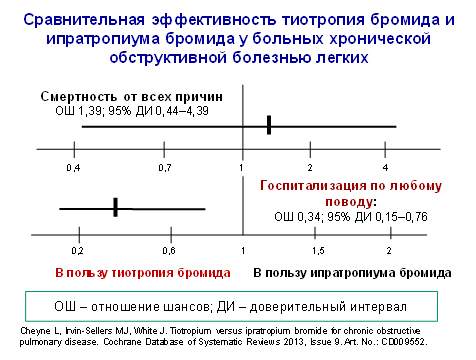
Через 1 год качество жизни больных, получавших тиотропия бромид, было лучше. Средняя разница в показателях респираторного опросника больницы Святого Георгия (SGRQ) составила 3,3 пункта [2]. Однако переоценивать эти данные не следует. Минимальная клинически значимая разница в изученном показателе составляет 4 пункта. Другими словами, выявленные различия имеют статистическое, но не клиническое значение.
Несмотря на ограниченность доказательной базы и неопределенность с выбором оптимального доставочного устройства при использовании тиотропия бромида, авторы пришли к заключению, что полученные данные свидетельствуют в пользу его применения вместо ипратропиума бромида в терапии больных со стабильной ХОБЛ. Этот вывод разделяют и авторы руководства GOLD, которые отмечают, что:
1) длительно действующие бронходилататоры (как β2-агонисты, так и антихолинергические средства) удобнее и эффективнее для достижения и сохранения облегчения симптомов ХОБЛ, чем короткодействующие бронходилататоры (уровень доказательств А); и
2) тиотропия бромид снижает частоту обострений ХОБЛ и связанных с ними госпитализаций, облегчает симптомы и улучшает состояние здоровья (уровень доказательств А), а также повышает эффективность легочной реабилитации (уровень доказательств В) [3].
3. Сравнение с β2-агонистами
Авторы руководства GOLD рассматривают длительно действующие бронходилататоры в качестве препаратов выбора для лечения больных ХОБЛ группы В (с большим количеством симптомов и низким риском обострений заболевания). При этом, по их мнению, в настоящее время отсутствуют доказательства в пользу превосходства антихолинергических средств над β2-агонистами, либо наоборот. Преимущество в каждом конкретном случае отдается тому классу медикаментов, при использовании которого больной испытывает большее симптоматическое облегчение [3].
С другой стороны, авторы Кокрановского сотрудничества указывают на превосходство тиотропия бромида над классом длительно действующих β2 -агонистов (сальметерол, формотерол, индакатерол) в предупреждении обострений ХОБЛ (отношение шансов (ОШ) 0,86, 95% ДИ 0,79–0,93), госпитализаций, связанных с обострением ХОБЛ (ОШ 0,87; 95% ДИ 0,77–0,99), переносимости (частоте возникновения несмертельных побочных эффектов: ОШ 0,88; 95% ДИ 0,77–0,98) и уменьшении вероятности отказа пациентов от продолжения лечения (ОШ 0,89; 95% ДИ 0,81–0,99). Не выявлено различий между тиотропия бромидом и длительно действующими β2-агонистами во влиянии на смертность, частоту госпитализаций по любой причине, динамику ОФВ1 и симптомы ХОБЛ. Такие результаты были получены при анализе данных о более 12 тыс. пациентов, принимавших участие в 7 исследованиях, причем тиотропия бромид во всех из них применяли в виде порошкового ингалятора [4].
Кроме того, тиотропия бромид превосходил сальметерол во всех 6 фармакоэкономических исследованиях, выполненных в учреждениях по оказанию первичной и вторичной медицинской помощи в странах Европы (Великобритания, Нидерланды, Греция) и Америки (США) – как с точки зрения клинических исходов (обострения ХОБЛ, качество жизни), так и расходов на лечение.
Авторы не смогли проанализировать сведения о влиянии изученных препаратов на качество жизни из-за неоднородности полученных результатов, которые во многом зависели от того, с каким именно длительно действующим β2-агонистом (сальметерол, формотерол или индакатерол) сравнивался тиотропия бромид. Вероятно, различия, между антихолинергическими средствами и β2-агонистами отсутствуют или невелики. На это косвенно указывают результаты, полученные авторами другого Кокрановского обзора (рис. 3) [5].
Остается неясной и целесообразность сочетанного использования комбинации длительно действующих антихолинергических средств и β2-агонистов. Добавление последних к тиотропия бромиду ассоциируется с некоторым улучшением качества жизни, однако клиническое значение этого обстоятельства сомнительно (по крайней мере, разница в снижении показателей опросника SGRQ была в 2,5 раза меньше той, которая признается клинически значимой). Различий же в других первичных исходах (смертность, частота госпитализаций) не было вовсе [6].
Рис. 3.
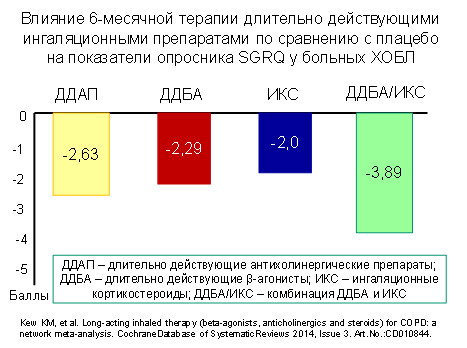
Среди вторичных исходов различия в пользу комбинации установлены только в приросте ОФВ1 (в среднем на 70 мл), однако это более чем в 2 раза меньше клинически значимой разницы. Частота обострений ХОБЛ, динамика симптомов, тяжелые побочные эффекты, частота отказов от продолжения лечения в обеих группах не различались.
Нет ответа и на обратный вопрос: насколько разумно добавлять тиотропия бромид к длительно действующему β2-агонисту? Прежде всего, из-за недостатка подобных исследований.
Таким образом, при декларируемом авторами программы GOLD «равноправии» длительно действующих антихолинергических средств и β2-агонистов выбор тиотропия бромида ассоциируется со снижением риска обострений ХОБЛ, госпитализаций в связи с обострениями и лучшей переносимостью. Оба класса медикаментов приводят к улучшению качества жизни больных, хотя это обстоятельство имеет скорее статистическое, нежели клиническое значение.
Безопасность
1. Влияние на смертность
Совершенствование способов доставки тиотропия бромида в дыхательные пути привело к созданию и внедрению в клиническую практику жидкостных ингаляторов, при использовании которых разовая доза препарата (5 мкг) в 3,5 раза меньше той, что используется в порошковом ингаляторе (18 мкг) – при сопоставимом клиническом эффекте. Однако вскоре стали появляться публикации, связывавшие прием тиотропия бромида через жидкостный ингалятор с повышением смертности от всех причин у больных ХОБЛ (примерно в 1,5 раза) [7]. В 2012 г. авторы Кокрановского сотрудничества, используя другую методологию, но проанализировав те же самые исследования, подтвердили увеличение смертности при использовании жидкостных ингаляторов тиотропия бромида (ОШ 1,47; 95% ДИ 1,04–2,08). С другой стороны, никакого риска возрастания смертности при использовании порошковых ингаляторов препарата установлено не было (ОШ 0,92; 95% ДИ 0,80–1,05) [1].
Наконец, еще в одной работе сравнили влияние разных классов медикаментов (длительность приема – не менее 6 мес.) на смертность от всех и от сердечно-сосудистых причин у пациентов с ХОБЛ. Оказалось, что при использовании жидкостного ингалятора тиотропия бромида риск смертности от всех причин возрастал по сравнению с плацебо (примерно в 1,5 раза) и другими классами медикаментов для лечения ХОБЛ (длительно действующие β2-агонисты в комбинации с ингаляционными кортикостероидами или без них). Кроме того, риск смерти при введении тиотропия бромида с помощью жидкостного ингалятора был выше, чем при использовании порошкового ингалятора (ОШ 1,65; 95% ДИ 1,13 – 2,43) [8].
Появление этих исследований, выполненных с помощью разных методик, вызвало широкую дискуссию о допустимости использования жидкостного ингалятора для введения тиотропия бромида [9, 10]. В этой связи следует вспомнить очень взвешенный комментарий экспертов FDA (Комиссия по оценке качества продуктов питания и лекарственных средств США) по затронутой проблеме: «Мы вступили в эру чрезвычайно частых публикаций мета-анализов; некоторые из них сигнализируют о возможных проблемах с безопасностью. Такие публикации обычно влекут за собой настойчивые призывы немедленно предпринять регуляторные действия – без признания возможных просчетов в интерпретации данных, полученных в ходе мета- и объединенных анализов, как это произошло при оценке тиотропия бромида. Нам следует проявлять дозированную сдержанность в наших оценках, чтобы гарантировать, что безопасное лекарство остается на рынке и что его использование не ограничивается таким образом, когда отказываются от полезных вмешательств у больных, в них нуждающихся. Продолжающаяся оценка сообщений по безопасности в FDA требует анализа всех доступных данных, полученных из многих источников, для достижения правильных выводов и таким путем, который понятен врачам и пациентам» [11]. Однако на момент публикации вопрос о безопасности жидкостного ингалятора тиотропия бромида оставался нерешенным и требовал дальнейшего изучения.
Прежде всего, следует отметить, что повышенный риск смертности приписывали не самому медикаменту, а лишь одному из способов его доставки в легкие – жидкостному ингалятору. При этом порошковые ингаляторы признавались вполне безопасными. Крупные рандомизированные контролируемые исследования обычно предназначены (и обладают для этого достаточной мощностью) для выяснения эффективности того или иного вмешательства, значимого для клиницистов, больных и регуляторных органов. Когда же эффективность установлена, но появились вопросы по безопасности, мощность доступных исследований обычно недостаточна, а специально спланированные для оценки безопасности организуются редко. Поэтому вполне логичным было провести прямое сравнение безопасности обоих ингаляторов тиотропия бромида в популяции пациентов, сопоставимой с ранее включавшимися в исследования больными.
В такое исследование (TIOSPIR) было включено 17135 пациентов с ХОБЛ. Тиотропия бромид назначали 1 раз сутки по 2,5 мкг и 5 мкг через жидкостный ингалятор или 18 мкг через порошковый ингалятор. Медиана продолжительности наблюдения составила 835 дней. Ни в сроках наступления смерти (рис. 4), ни во времени до наступления первого обострения ХОБЛ (рис. 5) различий между тремя сравниваемыми группами не было [12]. У больных с анамнестическими указаниями на нарушения ритма смертность во всех трех группах была сопоставимой, равно как и частота тяжелых сердечно-сосудистых событий.
Рис. 4.
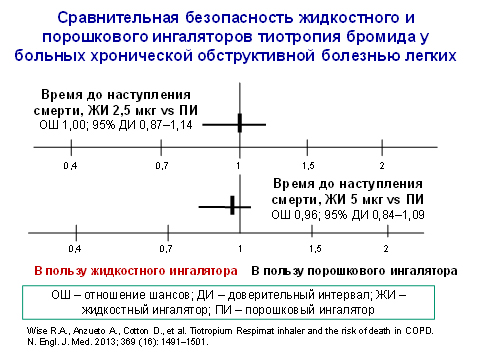
Таким образом, подтверждена сходная эффективность и безопасность разных ингаляторов для введения тиотропия бромида. В исследование TIOSPIR включали больных, отражающих реальную клиническую практику, то есть с сопутствующими заболеваниями, в том числе сердечно-сосудистыми, продолжавших прием медикаментов, выписанных по поводу коморбидных болезней, и др. Однако сделать вывод о том, что тиотропия бромид снижает смертность у больных ХОБЛ, исходя из полученных данных нельзя – в связи с отсутствием группы плацебо в этом исследовании [13].
Рис. 5.
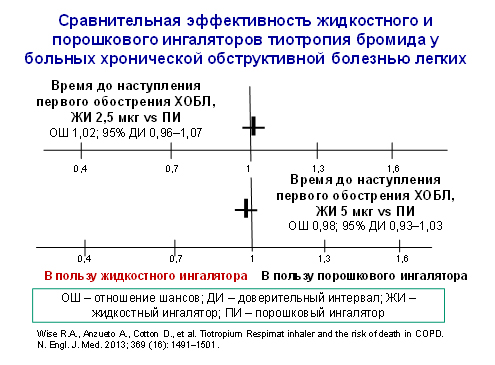
Наконец, уже в этом году опубликована работа, в которой проанализированы данные по безопасности введения тиотропия бромида у больных ХОБЛ с помощью порошковых (по 18 мкг 1 раз в сутки) и жидкостных ингаляторов (по 5 мкг 1 раз в сутки) – как вместе, так и раздельно. В ней систематизированы данные 28 исследований с порошковым ингалятором и 7 исследований – с жидкостным. Все клинические исследования длительностью ≥ 4 недель были рандомизированными, двойными слепыми, плацебо-контролируемыми, с параллельными группами. Общее количество больных составило 24555 человек (средний возраст 65 лет, средний ОФВ 1 – 41% от должного). Полученные данные свидетельствуют об отсутствии повышенного риска смерти от всех причин как в случае применения тиотропия бромида вообще (относительный риск (ОР) по сравнению с плацебо 0,90; 95% ДИ 0,79–1,01), так и при использовании порошкового (ОР 0,85; 95% ДИ 0,75–0,97) или жидкостного ингалятора (ОР 1,37; 95% ДИ 0,93 – 2,00) [14]. Напротив, количество умерших пациентов среди принимавших тиотропия бромид было меньшим, чем в группе плацебо, хотя различия и не достигли статистической значимости.
Таким образом, тиотропия бромид не влияет на смертность у больных ХОБЛ. Не подтвердились и опасения, что введение препарата с помощью жидкостного ингалятора оказывает негативное влияние на общую смертность.
2. Другие побочные эффекты
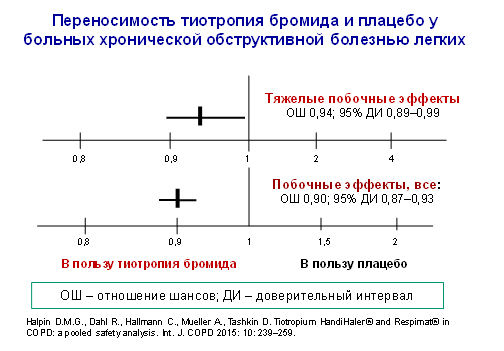
Хорошая переносимость тиотропия бромида документируется меньшим – по сравнению с плацебо! – числом как побочных эффектов вообще, так и тяжелых побочных эффектов (рис. 6).
Как и любой другой антихолинергический препарат, тиотропия бромид ассоциируется с повышенным риском нежелательных лекарственных явлений, обусловленных его механизмом действия. Среди них чаще всего отмечается сухость во рту (4% в группе вмешательства и 1,7% – в группе плацебо, ОР 2,35; 95% ДИ 1,99–2,77). Некоторые другие побочные эффекты (например, дизурия, запор) также встречаются чаще при приеме тиотропия бромида, но регистрируются существенно реже, чем сухость во рту.
Таким образом, учитывая сопоставимую эффективность и безопасность тиотропия бромида у больных ХОБЛ при использовании различных средств доставки, врачи вправе выбирать любую из них – в зависимости от доступности, собственных предпочтений и предпочтений пациента.
Рис. 6.
Место тиотропия бромида в современной терапии ХОБЛ
У больных группы А (мало симптомов, низкий риск обострений ХОБЛ) тиотропия бромид рассматривается в качестве одной из альтернатив короткодействующим бронходилататорам [3]. По-видимому, наибольшую пользу от использования препарата у пациентов данной группы можно ожидать у курящих людей, лиц с эмфиземой и с частично обратимой бронхообструкцией [15]. По согласованному мнению итальянских специалистов, регулярное лечение длительно действующими бронходилататорами (включая тиотропия бромид) при бронхиальной обструкции следует начинать как при наличии, так и в отсутствие симптомов ХОБЛ [16].
У больных группы В (много симптомов, низкий риск обострений ХОБЛ) длительно действующие антихолинергические средства и β2-агонисты являются препаратами выбора [3]. Аргументы в пользу предпочтения тиотропия бромида заключаются в 1) меньшем риске обострений ХОБЛ, 2) госпитализаций в связи с обострениями, 3) лучшей переносимости и 4) (вероятно) меньшей стоимости лечения. Первые два аргумента у пациентов данной группы не играют существенной роли (поскольку и так риск обострений невелик), четвертый предстоит еще изучить непосредственно в условиях Казахстана, а вот третий действительно важен. Можно ожидать, что лучшая переносимость тиотропия бромида проявится и большей приверженностью больных к лечению, и продолжительным «постоянством» (т.е. промежутком времени от начала до прекращения лечения) [17].
У больных группы С (мало симптомов, высокий риск обострений ХОБЛ) выбор лежит между фиксированной комбинацией ингаляционного кортикостероида (ИКС)/длительно действующего β2-агониста и длительно действующими антихолинергическими средствами. Поскольку прямое сравнение между представленными режимами терапии было проведено всего лишь единожды, сделать обоснованное заключение в чью-либо пользу затруднительно. Среди возможных альтернатив рассматривается и комбинация ИКС с длительно действующим антихолинергическим средством. Ограниченность доказательной базы в пользу такой комбинации, по мнению авторов программы GOLD, обусловлена скорее отсутствием должного интереса со стороны фармацевтических компаний, нежели сомнениями в ее разумности [3].
У больных группы D (много симптомов, высокий риск обострений ХОБЛ) тиотропия бромид в качестве препарата выбора используется в комбинации с ИКС (как альтернатива комбинации ИКС и длительно действующего β2-агониста), либо в сочетании с ИКС и длительно действующим β2-агонистом [3].
Перспективы применения титропия бромида для лечения больных бронхиальной астмой
Для обоснования использования длительно действующих антихолинергических средств в терапии БА существует множество патофизиологических наблюдений разной степени убедительности. Вот только некоторые из них:
· холинергическая активность – ключевая причина обратимой обструкции дыхательных путей при БА;
· холинергическая активность, вероятно, играет важнейшую роль в ремоделировании гладких мышц дыхательных путей;
· у больных БА, по-видимому, в результате возрастания холинергической активности, исходно повышен тонус гладких мышц дыхательных путей;
· лечение антихолинергическими препаратами снижает базальный тонус гладких мышц дыхательных путей;
· холинергические рецепторы в подслизистых клетках легких регулируют секрецию слизи;
· антагонисты холинорецепторов, возможно, оказывают не-нейрональное противовоспалительное действие [18].
Результаты проведенных к настоящему времени исследований тиотропия бромида у больных БА позволили документировать:
· значительное улучшение функции легких при добавлении к ИКС при среднетяжелой астме и к комбинации ИКС с длительно действующим β2-агонистом при тяжелой астме;
· значительное снижение риска обострений БА при добавлении к комбинации ИКС с длительно действующим β2-агонистом при тяжелой астме;
· незначительное улучшение контроля над симптомами БА и качества жизни со снижением потребления медикаментов «по требованию» у больных с сочетанием БА и ХОБЛ [19, 20];
· в условиях реальной клинической практики – значительное снижение частоты обострений БА и выписки антибиотиков по поводу инфекций нижних дыхательных путей в предшествующий год [21].
Хотя авторы Кокрановского обзора не нашли убедительных оснований для замены длительно действующих β2-агонистов на тиотропия бромид в качестве дополнения к ИКС у пациентов с БА [22], в недавнем обновлении рекомендаций Всемирной стратегии по лечению и профилактике бронхиальной астмы (GINA, май 2015 г.) тиотропия бромид, доставляемый при помощи жидкостного ингалятора, включен в качестве дополнительной возможности для лечения на 4 и 5 ступенях у больных ≥ 18 лет с анамнестическими указаниями на обострения заболевания (уровень доказательства В) [23]. Хотя подобная возможность рассматривалась и в прежних обновлениях GINA, только в этом году – после соответствующего регуляторного одобрения – тиотропия бромид был включен в схему ступенчатой терапии.
Заключение
Длительно действующий антихолинергический препарат тиотропия бромид применяется ингаляционно с помощью двух доставочных устройств – порошкового и жидкостного ингаляторов. На протяжении более десяти лет тиотропия бромид является неотъемлемой частью врачебного арсенала для лечения стабильной ХОБЛ на любом этапе эволюции заболевания. Эффективность и безопасность препарата подтверждены в многочисленных сравнительных клинических исследованиях. В 2015 г. в качестве дополнительной возможности у больных ≥ 18 лет он включен в схему ступенчатой терапии БА на 4 и 5 ступенях.
Список литературы:
1. Karner C., Chong J., Poole P. Tiotropium versus placebo for chronic obstructive pulmonary disease. Cochrane Database of Systematic Reviews 2014, Issue 7. Art. No.: CD009285.
2. Cheyne L., Irvin-Sellers M.J., White J. Tiotropium versus ipratropium bromide for chronic obstructive pulmonary disease. Cochrane Database of Systematic Reviews 2013, Issue 9. Art. No.: CD009552.
3. Global initiative for chronic obstructive lung disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease (updated 2015). 2015/ Доступно по адресу: www.goldcopd.org/uploads/users/files/GOLD_Report_2015.pdf
4. Chong J, Karner C, Poole P. Tiotropium versus long-acting beta-agonists for stable chronic obstructive pulmonary disease. Cochrane Database of Systematic Reviews 2012, Issue 9. Art. No.: CD009157.
5. Kew KM, et al. Long-acting inhaled therapy (beta-agonists, anticholinergics and steroids) for COPD: a network meta-analysis. CochraneDatabase of SystematicReviews 2014, Issue 3. Art.No.:CD010844.
6. Karner C, Cates CJ. Long-acting beta2-agonist in addition to tiotropium versus either tiotropium or long-acting beta2-agonist alone for chronic obstructive pulmonary disease. Cochrane Database of Systematic Reviews 2012, Issue 4. Art. No.: CD008989.
7. Cates C.J. Safety of tiotropium. BMJ 2011; 342: d2970.
8. Dong Y.H., Lin H.H., Shau W.Y., et al. Comparative safety of inhaled medications in patients with chronic obstructive pulmonary disease: systematic review and mixed treatment comparison meta-analysis of randomized controlled trials. Thorax 2013; 68: 48–56.
9. Beasley R. Tiotropium Respimat increases the risk of mortality: pro. Eur. Respir. J. 2013; 42: 584–589.
10. Bateman E.D. Tiotropium Respimat increases the risk of mortality: con. Eur. Respir. J. 2013; 42: 590–593.
11. Michele T.M., Pinheiro S., Iyasu S. The safety of tiotropium – the FDA’s conclusions. N. Engl. J. Med. 2010; 363: 1097–1099.
12. Wise R.A., Anzueto A., Cotton D., et al. Tiotropium Respimat inhaler and the risk of death in COPD. N. Engl. J. Med. 2013; 369 (16): 1491–1501.
13. Jenkins C.R. More than just reassurance on tiotropium safety. N. Engl. J. Med. 2013; 369 (16): 1555–1556.
14. Halpin D.M.G., Dahl R., Hallmann C., Mueller A., Tashkin D. Tiotropium HandiHaler® and Respimat® in COPD: a pooled safety analysis. Int. J. COPD 2015: 10: 239–259.
15. Cazzola M., Page C. Long-acting bronchodilators in COPD: where are we now and where are we going? Breathe 2014; 10 (2): 111–120.
16. Cazzola M., Brusasco V., Centanni S., et al. Project PriMo: sharing principles and practices of bronchodilator therapy monitoring in COPD: a consensus initiative for optimizing therapeutic appropriateness among Italian specialists. Pulm. Pharmacol. Ther. 2013; 26: 218–228.
17. Cramer JA, Roy A, Burrell A, et al. Medication compliance and persistence: terminology and definitions. Value Health. 2008; 11 (1): 44–47.
18. Price D., Fromer L., Kaplan A., van der Molen T., Román-Rodríguez M. Is there a rationale and role for long-acting anticholinergic bronchodilators in asthma? NPJ Primary Care Respiratory Medicine 2014; 24: 14023.
19. Novelli F., Costa F., Latorre M., et al. Tiotropium: a new therapeutic option in asthma. Monaldi Arch. Chest Dis. 2013; 79 (3-4): 109-115.
20. Befekadu E., Onofrei C., Colice G.L. Tiotropium in asthma: a systematic review. J. Asthma Allergy 2014; 7: 11–21.
21. Price D., Kaplan A., Jones R., et al. Long-acting muscarinic antagonist use in adults with asthma: real-life prescribing and outcomes of add-on therapy with tiotropium bromide. J. Asthma Allergy 2015; 8: 1–13.
22. Kew K.M., Evans D.J.W., Allison D.E., Boyter A.C. Long-acting muscarinic antagonists (LAMA) added to inhaled corticosteroids (ICS) versus addition of long-acting beta2-agonists (LABA) for adults with asthma. Cochrane Database of Systematic Reviews 2015, Issue 6. Art. No.: CD011438.
23. Global Initiative for Asthma (GINA). Global strategy for asthma management and prevention. 2015. 132 р. Доступно на сайте www.ginasthma.org







