Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "Антибактериальная терапия острого среднего отита"
Автор: И.Г. Березняков
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: ЛОР, Семейная медицина/Терапия
Просмотров: 3 057
Дата проведения:
Введение
Острый средний отит (ОСО) – это инфекционное заболевание среднего уха. Особенно часто оно встречается у детей (пик заболеваемости приходится на возраст 6–15 мес.) [1]. Каждый десятый ребенок переболевает ОСО в первые 3 мес. жизни, а 50–85% детей переносят хотя бы один эпизод ОСО в возрасте до 3-х лет [2].
Заболеваемость ОСО у детей младше 5 лет в России составляет 27,2 случаев на 100 человеко-лет [3]. В той же возрастной категории аналогичный показатель в Новой Зеландии оказался равным 27%, а в исследовании, проведенном в 9 странах Европы, Южной Америки и Азии – в среднем 38% [4, 5].
 Чаще всего ОСО возникает вследствие острой респираторной вирусной инфекции [6], которая обусловливает воспаление или отек евстахиевой трубы, создание отрицательного давления в среднем ухе и перемещение секрета, содержащего возбудителей респираторной инфекции и патогенные бактерии, из носоглотки в барабанную полость.
Чаще всего ОСО возникает вследствие острой респираторной вирусной инфекции [6], которая обусловливает воспаление или отек евстахиевой трубы, создание отрицательного давления в среднем ухе и перемещение секрета, содержащего возбудителей респираторной инфекции и патогенные бактерии, из носоглотки в барабанную полость.
Этиология
При использовании современных чувствительных микробиологических методик обнаружить вирусы и бактерии в жидкости среднего уха у больных ОСО удается в подавляющем большинстве случаев. Так, в одном из недавних исследований микроорганизмы были выделены в 96% случаев (в 68% – бактерии и вирусы, в 27% – только бактерии, в 4% – только вирусы) [7]. Частота выделения бактерий зависит от критериев, применявшихся для верификации диагноза ОСО, оснащенности микробиологических лабораторий, транспортных средств, использованных для доставки материала в лабораторию. Если перечисленные условия приближаются к оптимальным, патогенные бактерии из экссудата среднего уха выделяются в 85–90% случаев – изолированно или вместе с вирусами [8–10].
Из бактерий ОСО чаще всего вызывают S. pneumoniae, нетипируемые штаммы H. influenzae и M. catarrhalis. На долю S. pyogenes (b-гемолитических стрептококков группы А) приходится менее 5% случаев ОСО [11]. Предсказать этиологию ОСО на основании только клинических признаков без культурального исследования жидкости среднего уха более чем затруднительно. В то же время, в отдельных клинических ситуациях такое предсказание имеет смысл. В частности, сочетание ОСО с конъюнктивитом (синдром отита-конъюнктивита) чаще вызывают нетипируемые штаммы H. influenzae, нежели другие бактерии [12, 13].
Естественное течение ОСО, вызванного разными бактериями, существенно различается. В ранних исследованиях у детей с ОСО, не получавших антибиотики, было показано, что в 19% заболеваний, вызванных S. pneumoniae, и в 48% – вызванных H. influenzae (микробиологический диагноз устанавливали при культуральном исследовании жидкости среднего уха, полученной в ходе первоначального тимпаноцентеза), указанные бактерии не обнаруживали во время повторных тимпаноцентезов 2–7 дней спустя [14]. Еще более демонстративные данные получены при заболеваниях, вызванных M. catarrhalis: при назначении амоксициллина бактериологическое излечение было документировано в 75% случаев – антибиотика, к которому эти бактерии нечувствительны из-за выработки b-лактамаз [15, 16].
Антибиотикорезистентность
 На постсоветском пространстве чувствительность бактерий к антибиотикам систематически изучали нечасто. Наиболее убедительные данные получены в Российской Федерации. Они не только позволяют оценивать тенденции в изменениях антибиотикочувствительности возбудителей внебольничных инфекций дыхательных путей, но и могут использоваться в качестве ориентиров врачами Казахстана и Украины.
На постсоветском пространстве чувствительность бактерий к антибиотикам систематически изучали нечасто. Наиболее убедительные данные получены в Российской Федерации. Они не только позволяют оценивать тенденции в изменениях антибиотикочувствительности возбудителей внебольничных инфекций дыхательных путей, но и могут использоваться в качестве ориентиров врачами Казахстана и Украины.
В целом, ситуация с чувствительностью пневмококков к амоксициллину достаточно благоприятная. Гемофильные палочки редко вырабатывают b-лактамазы и сохраняют высокую чувствительность к амоксициллину (с клавулановой кислотой или без нее). Практически все моракселлы продуцируют b-лактамазы, однако сохраняют очень высокую чувствительность в амоксициллину/клавуланату. У пиогенных стрептококков также сохраняется 100%-ная чувствительность к амоксициллину [17, 18].
Диагностика
Клинический диагноз ОСО ранее базировался на выявлении 3-х обстоятельств: 1) острое начало заболевания, 2) наличие выпота в среднем ухе и 3) признаки острого воспаления среднего уха [19]. Подобное определение подвергалось обоснованной критике, в частности, оно не позволяло провести дифференциальную диагностику ОСО с экссудативным средним отитом (отитом с выпотом). В 2013 г. Американская академия педиатров (ААП) уточнила критерии диагностики ОСО. Заболевание диагностируется у детей в следующих случаях:
- при наличии умеренного или выраженного выпячивания барабанной перепонки (БП) или вновь появившейся отореи, не вызванной острым наружным отитом;
- при наличии незначительного выпячивания БП и недавнего (менее 48 ч тому назад) начала болей в ухе (прижимания, потягивания, потирания уха неразговаривающими детьми) или интенсивного покраснения БП.
Если при проведении пневматической отоскопии и/или тимпанометрии отсутствует выпот в среднем ухе, диагноз ОСО детям не ставят [11].
Абсолютные показания к назначению антибиотиков при ОСО
 Антибиотики назначаются всем больным с ОСО:
Антибиотики назначаются всем больным с ОСО:
- в возрасте до 6 мес. – вне зависимости от точности диагноза и тяжести заболевания [20];
- если заболевание протекает с отореей (гноетечением) – при несомненном ОСО;
- при тяжелом течении болезни.
Под тяжелым течением ОСО (одно- или двустороннего) понимают среднетяжелую или тяжелую оталгию (боли в ушах), либо оталгию длительностью не менее 48 ч, или повышение температуры тела до 39° С и выше [11].
Антибиотики также назначаются всем детям в возрасте 6–24 мес. с нетяжелым двусторонним ОСО (незначительная оталгия длительностью до 48 ч, температура тела менее 39° С) [11].
Возможные показания к назначению антибиотиков при ОСО
Антибиотики могут назначаться:
- детям в возрасте 6–24 мес. с нетяжелым односторонним отитом;
- детям старше 2-х лет с нетяжелым двусторонним или односторонним ОСО [11].
Альтернативой антибактериальной терапии (АБТ) является лечение без антибиотиков и активное наблюдение за больным на протяжении 48–72 ч. Решение об активном наблюдении и лечении без антибиотиков согласовывается с родителями (родственниками, опекунами) ребенка. При ухудшении в любой момент состояния ребенка или отсутствии улучшения в указанные сроки назначается АБТ.
Срочная АБТ или активное наблюдение?
Итак, у детей с нетяжелым ОСО возможно использование двух технологий: срочной АБТ или активного наблюдения, вариантом которого является отложенное (отсроченное) назначение антибиотиков. Под срочной АБТ понимают назначение антибиотиков сразу после постановки диагноза и начало их приема сразу вслед за приобретением в аптеке. При активном наблюдении пациента вначале лечат при помощи симптоматических средств (анальгетики, жаропонижающие и др.) без использования антибиотиков. Рецепт же на приобретение антибиотиков выдается родителям (родственникам, опекунам) больного одновременно с предложением «отоварить» его в аптеке в случаях ухудшения в любое время или отсутствия улучшения на протяжении 48–72 ч, либо же рецепт на антибиотик будет доступен для пациента в приемном покое медицинского учреждения (либо у лечащего врача), но только в случае повторного обращения в связи с ухудшением или отсутствием улучшения.
 Основным аргументом в пользу допустимости активного наблюдения служит в целом благоприятное течение ОСО и высокая частота спонтанного выздоровления. По данным авторов Кокрановского сотрудничества, 60% детей, получавших плацебо в ходе рандомизированных клинических исследований (РКИ), выздоравливают в течение 24 ч от начала вмешательства (т.е. не испытывают болей). Через 2–3 дня от начала вмешательства их доля достигает уже 84% (рис. 1) [21]. Некоторое снижение доли выздоровевших пациентов в более поздние сроки наблюдения объясняется, скорее всего, недостаточной четкостью в постановке диагноза ОСО перед включением больных в РКИ (например, включение детей с симптомами острой респираторной вирусной инфекции, но без отита), но, в любом случае, остается очень высокой.
Основным аргументом в пользу допустимости активного наблюдения служит в целом благоприятное течение ОСО и высокая частота спонтанного выздоровления. По данным авторов Кокрановского сотрудничества, 60% детей, получавших плацебо в ходе рандомизированных клинических исследований (РКИ), выздоравливают в течение 24 ч от начала вмешательства (т.е. не испытывают болей). Через 2–3 дня от начала вмешательства их доля достигает уже 84% (рис. 1) [21]. Некоторое снижение доли выздоровевших пациентов в более поздние сроки наблюдения объясняется, скорее всего, недостаточной четкостью в постановке диагноза ОСО перед включением больных в РКИ (например, включение детей с симптомами острой респираторной вирусной инфекции, но без отита), но, в любом случае, остается очень высокой.
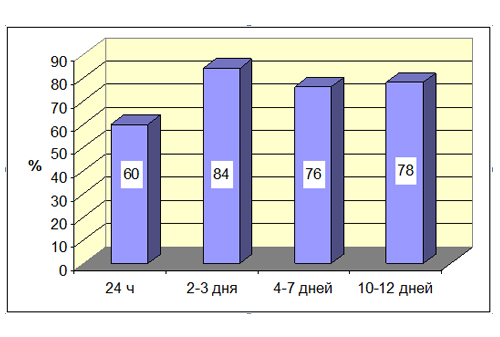
Рисунок 1. Частота спонтанного выздоровления детей с ОСО в разные сроки наблюдения
Следующий аргумент в пользу активного наблюдения – небольшая или умеренная польза от назначения антибиотиков. По данным авторов Кокрановского сотрудничества, антибиотики не увеличивают число выздоровевших больных с ОСО по сравнению с плацебо в первые сутки от начала лечения, однако в последующие дни польза от их использования несомненна (рис. 2). Это означает, что по сравнению с группой плацебо в группе детей, получающих антибиотики, на 2–3 сут. от начала вмешательства в среднем на 5% меньше больных будут испытывать боли, на 4–7 сут. – в среднем на 6%, а на 10–12 сут. – на 14% меньше. Кроме того, лечение антибиотиками примерно в 3 раза снижает риск перфорации БП и в 2 раза – возникновения контралатерального отита (при изначально одностороннем поражении, рис. 3).
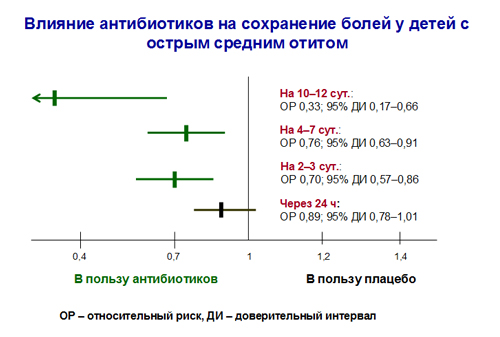
Рисунок 2.
Следует сразу оговориться, что в большинство проанализированных исследований не включали больных с тяжелым ОСО и пациентов с другими бактериальными инфекциями (пневмония, мастоидит, стрептококковый тонзиллофарингит). Поэтому истинная польза от назначения антибиотиков пациентам с ОСО в действительности может быть значительно выше, что, в частности, подтверждается в более поздних работах, выполненных с использованием жестких критериев постановки диагноза [22, 23].
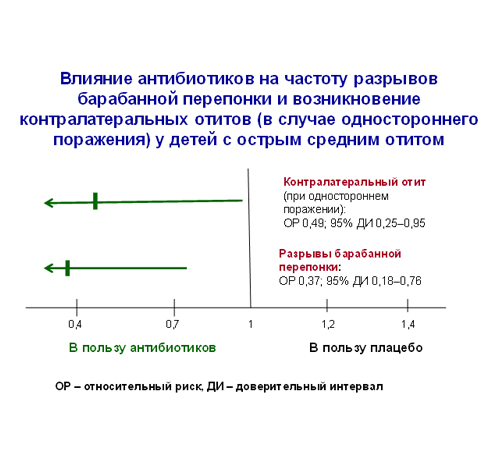
Рисунок 3.
Наконец, эффективность и безопасность активного наблюдения (с назначением антибиотиков спустя 48–72 ч или без него) подтверждена в ходе клинических исследований. Такой подход не уступал срочной АБТ по влиянию на сроки сохранения болей и при этом ассоциировался с лучшей переносимостью (рис. 4).
По сравнению со срочной АБТ активное наблюдение имеет ряд несомненных преимуществ. Это и снижение стоимости лечения, и снижение риска нежелательных лекарственных явлений, и снижение риска возникновения и распространения резистентности к антибиотикам. Наконец, допустимость и безопасность активного наблюдения за больными с ОСО подтверждена в клинических исследованиях. Тем не менее, решение о возможном лечении ребенка с ОСО без антибиотиков (или отсроченном их применении) лечащий врач должен согласовывать с родителями (родственниками или опекунами) пациента – после обсуждения достоинств и недостатков подобного подхода. В случае их отказа антибиотики следует назначить. Если же родители (родственники, опекуны) не возражают против лечения без антибиотиков, врачу следует учитывать возможность усугубления клинической симптоматики, а также развития инфекционных осложнений (мастоидит и др.). Если течение заболевания будет складываться неблагоприятно, антибиотики назначают незамедлительно.

Рисунок 4.
Наконец, надо быть «внутренне» готовым к тому, что в случаях усугубления клинической симптоматики или развития осложнений возрастает риск разного рода личностного, материального, административного, юридического, карьерного ущерба для врача. Личностного – значит быть готовым выслушать нелицеприятное мнение родителей (родственников, опекунов) о себе самом и о своей квалификации. Административного – получить «нагоняй» от своего руководителя (если будут жалобы). Юридического – отстаивать свою честь и достоинство в суде (если до этого дойдет дело). И так далее…
Какие категории детей с ОСО могут получить наибольшую пользу от АБТ?
На основании анализа индивидуальных данных в 6 РКИ выделены 2 группы пациентов с ОСО, которые могут получить наибольшую пользу от назначения антибиотиков. Во-первых, это дети в возрасте до 2-х лет с двусторонним отитом. Вероятность сохранения болей, лихорадки, или обоих симптомов на 3–7 сут. от начала лечения в группе получавших антибиотики была на 25% ниже, чем в группе плацебо. У детей ³ 2-х лет с двусторонним отитом, леченых антибиотиками, аналогичный показатель по сравнению с плацебо снижался только на 12%, что было статистически значимо меньше, чем у детей раннего возраста (< 2-х лет). Во-вторых, это дети с отореей (любого возраста), у которых вышеупомянутый показатель (т.е. боли, лихорадка, или оба симптома) в указанные сроки (на 3–7 сут. от начала лечения) снижался по сравнению с плацебо на 36%, а у детей без отореи – только на 14% (различия между группами опять-таки были статистически значимыми) [24].
Какие антибиотики назначать?
За некоторыми исключениями препарат выбора при лечении ОСО – амоксициллин. К исключениям относятся: 1) новорожденные; 2) лечение амоксициллином по любому поводу в предшествующие нынешнему заболеванию 30 дней; 3) сочетание ОСО с гнойным конъюнктивитом; 4) анамнестические указания на аллергию на пенициллин.
Выбор амоксициллина продиктован:
- высокой активностью в отношении ключевых возбудителей ОСО – пневмококков и не продуцирующих b-лактамазы гемофильных палочек;
- редкостью H. influenzae, вырабатывающих b-лактамазы, и благоприятным клиническим течением ОСО, вызванного M. catarrhalis, на которых амоксициллин не действует;
- доказанной эффективностью при лечении данного заболевания;
- безопасностью;
- приемлемыми вкусовыми свойствами (что немаловажно в педиатрической практике);
- невысокой стоимостью;
- сравнительно узким спектром микробиологической активности;
- отсутствием связи со временем приема пищи (препарат принимают независимо от еды).
Из всех лекарственных форм для приема амоксициллина внутрь (таблетки и капсулы, которые могут использоваться у детей старшего возраста, порошок для приготовления суспензии и др.) наиболее удобными являются диспергируемые таблетки амоксициллина. Их преимущества можно суммировать так:
- процесс растворения диспергируемой таблетки намного быстрее и проще приготовления суспензии из порошка амоксициллина;
- антибиотик, заключенный в кислотоустойчивые микрогранулы, не разрушается под действием желудочного сока и почти полностью всасывается в кишечнике;
- максимальная биодоступность препарата (93% по сравнению с 70–80% в лекарственных формах в обычных таблетках или капсулах) и, соответственно, минимальное нарушение микроэкологии кишечника;
- удобство приема (таблетка (или ее часть) растворяется в воде, либо проглатывается целиком);
- возможность визуально проконтролировать процесс растворения (таблетка быстро распадается на гранулы без выделения газа) и убедиться в подлинности препарата;
- приятные органолептические свойства (и, соответственно, меньший риск срыгивания, выплевывания антибиотика).
Доза амоксициллина определяется в зависимости от исходной тяжести заболевания. У детей с нетяжелым ОСО она составляет 45 мг/кг/сут. в 2 приема, у больных с тяжелым ОСО – увеличивается до 80–90 мг/кг/сут., также в 2 приема. Кроме того, высокие дозы амоксициллина могут назначаться детям с факторами риска инфицирования пенициллинорезистентными пневмококками:
1) возраст до 2 лет;
2) посещение яслей или детского садика;
3) частые ОСО в анамнезе и/или недавняя АБТ (в предшествующие 3 мес.).
У новорожденных вероятными возбудителями ОСО являются кишечная палочка (E. coli) и другие представители семейства Enterobacteriaceae. Препаратом выбора является цефотаксим, который назначают парентерально по 50 мг/кг 2–3 раза в сутки. Кратность дозирования определяется в зависимости от гестационного возраста и хронологического возраста пациента [25].
Если ребенок с ОСО получал лечение амоксициллином по любому поводу в предшествующие нынешнему заболеванию 30 дней, а также при сочетании ОСО с гнойным конъюнктивитом препаратом выбора становится амоксициллин/клавуланат. Кроме того, данный антибиотик назначают и при наличии рецидивов ОСО в анамнезе – с неубедительным эффектом от лечения амоксициллином [11].
Амоксициллин/клавуланат активен в отношении всех ключевых возбудителей ОСО, включая продуцентов b-лактамаз. Рекомендуемая доза (90 мг/кг/сут. по амоксициллину, 6,4 мг/кг/сут. по клавуланату – в 2 приема) готовится путем смешивания суспензий амоксициллина/клавуланата и амоксициллина в необходимых количествах. Такое соотношение амоксициллина и клавулановой кислоты (14:1), как полагают, реже вызывает диарею, чем другие лекарственные формы амоксициллина/клавуланата [11]. Кстати, амоксициллин/клавуланат, как и амоксициллин, выпускается в виде диспергируемых таблеток.
Альтернативами аминопенициллинам могут быть цефалоспорины для приема внутрь (цефуроксим аксетил по 30 мг/кг/сут. в 2 приема, цефподоксим проксетил по 10 мг/кг/сут. в 2 приема) или для парентерального введения (цефтриаксон по 50 мг/кг 1 раз в сутки внутримышечно или внутривенно). К недостаткам пероральных цефалоспоринов следует отнести неприятные вкусовые свойства суспензий, которые можно попытаться замаскировать ароматизаторами со вкусом шоколада или клубники. Если ребенок все равно отказывается принимать пероральный цефалоспорин (даже с замаскированным вкусом), можно прибегнуть к парентеральному введению цефтриаксона. Допускается лечение ОСО однократной инъекцией цефтриаксона, однако более надежным представляется 3-дневный курс лечения.
Какие антибиотики назначают при аллергии на пенициллин?
Представления о перекрестной аллергии на цефалоспорины у больных с повышенной чувствительностью к пенициллину преувеличены. Риск перекрестной реактивности определяется химической формулой цефалоспоринов и минимален между пенициллином и цефалоспоринами II (цефуроксим аксетил) и III поколения (цефподоксим проксетил, цефтриаксон). Они могут использоваться у больных с анамнестическими указаниями на аллергию на пенициллин, за исключением случаев тяжелых и (или) недавних аллергических реакций.
Из других альтернатив можно упомянуть макролиды и клиндамицин (суспензии которого отличаются неприятными вкусовыми свойствами).
Какова длительность антибактериальной терапии ОСО?
У детей в возрасте до 2 лет и при тяжелом течении ОСО у детей любого возраста длительность терапии составляет 10 дней. У больных в возрасте от 2 до 5 лет с нетяжелым ОСО антибиотики назначаются внутрь сроком на 7 дней. У детей 6 лет и старше с нетяжелым ОСО курс АБТ может быть короче – от 5 до 7 дней [11].
Приведенные рекомендации не распространяются на цефтриаксон (курс лечения – 1 или 3 дня) и азитромицин (курс лечения – 5 дней).
Сохранение выпота в среднем ухе после исчезновения всех симптомов ОСО и завершения курса АБТ – явление нередкое. Через 2 недели после успешного лечения ОСО антибиотиками выпот в среднем ухе обнаруживают у 60–70% детей, через 1 мес. – у 40%, а через 3 мес. – у 10–25% [26]. Наличие выпота в среднем ухе в отсутствие симптомов заболевания трактуется как экссудативный средний отит. Такие дети не нуждаются в лечении антибиотиками [11].
Что делать в случае неэффективности стартовой антибактериальной терапии?
В первые 24 ч после постановки диагноза ОСО и назначения антибиотиков симптомы заболевания могут незначительно ухудшиться. На следующие сутки симптоматика начинает улучшаться. Исходно повышенная температура тела должна снижаться в ближайшие 48–72 ч от начала АБТ, нормализуются сон и аппетит. При отсутствии улучшения в течение 48–72 ч стартовая АБТ расценивается как неэффективная.
Если ребенка начинали лечить амоксициллином, следует назначить амоксициллин/клавуланат. В случаях, когда стартовыми антибиотиками были амоксициллин/клавуланат или пероральные цефалоспорины, можно прибегнуть к парентеральному введению цефтриаксона по 50 мг/кг 1 раз в сутки; длительность курса лечения – 3 дня.
ОСО у взрослых
В связи с редкостью заболевания у взрослых людей предложения по его лечению антибиотиками во многом опираются на соответствующие рекомендации у детей. В отсутствие факторов риска антибиотикорезистентности при ОСО разной степени тяжести препаратом выбора остается амоксициллин, который назначают внутрь в дозе 0,5–1,0 г 2–3 раза в сутки. Если же в предшествующие 6 недель больной принимал антибиотики (по любому поводу), а также при неэффективности стартовой терапии препаратом выбора назначают амоксициллин/клавуланат внутрь по 0,625 г 3 раза в сутки или по 1,0 г 2 раза в сутки.
Литература
- Klein J.O. Epidemiology of otitis media. Infect. Dis. J. 1989; 8 (Suppl 1): 89.
- Teele D.W., Klein J.O., Rosner B. Epidemiology of otitis media during first seven years of life in children in greater Boston: a prospective cohort study. J. Infect. Dis. 1989; 160: 83–94.
- Козлов Р.С., Кречикова О.И., Муравьев А.А., с соавт. Результаты исследования распространенности в России внебольничной пневмонии и острого среднего отита у детей в возрасте до 5 лет (PAPIRUS). Роль S. pneumoniae и H. influenzae в этиологии этих заболеваний. Клин. микробиол. антимикроб. химиотер. 2013; 15 (4): 247–260.
- Gribben B., Salkeld L.J., Hoare S., Jones H.F. The incidence of acute otitis media in New Zealand children under five years of age in the primary care setting. Prim. Health Care 2012; 4 (3): 205-12.
- Arguedas A., Kvaerner K., Liese J., et al. Otitis media across nine countries: disease burden and management. Int. J. Pediatr. Otorhinolaryngol. 2010; 74 (12): 1419-24.
- Klein J.O., Bluestone C.D. Otitis media. In: Feigin R.D., Cherry J.D., Demmler-Harrison G.J., Kaplan S.L., eds. Textbook of pediatric infectious diseases. 6th ed. Philadelphia, PA: Saunders; 2009:216–237.
- Ruohola A., Meurman O., Nikkari S., et al. Microbiology of acute otitis media in children with tympanostomy tubes: prevalences of bacteria and viruses. Clin. Infect. Dis. 2006; 43 (11): 1417–1422.
- Del Beccaro M.A., Mendelman P.M., Inglis A.F., et al. Bacteriology of acute otitis media: a new perspective. J. Pediatr. 1992; 120 (1): 81–84ю
- Block S.L., Harrison C.J., Hedrick J.A., et al. Penicillin-resistant Streptococcus pneumoniae in acute otitis media: risk factors, susceptibility patterns and antimicrobial management. Pediatr. Infect. Dis. J. 1995; 14 (9): 751–759.
- Rodriguez W.J., Schwartz R.H. Streptococcus pneumoniae causes otitis media with higher fever and more redness of tympanic membranes than Haemophilus influenzae or Moraxella catarrhalis. Infect. Dis. J. 1999; 18 (10): 942–944.
- Lieberthal A.S., Carroll A.E., Chonmaitree T., et al. The diagnosis and management of acute otitis media. Pediatrics 2013; 131: e964–e999.
- Bingen E., Cohen R., Jourenkova N., Gehanno P. Epidemiologic study of conjunctivitis-otitis syndrome. Pediatr. Infect. Dis. 2005; 24 (8): 731–732.
- Barkai G., Leibovitz E., Givon-Lavi N., Dagan R. Potential contribution by nontypable Haemophilus influenzae in protracted and recurrent acute otitis media. Pediatr. Infect. Dis J. 2009; 28 (6): 466–471.
- Howie V.M., Ploussard J.H. Efficacy of fixed combination antibiotics versus separate components in otitis media. Effectiveness of erythromycin estrolate, triple sulfonamide, ampicillin, erythromycin estolate-triple sulfonamide, and placebo in 280 patients with acute otitis media under two and one-half years of age. Clin. Pediatr. (Phila). 1972; 11 (4): 205–214.
- Klein J.O. Microbiologic efficacy of antibacterial drugs for acute otitis media. Pediatr. Infect. Dis. 1993; 12 (12): 973–975.
- Barnett E.D., Klein J.O. The problem of resistant bacteria for the management of acute otitis media. Pediatr. Clin. North Am. 1995; 42 (3): 509–517.
- Азовскова О.В., с соавт., исследовательская группа «ПеГАС». Динамика антибиотикорезистентности респираторных штаммов Streptococcus pyogenes в России за период 1999–2009 гг. Клин. микробиол. антимикроб. химиотер. 2012; 14 (4): 309-21.
- American Academy of Pediatrics Subcommittee on Management of Acute Otitis Media. Diagnosis and management of acute otitis media. Pediatrics. 2004; 113 (5): 1451–1465.
- Применение антибиотиков у детей в амбулаторной практике. Практические рекомендации. Под ред. Баранова А.А., Страчунского Л.С. Клин. микробиол. антимикроб. химиотер. 2007; 9 (3): 200–210.
- Venekamp R.P., Sanders S.L., Glasziou P.P., et al. Antibiotics for acute otitis media in children. Cochrane Database of Systematic Reviews 2015, Issue 6. Art. No.: CD000219.
- Hoberman A., Paradise J.L., Rockette H.E., et al. Treatment of acute otitis media in children under 2 years of age. N. Engl. J. Med. 2011; 364 (2): 105–115.
- Tahtinen P.A., Laine M.K., Huovinen P., et al. A placebo-controlled trial of antimicrobial treatment for acute otitis media. N. Engl. J. 2011; 364 (2): 116–126.
- Rovers M.M., Glasziou P., Appelman C.L., et al. Antibiotics for acute otitis media: a meta-analysis with individual patient data. Lancet 2006; 368: 1429–35.
- Березняков И.Г. Краткий справочник по эмпирическому использованию антибиотиков с лечебной и профилактической целью. Киев: Корпорация Артериум, 2014: 86–87.
- Rosenfeld R.M., Kay D. Natural history of untreated otitis media. In: Rosenfeld R.M., Bluestone C.D., eds. Evidence-Based Otitis Media. 2nd ed. Hamilton, Canada: BC Decker; 2003:180–198.






