Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "Хроническое обструктивное заболевание легких: эпидемиология, патофизиология, клиника, диагностика и лечение"
Автор: И.И.Вишнивецкий, А.И. Дядык
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Пульмонология, Семейная медицина/Терапия
Просмотров: 3 190
Дата проведения: с 15.09.2014 по 15.09.2015
Хроническое обструктивное заболевание легких (ХОБЛ) является серьезной медицинской и социальной проблемой, являясь одной из ведущих причин снижения качества жизни и работоспособности, инвалидизации и летальности.
В 2011 году комитет GOLD (Global Іnitiative for Obstructive Lung Disease – Глобальная инициатива по обструктивному заболеванию легких) – «Глобальная стратегия диагностики, лечения и профилактики ХОБЛ» («Global Strategy for Diagnosis, Management, and Prevention of COPD») издал новый, существенно переработанный, вариант клинических рекомендаций, в которых отражены вопросы классификации, диагностики, клиники, лечения и профилактики ХОБЛ. В последующие годы данные рекомендации были уточнены и дополнены, однако ключевые положения остались неизменными. Настоящее сообщение базируется на редакции рекомендаций GOLD 2014 года.
Определение. ХОБЛ – распространенное, поддающееся профилактике и лечению заболевание, которое характеризуется персистирующим ограничением проходимости дыхательных путей (обычно прогрессирующим) и связано с повышенным хроническим воспалительным ответом в дыхательных путях и легких на действие вредных частичек или газов. Наличие частых обострений и сопутствующих заболеваний оказывает существенное влияние на тяжесть заболевании и прогноз.
Распространенность. ХОБЛ характеризуется широкой распространенностью. По данным масштабного мета-анализа, его распространенность в мире составляет в среднем 7,6%, в Европе – 7,4%. Заболевание наблюдается значительно чаще у курильщиков и бывших курильщиков, чем у некурящих; у лиц старше 40 лет по сравнению с более молодыми; чаще у мужчин, чем у женщин; среди городских жителей почти вдвое чаще, чем у жителей сельской местности. Повсеместно отмечается низкий уровень качества диагностики ХОБЛ. Так, по данным популяционных скрининговых исследований, среди лиц с выявленным впервые ХОБЛ только у 20% этот диагноз был поставлен ранее.
Морбидность и летальность. При оценке морбидности традиционно учитываются качество жизни, количество обращений к врачу и госпитализаций по поводу обострений заболевания, а также изменения лечебного режима. В большинстве стран число обращений к врачу по поводу ХОБЛ намного превосходит таковое по поводу бронхиальной астмы, пневмонии, рака легких и туберкулеза. На показатели морбидности при ХОБЛ могут влиять сопутствующие хронические заболевания (например, сердечно-сосудистые заболевания, болезни опорно-двигательного аппарата, сахарный диабет, тревожно-депрессивные расстройства).
ХОБЛ ассоциируется с высоким риском смертности. На протяжении последних 30 лет отмечен неуклонный рост летальных исходов, обусловленных ХОБЛ. По прогнозам экспертов ВОЗ к 2030 году ХОБЛ будет занимать 4-е место среди других причин летальности.
Социально-экономическое значение. ХОБЛ обусловливает высокие финансовые затраты – как прямые (бюджетные ресурсы системы здравоохранения для обеспечения диагностики и лечения), так и непрямые (экономические потери вследствие инвалидизации, больничных листов, преждевременной смертности, дополнительные затраты семей, ухаживающих за больным). В Европейском союзе общие прямые затраты на болезни органов дыхания составляют примерно 6% всего бюджета здравоохранения, среди которых на ХОБЛ приходится 56%.
Этиология, патоморфология, патофизиология.
К факторам риска развития ХОБЛ относят:
- активное и пассивное курение (главный фактор!);
- длительное воздействие профессиональных или бытовых (загрязнение атмосферного воздуха, продукты сгорания топлива) поллютантов на дыхательные пути;
- возраст старше 40 лет;
- частые респираторные инфекции;
- нарушение развития легких в раннем возрасте;
- наследственная предрасположенность (в т. ч. генетически детерминированный дефицит α1-антитрипсина).
Эпидемиологические исследования подтверждают, что активное курение табака является важнейшим фактором риска развития ХОБЛ. Если пациент курит или курил ранее, необходимо оценить интенсивность курения (стаж курения, количество сигарет в день) и рассчитать индекс курения (ИК):
ИК (пачек-лет) = [количество сигарет в день × стаж курения (годы)] / 20
Например, при курении 1 пачки (20 сигарет) в день в течение 10 лет или 0,5 пачки (10 сигарет) в течение 20 лет ИК составляет 10 пачек-лет. ИК более 10 пачек-лет является общепризнанным важным фактором риска ХОБЛ. Следует отметить, что большинство пациентов с ХОБЛ обычно имеет ИК более 20-30 пачек-лет.
Примерно в 25% случаев развитие ХОБЛ обусловлено другими ингаляционными агрессивными факторами (профессиональными, экологическими, бытовыми и др.). Риск развития ХОБЛ повышается у лиц старшего возраста. При сочетании этих факторов (интенсивного курения и возраста старше 40-50 лет) риск развития ХОБЛ достигает 85%.
Сигаретный дым или другие ингаляционные агрессивные факторы вызывают воспаление в легких, что является нормальным защитным ответом организма. В то же время, этот ответ приобретает патологический характер у лиц, склонных к развитию ХОБЛ. Механизмы такого воспалительного ответа остаются малоизученными, но могут быть генетически детерминированы. В качестве основных механизмов развития ХОБЛ рассматриваются оксидативный стресс и нарушенный баланс протеиназ и антипротеиназ в легких. Оксиданты, генерируемые сигаретным дымом или другими выдыхаемыми вредными частицами, высвобождаются из активированных воспалительных клеток – макрофагов и нейтрофилов. Биомаркеры оксидативного стресса выявляются в конденсатах выдыхаемого воздуха, мокроте и в системной циркуляции у больных ХОБЛ. Оксидативный стресс отчетливо нарастает при обострении ХОБЛ.
ХОБЛ присущ специфический характер воспаления, включающий наряду с присутствием нейтрофилов и макрофагов увеличение числа СD8 (цитотоксических) Тс1 лимфоцитов. Эти клетки совместно с нейтрофилами и макрофагами высвобождают воспалительные медиаторы и энзимы, взаимодействуя со структурными клетками воздухоносных путей, легочной паренхимы и легочных сосудов.
Множество воспалительных медиаторов, наблюдаемых у больных ХОБЛ, привлекают воспалительные клетки из циркуляции (хемотаксические эффекты), усиливают воспалительный процесс (провоспалительные цитокины) и индуцируют структурные изменения (факторы роста).
Хотя ХОБЛ и бронхиальная астма (БА) ассоциируются с хроническим воспалением респираторного тракта, имеются различия в составе воспалительных клеток и медиаторах при этих заболеваниях, что объясняет различия в клинических симптомах и ответе на терапию. У части больных с ХОБЛ наблюдаются клинические проявления, присущие БА, и подобные БА воспалительные реакции с повышением уровней эозинофилов.
Характерными для ХОБЛ патофизиологическими изменениями являются гиперсекреция слизи, ограничение скорости воздушного потока и «воздушные ловушки», приводящие к гиперинфляции легких.
Гиперсекреция мокроты, сопровождающаяся хроническим продуктивным кашлем, является признаком хронического бронхита и не всегда ассоциируется с бронхиальной обструкцией (т.е. ХОБЛ). Вместе с тем, не у всех больных с ХОБЛ имеют место симптомы, связанные с гиперсекрецией мокроты.
Морфологически на начальных этапах ХОБЛ обычно имеет место негнойное воспаление и гиперсекреция слизи в бронхах диаметром более 2 мм, менее выраженное продуктивное воспаление – в бронхиолах меньшего диаметра при отсутствии изменений в зоне ацинусов (дистальный респираторный отдел легких).
Персистенция ХОБЛ и особенно развитие обострений заболевания сопровождается прогрессированием структурных изменений в бронхах. Так, продуктивное воспаление в бронхиолах диаметром менее 2 мм сопровождается утолщением стенок бронхиол, формированием бронхиолоэктазов и бронхиолита с формированием вентиляционных нарушений обструктивного характера. Выраженность воспаления, экссудации и фиброза в дистальных воздушных путях коррелирует со снижением ОФВ1. Периферическая обструкция ведет к ограничению скорости воздушного потока и прогрессивному увеличению «воздушных ловушек» во время выдоха, что приводит к повышенной воздушности легких – гиперинфляции. Гиперинфляция развивается на ранних стадиях ХОБЛ и является ведущим механизмом в развитии экспираторной одышки. Динамическая (при физических нагрузках) гиперинфляция приводит к усилению одышки и снижению толерантности к физической нагрузке (ТФН).
С развитием центрилобулярной эмфиземы начинается опустошение капиллярного русла, утолщение стенок артериол за счет пролиферации интимы, а в зонах эмфиземы – и мышечной оболочки их стенок. В последующем эмфизема распространяется на значительный объем легких. Постепенная деструкция легочной паренхимы, обусловленная эмфиземой, способствует увеличению «воздушных ловушек» на выдохе. Бронходилататоры, уменьшающие «воздушные ловушки», улучшают клиническую картину и ТФН при ХОБЛ.
Деструкция паренхимы, обусловленная эмфиземой, способствует как ограничению воздушного потока, так и нарушениям газового обмена. Нарушения альвеолярной вентиляции и уменьшение легочного васкулярного объема ведет к прогрессируюшему ухудшению показателя Va/Q и задержке СО2 (т.е. гипоксемии и гиперкапнии). Все эти факторы способствуют нарушению сократительных свойств дыхательной мускулатуры (т.н. «усталость» дыхательной мускулатуры).
На поздних стадиях течения ХОБЛ может развиваться легочная гипертензия (ЛГ), которая обусловлена главным образом гипоксической вазоконстрикцией малых легочных артерий. При этом развиваются структурные изменения артериальных сосудов малого круга в виде гиперплазии интимы, медии и гладкой мускулатуры. Наряду с этим развивается дисфункция эндотелия сосудов.
Уменьшение количества легочных капилляров, обусловленное эмфиземой, также способствует повышению давления в легочной циркуляции, появлению мозаичной гипертрофии кардиомиоцитов правого желудочка (ПЖ) с гипертрофией сосочковых и трабекулярных мышц, а затем и фиброза ПЖ. При этом повышается жесткость его миокарда, снижается коронарная перфузия, что в конечном итоге приводит к правожелудочковой сердечной недостаточности. Развивающаяся вследствие дилатации ПЖ трикуспидальная недостаточность еще более увеличивает перегрузку ПЖ объемом, снижает объем крови, изгоняемый в легочную циркуляцию, и снижает давление наполнения левого желудочка. Постепенно повышается давление в правом предсердии, в случае открытого овального окна может развиваться значимый сброс крови справа налево (дополнительный фактор снижения оксигенации артериальной крови).
Таким образом, основными патофизиологическими этапами ХОБЛ являются:
1) гиперсекреция слизи и негнойное продуктивное воспаление, которые создают условия для нарушения мукоцилиарного клиренса (мукостаз) и развития инфекционного процесса;
2) структурные изменения стенок дистальных бронхиол с формированием персистирующих вентиляционных нарушений обструктивного характера и «воздушных ловушек» – гиперинфляции легких;
3) эмфизематозная трансформация паренхимы легких (склероз межальвеолярных перегородок) с постепенным нарушением перфузионной функции легких (процессов газообмена);
4) прогрессирующая легочная гипертензия и формирование хронического легочного сердца с недостаточностью кровообращения.
ДИАГНОСТИКА ХОБЛ
Жалобы
Больные ХОБЛ на ранних этапах заболевания часто не предъявляют каких-либо определенных жалоб. Развернутая клиническая картина ХОБЛ наблюдается через 10-20 и более лет после начала регулярного курения.
Характерные клинические проявления ХОБЛ включают хроническую и прогрессирующую одышку, кашель и выделение мокроты.
Одышка – кардинальный симптом ХОБЛ, являющийся ведущей причиной снижения качества жизни, толерантности к физической нагрузке и трудоспособности. В типичных случаях больные ХОБЛ описывают одышку как ощущение затрудненности дыхания, тяжести в грудной клетке, нехватки воздуха и/или удушье.
Хронический кашель и продукция мокроты могут наблюдаться задолго до развития ограничения проходимости дыхательных путей и, напротив, существенное нарушение проходимости дыхательных путей может развиваться у лиц без предшествующего кашля и/или выделения мокроты. Сочетание одышки, кашля и выделения мокроты у курильщика в возрасте старше 40 лет позволяет предположить наличие ХОБЛ с высокой вероятностью.
Хронический кашель часто является первым симптомом развивающегося ХОБЛ и может существенно уменьшаться или даже исчезать после прекращения курения или воздействий вредных частичек окружающей среды. На начальных этапах заболевания кашель нередко носит интермиттирующий характер, но на далеко зашедших стадиях заболевания наблюдается ежедневно (нередко на протяжении всего дня). Хронический кашель при ХОБЛ может быть непродуктивным. В ряде случаев ХОБЛ может протекать без кашля.
Кашель может быть представлен также при целом ряде заболеваний и патологических состояний, не имеющих отношения к ХОБЛ, что требует внимательной дифференциальной диагностики. Ниже, в таблице 1 представлены различные причины, обусловливающие развитие хронического кашля.
Таблица 1
Различные причины хронического кашля
|
Интраторакальные |
Экстраторакальные |
|
Хронический бронхит (необструктивный) ХОБЛ БА Рак легкого Туберкулез Бронхоэктазы Левожелудочковая сердечная недостаточность Интерстициальные процессы в легких |
Хронические аллергические риниты / синуситы Гастроэзофагеальный рефлюкс Кашель, обусловленный применением ингибиторов агнгиотензинпревращающего фермента |
Кашель и регулярная продукция мокроты в течение 3 или более месяцев в течение 2-х последовательных лет (при отсутствии других причин) является критерием диагностики хронического бронхита без обструкции. Наличие значительного количества мокроты (обычно гнойной) или кровохарканье предполагает наличие бронхоэктазов. Наличие гнойной мокроты отражает увеличение воспалительных маркеров и может свидетельствовать о начале инфекционного обострения.
Свистящее дыхание и ощущение сдавления грудной клетки – типичные, но неспецифические симптомы ХОБЛ, особенно часто наблюдающиеся во время обострений. При этом свистящие хрипы могут выслушиваться над легкими на вдохе и выдохе. Источником «свистящего» дыхания также может быть уровень гортани (при этом отсутствуют сухие хрипы над легкими при аускультации). Чувство сдавления грудной клетки является следствием активного участия межреберной мускулатуры в акте дыхания.
У многих больных ХОБЛ имеют место cистемные (внелегочные) проявления, существенно влияющие на качество жизни и выживаемость. Ограничение проходимости дыхательных путей и особенно гиперинфляция легких неблагоприятно влияет на кардиальную функцию. Утомляемость, анорексия и исхудание с потерей мышечной массы – обычные симптомы у больных с тяжелым ХОБЛ. Персистенция воспалительных медиаторов в циркуляции способствует потере мышечной массы и снижению веса вплоть до развития кахексии, а также ухудшению течения ИБС, сердечной недостаточности, остеопороза, сахарного диабета, депрессии и тревоги, снижению сексуальной активности. При развитии ХЛС появляются и прогрессируют симптомы недостаточности кровообращения в виде гепатомегалии, периферических отеков, асцита.
Анамнестические данные
В диагностике ХОБЛ важное место отводится детально проведенному анамнезу, включающему выявление основных факторов риска заболевания:
- курение и другие вредные факторы окружающей среды;
- указания на наличие астмы, аллергии, синуситов, носовых полипов,
- частых респираторных инфекций, особенно в детстве;
- наличие заболеваний легких у кровных родственников;
- наличие сопутствующих заболеваний сердечно-сосудистой системы (ишемическая болезнь сердца, артериальные гипертензии, метаболический синдром), мышечно-скелетной системы (деформации грудной клетки, миопатии).
Физикальное исследование
Данные физикального исследования легких не играют решающей роли в ранней диагностике ХОБЛ, однако обязательно учитываются при постановке такого диагноза в комплексе с показателями функции внешнего дыхания (ФВД).
Результаты объективного исследования у больных ХОБЛ зависят от степени бронхиальной обструкции, наличия эмфиземы легких и легочной недостаточности (ЛН), признаков ХЛС и пр.
Так, при осмотре обращают внимание на участие дыхательной мускулатуры в акте дыхания, которое ассоциировано с тяжелой обструкцией (III-IV степени).
У лиц с развитием эмфиземы при осмотре грудная клетка имеет нередко бочкообразную форму, заполненные надключичные промежутки, границы легких смещены книзу, при перкуссии – коробочный перкуторный звук, ослабление везикулярного дыхания.
Цианоз/акроцианоз характеризутся как «теплый» и является проявлением гипоксии/гиперкапнии и наблюдается при тяжелой дыхательной / сердечной недостаточности.
Признаком бронхиальной обструкции является наличие сухих (свистящих и жужжащих) хрипов преимущественно на выдохе, количество которых нередко увеличивается в горизонтальном положении.
Одышка у больных ХОБЛ носит экспираторный характер и, даже будучи выраженной, не приводит к положению ортопное.
Отсутствие какой-либо патологии в физикальных данных не исключает наличия ХОБЛ.
Исследование функции внешнего дыхания
Исследование функции внешнего дыхания (ФВД) является обязательным этапом диагностики ХОБЛ. Только спирометрия позволяет установить наличие обструктивных нарушений – ключевого диагностического признака заболевания. Она позволяет оценить ряд объемных и скоростных показателей функции легких, выявить наличие обструктивных или рестриктивных нарушений вентиляции, оценить обратимость изменений под воздействием бронходилататоров.
Главный спирометрический критерий, подтверждающий диагноз ХОБЛ – отношение объема форсированного выдоха за первую секунду к форсированной жизненной емкости легких (ОФВ1/ФЖЕЛ) < 0,7 после ингаляции сальбутамола в дозе 400 мкг (т.е. после проведения бронходилатационного теста). Степень тяжести обструкции оценивается по постбронходилатационной величине ОФВ1 в соответствии с классификацией, представленной ниже, в таблице 2.
Таблица 2
Характеристика тяжести обструкции при ХОБЛ
|
Степень (тяжесть) обструкции |
Количественные показатели ОФВ1* |
|
|
I – легкая |
ОФВ1*/ФЖЕЛ < 0,7 |
ОФВ1 * ≥ 80% |
|
II – средне-тяжелая |
50% ≤ ОФВ1 *< 80% |
|
|
III – тяжелая |
30% ≤ ОФВ1*< 50% |
|
|
IV – очень тяжелая |
ОФВ1* < 30% |
|
Примечание: ОФВ1 * – постбронходилатационные значения
Следует отметить, что до недавнего времени наличие прироста ОФВ1 ≥ 12% (и/или ≥ 200 мл) при выполнении бронходилатационного теста считалось признаком обратимой бронхиальной обструкции, что, в свою очередь, давало основания для дифференциальной диагностики ХОБЛ и БА. В последние годы в целом ряде масштабных исследований продемонстрировано, что до 40% больных ХОБЛ наблюдается положительный ответ на тест с бронходилататором, т.е. прирост ОФВ1 на величину более 12%, причем иногда достигающую 30-40%! Поэтому обязательным критерием диагностики ХОБЛ является сохранение после бронходилатации ОФВ1/ФЖЕЛ < 0,7, а не отсутствие значительного прироста ОФВ1. Таким образом, проведение бронходилатационного теста позволяет диагностировать ХОБЛ, а также оценить тяжесть обструкции по постбронходилатационным значениям ОФВ1.
При постановке диагноза ХОБЛ после оценки ФВД окончательно исключают наличие состояний, при которых может наблюдаться неполностью обратимая бронхообструкция (БА, облитерирующий бронхиолит, саркоидоз, диффузные интерстициальные процессы), а также возрастное снижение ОФВ1.
Таким образом, диагноз ХОБЛ должен рассматриваться у каждого пациента старше 40 лет с респираторными жалобами (одышкой, хроническим кашлем, продукцией мокроты) и наличием ингаляционных факторов риска.
Ключевые подходы к диагностике ХОБЛ и наиболее распространенные причины некорректной постановки диагноза проиллюстрированы на рисунке 1.
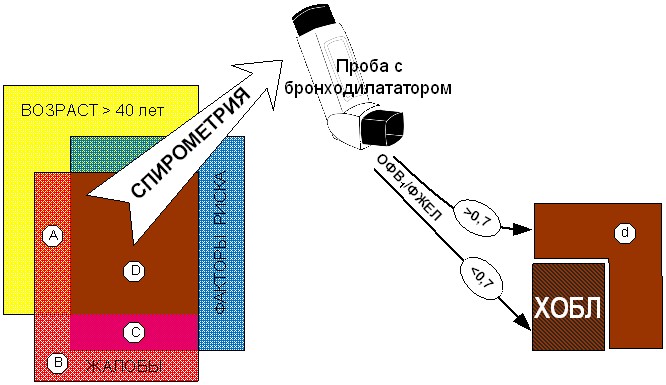
Рисунок 1. Диагностика ХОБЛ и возможные источники некорректного диагноза
Примечания:
ЖАЛОБЫ при ХОБЛ:
- одышка;
- хронический кашель;
- отделение мокроты
ФАКТОРЫ РИСКА ХОБЛ:
курение (10 и более пачек-лет);
бытовые и профессиональные ингаляционные загрязнения
СПИРОМЕТРИЯ:
Диагноз ХОБЛ устанавливается при наличии обструкции (ОФВ1/ФЖЕЛ < 0,7) после применения бронходилататора.
Как показано на рисунке 1, ХОБЛ должна рассматриваться у всех лиц старше 40 лет, подвергавшихся воздействию факторов риска (курение, бытовые и промышленные загрязнения воздуха) и имеющих характерные клинические проявления (одышку / хронический кашель / продукцию мокроты): в таких случаях необходимо выполнение спирометрического исследования. Выявление обструкции, сохраняющейся после приема бронходилататора (необратимой или не полностью обратимой), подтверждает наличие ХОБЛ.
Наиболее частые причины некорректной диагностики ХОБЛ включают:
- Отсутствие в анамнезе экспозиции ингаляционных факторов риска (преимущественно курения) – сегменты А и В;
- Молодой возраст – сегмент С: у лиц моложе 40 лет вероятность наличия ХОБЛ очень низкая (менее 2%);
- Отсутствие спирометрического подтверждения – сегменты D и d: без проведения спирометрии достоверный диагноз ХОБЛ невозможен, так как у 23 лиц с клиническими проявлениями и факторами риска ХОБЛ обструкция может отсутствовать или быть обратимой (d).
Дифференциальная диагностика
ХОБЛ необходимо дифференцировать с рядом заболеваний, имеющих сходные клинические симптомы. В таблице 3 представлена краткая характеристика ХОБЛ и заболеваний, с которыми следует проводить дифференциальную диагностику.
Таблица 3
Дифференциальная диагностика ХОБЛ
|
Диагноз |
Ведущие признаки |
|
ХОБЛ |
Развивается после 40 лет Симптомы медленно прогрессируют. Длительное предшествующее табакокурение или экспозиция других вредных факторов внешней среды. Появление одышки при физической нагрузке и ее неуклонное прогрессирование. Прогрессирование необратимой бронхиальная обструкции |
|
Бронхиальная астма |
Начинается в молодом возрасте (часто в детстве). Симптомы варьируют ото дня ко дню. Симптомы наблюдаются преимущественно ночью и/или в ранние утренние часы Часто имеют место аллергия, риниты, экзема, носовые полипы Семейная БА в анамнезе Обычно бронхиальная обструкция, обратимая после применения бронходилататоров. |
|
Застойная сердечная недостаточность |
Часто в нижне-боковых отделах легких наблюдаются крепитация, субкрепитирующие и мелкопузырчатые хрипы Рентгенография грудной клетки позволяет выявлять расширение тени сердца, признаки венозной гипертензии (застой в легких) Функциональные легочные тесты показывают объемную рестрикцию, а не обструкцию бронхов. |
|
Бронхоэктазы |
Обильное выделение гнойной мокроты, кровохарканье КТ органов грудной клетки позволяет выявить бронхоэктазы |
|
Туберкулез |
Учитывать высокую распространенность туберкулеза! Начинается в любом возрасте. Рентгенография грудной клетки демонстрирует легочный инфильтрат/плеврит/округлую тень и пр. Микробиологическое подтверждение |
|
Облитерирующий бронхиолит |
Начало в молодом возрасте, в том числе у некурящих Наличие ревматоидного артрита или воздействие токсических промышленных газов КТ на выдохе позволяет выявить участки пониженной плотности |
|
Диффузный панбронхиолит |
Наблюдается преимущественно в странах Азии Большинство пациентов мужчины (в том числе некурящие) У подавляющего большинства больных хронические синуситы Рентгенография грудной клетки или КТ высокого разрешения позволяет выявить диффузные малые центрилобулярные узловые затенения и гиперинфляцию |
КЛИНИЧЕСКАЯ ОЦЕНКА ПАЦИЕНТА И КЛАССИФИКАЦИЯ ХОБЛ.
В рекомендациях GOLD 2014 используется классификация ХОБЛ, базирующаяся на всесторонней клинической оценке состояния больного. Так, оценка клинического статуса ХОБЛ должна основываться на: 1) интенсивности симптомов, 2) прогнозировании риска осложнений, 3) тяжести спирометрических нарушений и 4) выявлении серьезных сопутствующих заболеваний и патологических состояний (ишемическая болезнь сердца, сердечная недостаточность, фибрилляция предсердий, артериальная гипертензия, остеопороз, тревожные и депрессивные расстройства, рак легкого, сахарный диабет, почечная недостаточность, хронические инфекции).
С 2011 года эксперты GOLD предложили отказаться от концепции стадийности заболевания. Это связано с тем, что не у каждого пациента отмечается клинически значимое прогрессирование заболевания со временем, а также с отсутствием строгой корреляции между возрастом и стадиями заболевания (например, в масштабном исследовании Jones P.W. с соавт. (2011) средний возраст пациентов на всех стадиях ХОБЛ оказался одинаковым – около 65 лет). Наряду с этим, вместо выделения стадий ХОБЛ предлагается распределение больных по тяжести бронхиальной обструкции (см. выше табл. 2).
Клиническая характеристика больных ХОБЛ, соответствующая указанным градациям тяжести обструкции, приведена в таблице 4.
Таблица 4
Клиническая характеристика ХОБЛ с различной степенью обструкции (I-IV)
Степень (тяжесть) обструкции |
Клиническая характеристика |
I (легкая)ОФВ1 ≥ 80% от должных величин |
Можно (но не всегда) прицельно установить наличие хронического кашля и выделение мокроты. Больные обычно не имеют представления о наличии у них нарушений легочных функций |
II (умеренная)50% ≤ ОФВ1 < 80% |
Можно определить появление одышки на фоне физической нагрузки. Пациенты обычно обращаются за медпомощью в связи с обострением заболевания. Наличие повторных обострений влияет на качество жизни пациентов и требует соответственной тактики лечения. Вне обострений при спирометрии отчетливо превалируют обструктивные вентиляционные нарушения |
III (тяжелая)30% ≤ ОФВ1 < 50% |
Прогрессирование одышки существенно снижает качество жизни пациентов. Частые обострения могут представлять угрозу для жизни из-за развития острой легочной недостаточности, поэтому ХОБЛ приобретает инвалидизирующее течение |
IV (очень тяжелая)ОФВ1*< 30% |
Характеризуется крайне тяжелой бронхиальной обструкцией, часто в сопровождении с признаками гипоксемии (т.е. SаO2 < 90 %) и/или ХЛС |
Важным аспектом является «комбинированная оценка» ХОБЛ. Цель этой комбинированной оценки – определение тяжести заболевания, и риска будущих осложнений (обострений и госпитализаций) для последующего выбора лечебной тактики. Алгоритм оценки пациента в соответствии с рекомендуемым подходом состоит из следующих шагов.
- Оценить интенсивность симптомов. С этой целью рекомендуется использовать модифицированную шкалу одышки Медицинского исследовательского совета (МMRC) (табл. 4), опросник оценки ХОБЛ – САТ (COPD Assessment Test) (рис.2), или Клинический опросник ХОБЛ – CCQ (Clinical COPD Questionnaire). Предпочтение следует отдавать последним, так как они более полно характеризуют функциональный статус пациента; использовать оба показателя нецелесообразно. В клинической практике целесообразнее говорить о САТ, потому что он переведен и валидизирован для большинства языков и стран.
Таблица 4
Модифицированная шкала одышки Медицинского исследовательского совета (Modified Medical Research Council Dyspnea Scale – MMRC)
|
Степень |
Клиническая характеристика |
|
0 |
Одышка не беспокоит, за исключением очень интенсивной нагрузки |
|
1 (легкая) |
Одышка при быстрой ходьбе или при подъеме на небольшое возвышение |
|
2 (умеренная) |
Одышка приводит к замедлению ходьбы по сравнению с другими людьми того же возраста или заставляет делать остановки при ходьбе в обычном темпе по ровной поверхности |
|
3 (тяжелая) |
Одышка заставляет делать остановки при ходьбе на расстояние до 100 м или через несколько минут ходьбы по ровной поверхности |
|
4 (очень тяжелая) |
Одышка делает невозможным выход за пределы квартиры, или появляется при одевании и раздевании |
Рисунок 2. Опросник САТ (COPD Assessment Test) (в свободном доступе на разных языках на ресурсе www.catestonline.org)
Подсчет баллов в предложенных опросниках позволяет выделить категории пациентов («малосимптомный» и «значительносимптомный»), которые следует внести в клинический диагноз. Так, «значительносимптомными» считаются больные с уровнем одышки по шкале МMRC ≥ 2 баллов или те, которые имеют ≥ 10 баллов по опроснику САТ или ≥ 1 балла по опроснику CCQ.
- Оценить риск осложнений ХОБЛ. Определить риск осложнений можно двумя путями. Во-первых, на основании спирометрической тяжесть обструкции. Так, при I-II степени тяжести (постбронходилатационный ОФВ1 > 50%) предполагается невысокий риск осложнений, а при III-IVстепени (ОФВ1 < 50%) – высокий. Во-вторых, следует оценить количество перенесенных обострений за прошедший год. Наличие в течение 12 месяцев 2 и более обострений ХОБЛ, потребовавших лечения или хотя бы 1 госпитализация из-за обострения, является достоверным предиктором частых обострений и госпитализаций в будущем. Таким образом, прогнозирование риска обострений у пациента с ХОБЛ оценивается в зависимости от спирометрической тяжести, или от частоты и тяжести перенесенных ранее обострений. Если эти два подхода у конкретного пациента оценивают риск неоднозначно, необходимо опираться на более высокую (тяжелую) оценку.
- Определить клиническую группу. На основании оценки выраженности симптомов и риска возможных осложнений, следует определить, к какой клинической группе (A, B, C или D) относится пациент с ХОБЛ. Схематично это представлено на рисунке 2. Выделяется группа А – «Низкий риск, незначительные симптомы», группа B – «Низкий риск, значительные симптомы», группа С – «Высокий риск, незначительные симптомы» и группа D –«Высокий риск, значительные симптомы». Подавляющее большинство больных (80-90 % ) относятся к группам B и D, около 10% – к группе А и лишь несколько процентов – к группе С.
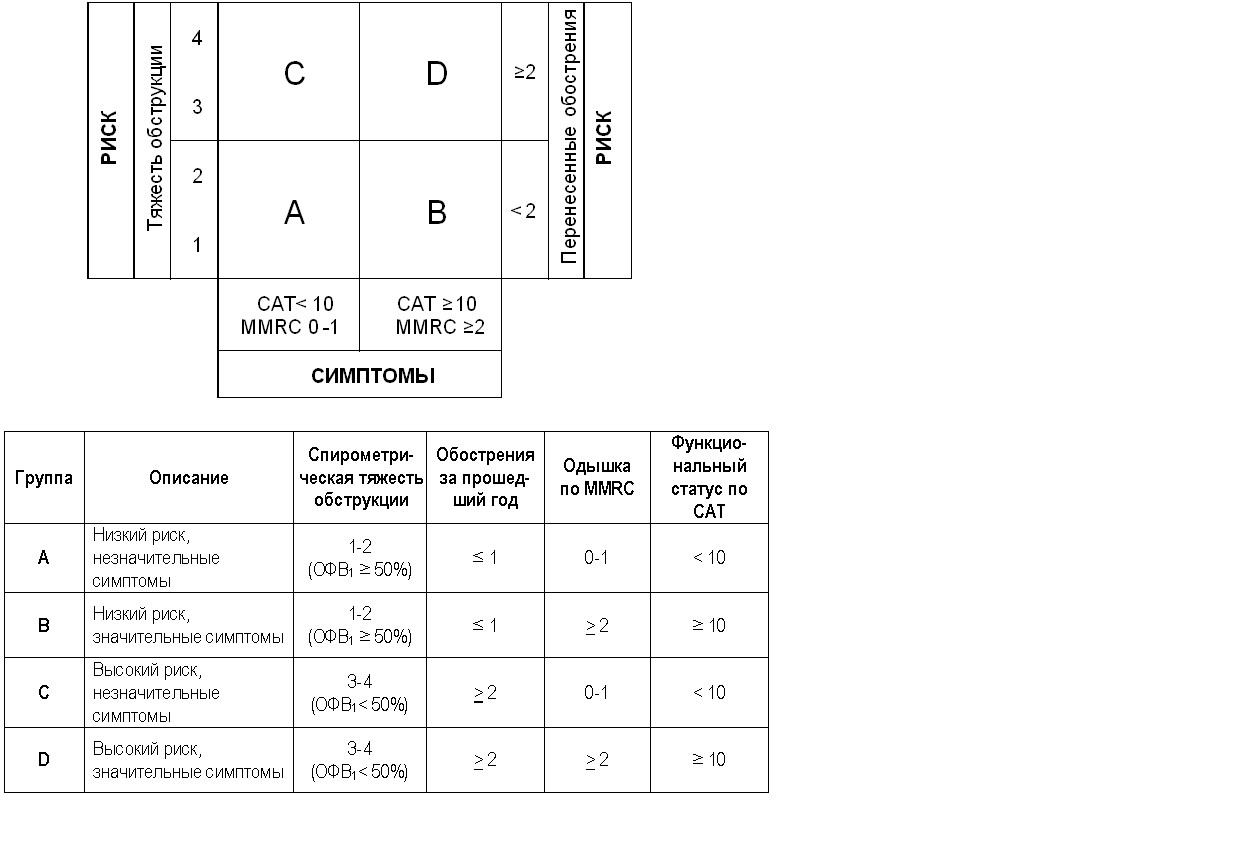
Рисунок 3. Классификация и схема для определения клинической группы ХОБЛ (A, B, C, D – в зависимости от выраженности симптомов и оценки риска возможных осложнений). При оценке риска у индивидуального пациента выбирается показатель, отражающий наибольший риск.
Примечание: дополнительным маркером высокого риска является госпитализация по поводу обострения ХОБЛ за последние 12 мес.
Формулирование диагноза. При формулировке диагноза ХОБЛ должна быть указана клиническая группа (А-D), тяжесть бронхиальной обструкции (I-IV), обострение или ремиссия заболевания и наличие других осложнений заболевания. Указание на наличие хронического бронхита и / или эмфиземы является лишним и избыточным, потому что они являются составными компонентами понятия ХОБЛ.
В качестве иллюстрации можно привести клиническую оценку пациента 57 лет, обратившегося за помощью в связи с усилением кашля и выделением мокроты, а также одышкой 3 степени по MMRC, у которого диагностирована ХОБЛ (ОФВ1/ФЖЕЛ < 0,7, постбронходилатационное значение ОФВ1 – 57%, 17 баллов по шкале САТ и за последние 12 месяцев он перенес 2 обострения, потребовавших применения антибиотиков). Оценка симптомов по САТ относит его к «значительно симптомным» пациентам (группа В или D). Из-за высокой частоты обострений в течение года пациент относится к группе более высокого риска –группе D. Таким образом, клинический диагноз у больного выглядит следующим образом: ХОБЛ, бронхиальная обструкция 2 степени, клиническая группа D, обострение.
Описанный выше комбинированный подход к оценке больного ХОБЛ лучше отражает многофакторность заболевания и позволяет индивидуализировать лечение в большей мере, чем использовавшаяся ранее однонаправленная оценка пациента преимущественно по степени спирометрических нарушений.
ЛЕЧЕНИЕ ХОБЛ
Основными стратегическими подходами к лечению ХОБЛ в стабильном периоде являются:
- прекращение курения (предлагается в качестве первоочередной задачи, при этом могут рекомендоваться различные варианты никотин-заместительной терапия, значительно увеличивает частоту устойчивого воздержания от табакокурения);
- рациональная базисная фармакотерапия, которая позволяет не только эффективно контролировать респираторную симптоматику и предупреждать развитие обострений, а также улучшать качество жизни, способствуя повышению толерантности к физической нагрузке (ТФН).
- проведение легочной реабилитации (всем пациентам, имеющим одышку при ходьбе в обычном темпе по ровной местности для существенного улучшения качества жизни).
- противогриппозная и антипневмококковая вакцинация (должна рекомендоваться всем пациентам, особенно пожилым, с тяжелой ХОБЛ или сопутствующими кардиоваскулярными заболеваниями).
Прекращение курения
Прекращение курения – один из ведущих и наиболее эффективных подходов первичной и вторичной профилактики ХОБЛ. Прекращение курения тесно ассоциируется с замедлением прогрессирования бронхообструкции, улучшением качества жизни и снижением летальности больных ХОБЛ.
Важное место в программах, направленных на прекращение курения больными ХОБЛ отводится медицинским работникам. Даже короткая (3-минутная) беседа, объясняющая пагубное влияние курения на течение заболевания увеличивает частоту отказа от курения на 5–10%.
Каждому курильщику, который начинает серьезную попытку отказа от курения, должно быть предложено фармакологическое лечение никотиновой зависимости. При использовании медикаментов первой линии (никотинзаместительная терапия, бупропион и варениклин) вероятность успешного прекращения курения удваивается.
Никотинзаместительные препараты представлены несколькими формами, которые позволяют учитывать индивидуальные особенности пациента. Эффективность нижеуказанных подходов одинакова.
Никотиновый полакрилекс (жевательная резинка) содержит никотин, прикрепленный к полакрилексной резины вместе с буферной веществом. Жевание высвобождает из полакрилекса никотин, который абсорбируется через слизистую щеки. Существуют формы, содержащие 2 или 4 мг никотина. Рекомендуется применение от 8 до 10 резинок в день. Рекомендуется лечение в течение 3-6 мес.
Трансдермальная никотиновая система, или «пластырь», наклеивается на свободную от волос кожу туловища или проксимальной части конечностей. Трансдермальный никотин снижает интенсивность, но не исключает полностью симптомы абстинентного синдрома. Лечение такими пластырями обычно рекомендуется в полной дозе в течение 4-6 нед. Часто за этим следует период лечения сниженной дозой в течение еще нескольких недель.
Никотиновый назальный спрей состоит из водного раствора никотина. Он доставляется путем прямого впрыска на слизистую носа. Одно впрыскивание обеспечивает дозу 1 мг никотина. Абсорбция относительно быстрая, пиковый уровень достигается за ~ 10 мин. Это наиболее близко к тому, что происходит при курении. В связи с этим никотиновый назальный спрей имеет увеличенный потенциал продолжения никотиновой зависимости по сравнению с другими препаратами.
Никотиновые пастилки как средство помощи для отказа от курения является относительно новой формой никотина. Представлены в дозах 2 и 4 мг. Курильщику предлагается выбрать дозу на основании интервала времени от пробуждения до первой сигареты (мера интенсивности зависимости). Для тех, кто закуривает сигарету течение 30 мин после утреннего пробуждения, рекомендуется 4 мг никотина. Необходимо принимать до 9 пастилок в день (через каждые 1-2 ч) в течение 6 недель, снижая затем дозу с последующим упразднением через 6 мес. Лечение обычно начинается в день отказа от курения.
Бупропион является не-никотиновым средством, который раньше использовали как антидепрессант. Бупропион удваивает частоту отказа от курения по сравнению с плацебо. Лечение обычно начинают в дозе 150 мг ежедневно с последующим увеличением через 3 дня до 150 мг дважды в день, если препарат хорошо переносится. День отказа от курения должен назначаться через 1 неделю после начала лечения бупропионом. Лечение обычно длится 7-12 мес. У некоторых лиц с указаниями на депрессию бупропион может быть более эффективным, чем никотинзаместительная терапия.
Варениклин применяется в качестве средства против курения у взрослых, в большинстве исследований зарекомендовал себя как наиболее эффективный препарат. Эффективность варениклина в лечении никотиновой зависимости связана с частичным агонизмом в отношении α4β2-никотиновых рецепторов. Связывание препарата с этими рецепторами позволяет уменьшить тягу к курению и синдром отмены, а также одновременно приводит к уменьшению эффекта получения удовольствия от курения. Пациент должен выбрать дату прекращения курения. Лечение варениклином следует начать за 1-2 недели до этой даты. Варениклин принимают внутрь: рекомендуемая доза составляет 1 мг два раза в день, при этом предлагается следующий режим титрования: в течение первой недели 1-3 дня – 0,5 мг один раз в день, 4-7дни – 0,5 мг два раза в день, 8 день – конец титрования – 1 мг два раза в день, что продолжают в течение 12 недель. У больных, прекративших курение в течение 12 недель, возможен дополнительный 12-недельный курс лечения в дозе 1 мг два раза в день.
Характеристика медикаментозных препаратов, применяющихся при лечении ХОБЛ
Бронходилататоры.
Ведущее место в комплексной фармакотерапии ХОБЛ занимают бронходилататоры (бронхолитики), которые объединяют несколько групп фармакологических препаратов: β2-агонисты и антихолинэргические препараты короткого и длительного действия, а также метилксантины (или ингибиторы фосфодиэстеразы). Фармакологическая характеристика наиболее распространенных препаратов бронхолитического ряда представлена в таблицах 5 и 6.
Таблица 5
Характеристика основных ингаляционных бронходилататоров, используемых при лечении ХОБЛ
|
Препарат |
Доза, мкг |
Пик действия, мин |
Продолжительность действия, час |
|
β2-агонисты короткого действия (БАКД) |
|||
|
Сальбутамол |
100, 200 |
30−60 |
4−6 |
|
Фенотерол |
100 |
30 |
4−6 |
|
Антихолинэргические препараты короткого действия (АХП КД) |
|||
|
Ипратропия бромид |
20,40 |
45−60 |
6−8 |
|
β2-агонисты длительного действия (БАДД) |
|||
|
Формотерол |
4,5-12 |
120−360 |
12 |
|
Сальметерол |
25-50 |
120−360 |
12 |
|
Индакатерол |
75-300 |
120−360 |
24 |
|
Антихолинэргические препараты длительного действия (АХП ДД) |
|||
|
Тиотропия бромид |
18 |
30−45 |
24 |
|
Аклидиниум бромид |
322 |
30−45 |
24 |
|
Гликопиррониум бромид |
44 |
30−45 |
24 |
Эффект β2-агонистов короткого действия (БАКД) (сальбутамол, фенотерол) проявляется уже через несколько минут, достигая пика через 15-30 мин, и продолжается 4-6 часов. Больные ХОБЛ в большинстве случаев отмечают облегчение дыхания сразу после ингаляции этих препаратов, что является несомненным их преимуществом. Данные препараты используются по 1-2 дозы по требованию – при одышке на высоте физической нагрузки, приступах удушья.
β2-агонисты длительного действия (БАДД) (сальметерол, формотерол, индакатерол) уменьшают бронхиальное сопротивление за счет снижения тонуса мускулатуры бронхов. Сальметерол также улучшает сократимость дыхательных мышц, уменьшая их слабость и дисфункцию. Формотерол в отличие от сальметерола имеет более быстрое начало действия – 5-7 мин.
Стандартный режим назначения БАДД: сальметерол по 50-100 мкг дважды в день, формотерол – 4,5-9 мкг дважды в день, индакатерол по 150-300 мкг однократно в сутки. Длительное действие БАДД позволяет рекомендовать их для регулярного применения в терапии стабильной ХОБЛ. БАДД продемонстрировали благоприятные эффекты на показатели как функции внешнего дыхания (т.е. симптомы бронхообструкции), так и качество жизни у больных ХОБЛ (в частности, частоту обострений).
Антихолинэргические препараты (АХП). Основной представитель АХП КД – ипратропия бромид. Он также используется в качестве скоропомощного препарата по требованию и при лечении обострений ХОБЛ. Ипратропий характеризуется более медленным началом действия по сравнению с БАКД (через 10-20 минут, пик через 45-60 минут), но большей продолжительностью эффекта (6-8 часов). АХП КД часто применяются в виде фиксированных комбинаций с БАКД –фенотреол/ипратропий или сальбутамол/ипратропий. Такое сочетание позволяет обладает аддитивными свойствами с оптимизированой эффективностью. В то же время следует помнить, что в целом ряде мета-анализов АХП КД продемонстрировали существенно негативный профиль сердечно-сосудистой безопасности: длительное применение ипратропия сопровождается увеличением риска развития или декомпенсации сердечной недостаточности, нарушений ритма, кардиоваскулярной летальности.
Одним из наиболее часто применяемых базисных препаратов в лечении ХОБЛ является АХП ДД тиотропия бромид, который преимущественно блокирует М1 и М3 -холинорецепторы, действуя на протяжении суток. Продолжительное (в течение 12 мес) лечение АХП ДД сопровождается улучшением показателей бронхиальной проходимости, регрессом респираторной симптоматики, улучшением качества жизни больного за счет уменьшения частоты обострений и госпитализаций, а также характеризуется благоприятным профилем сердечно-сосудистой безопасности.
Таблица 6.
Характеристика лекарственных форм ингаляционных бронходилататоров
|
Лекарственное вещество |
Лекарственная форма |
Доза, мкг |
|
БАКД |
|
|
|
Сальбутамол |
ДАИ |
100 |
|
Фенотерол |
ДАИ |
100 |
|
АХП КД |
|
|
|
Ипратропия бромид |
ДАИ |
40 |
|
БАДД |
|
|
|
Сальметерол |
ДАИ |
25 |
|
Формотерол |
ПИ |
12 |
|
Индакатерол |
ПИ |
75; 150; 300 |
|
АХП ДД |
|
|
|
Тиотропия бромид |
Капс. д/инг. Хенди Хэйлер Картридж р-р д/инг Респимат 4 мл (60 доз) |
18 2,5; 5 |
|
Аклидиниум бромид |
ПИ |
322 |
|
Гликопиррониум бромид |
ПИ |
44 |
Примечание: ДАИ дозированный аэрозольный ингалятор, ПИ – порошковый ингалятор
Метилксантины (эуфиллин, доксофиллин, теофиллин) представляют собой неселективные ингибиторы фосфодиэстеразы 1-3 типов и аденозиновых рецепторов бронхов, эффектом которого является внутриклточное накопление цАМФ в гладкомышечных клетках бронхов и их расслабление. Метилксантины проявляют бронхолитические эффекты, хотя и менее значимые по сравнению с вышеприведенными группами ингаляционных препаратов.
Множество сообщений свидетельствуют о некотором противовоспалительном действии метилксантинов, способности их увеличивать силу дыхательной мускулатуры, снижать давление в системе легечной артерии, стимулировать продукцию глюкокортикоидов надпочечниками, усиливать диурез. Из-за риска побочных эффектов метилксантины используются в качестве терапии второй линии в комбинации с БАДД и/или АХП ДД при тяжелом течении ХОБЛ в группах В, С, D, а также при обострениях ХОБЛ.
Из препаратов класса метилксантинов только теофилин ДД в международных согласительных документах допускается для длительного использования при ХОБЛ в качестве базисного препарата. Он является средством для контроля респираторных симптомов и показателей функции внешнего дыхания у пациентов с ХОБЛ, которые не привержены к ингаляционным препаратам, способен отсрочить признаки утомления дыхательной мускулатуры в условиях повышенной нагрузки, несколько повышает физическую работоспособность и качество жизни.
Теофиллин ДД представляет собой таблетки или капсулы с пролонгированным высвобождением препарата, что позволяет использовать эти лекарственные формы по 300-600 мг 1-2 раза в сутки (при использовании большей дозы риск токсических эффектов теофиллина существенно повышается!).
Побочными (токсическими) эффектами теофиллина считают проявления тревоги, раздражительность, головную боль, тремор, дисфункции желудочно-кишечного тракта (тошнота, рвота, абдоминальные боли, усиленный диурез, гиперемия кожи, субфебрильная лихорадка). При достижении высоких концентраций есть риск появления судорог или эпилептиформных приступов (при концентрации в плазме крови > 20 мкг/мл) и различных аритмий (экстрасистолия, желудочковые тахикардии, фибрилляция предсердий и желудочков) с летальным исходом (при концентрации > 30 мкг/мл).
Место теофиллина КД (эуфиллина) отводится лишь избранным случаям купирования тяжелых обострений ХОБЛ при недостаточной эффективности других мероприятий.
Отдельного внимания заслуживает ингибитор фосфодиэстеразы-4 (ИФДЭ-4) рофлумиласт (таб. по 500 мкг, применятся 1 раз в сутки). Данный препарат сочетает свойства слабого бронходилататора и противовоспалительного агента. Следует помнить, что единственное показание для добавления этого препарата в схему лечения – необходимость в дополнительной профилактике обострений ХОЗЛ. Он изучался в исследованиях исключительно при добавлении к ингаляционным препаратам, где было установлено, что он позволяет дополнительно снизить частоту обострений на 25-30% у пациентов с четко очерченным фенотипом ХОБЛ: при наличии ОФВ1<50%, выделением значительного количества мокроты и частыми обострениями. Применение рофлумиласта у другой категории пациентов или в качестве монотерапии недопустимо.
Основные принципы использования бронходилататоров в терапии ХОБЛ представлены следующими позициями:
- Бронходилататоры занимают центральное место в симптоматическом лечении ХОБЛ;
- Ингаляционная терапия имеет многочисленные преимущества перед системным использованием препаратов;
- Бронходилататоры назначаются «по требованию» или на регулярной основе;
- Пролонгированные бронходилататоры снижают риск обострений, госпитализаций, улучшают симптомы и качество жизни.
- Комбинации различных бронходилататоров позволяют уменьшить частоту побочных эффектов по сравнению с увеличение дозы одного препарата.
- Метилксантины (теофиллин ДД) менее эффективны и хуже переносятся по сравнению с ингаляционными средствами. Они используются как препараты второй линии при недостаточном клиническом эффекте АХП , β2-агонистов или их комбинаций. С целью снижения побочных эффектов теофиллина ДД следует начинать лечение с низких дозировок препарата, увеличивая их при необходимости и хорошей переносимости.
Место глюкокортикоидов в терапии ХОБЛ
Глюкокортикоиды (ГК) не влияют на нейтрофильное воспаление в бронхах при ХОБЛ и не относятся к классу бронходилататоров, но влиять на бронходилатирующий эффект за счет: 1) уменьшения отека слизистой оболочки и улучшения проходимости дыхательных путей; 2) восстановления чувствительности β2-рецепторов бронхов к соответствующим препаратам; 3) неселективной стимуляции продукции сурфактанта; 4) уменьшения таксиса ПМЯЛ к легким; 5) повышение активности ингибиторов протеаз в бронхиальном секрете; 6) уменьшение секреции слизи бронхиальными железами и бокаловидными клетками.
Ингаляционные ГК (ИГК) при регулярном применении у пациентов с ОФВ1< 60% улучшают симптомы, легочную функцию, качество жизни и снижают частоту обострений. Монотерапия ингаляционными ГК не осуществляется, при ХОБЛ ИГК применяются только в сочетании с пролонгированными бронходилататорами, как правило, БАДД. Характеристика ингаляционных препаратов (фиксированных комбинаций), содержащих БАДД и ИГК представлена в таблице 7.
Таблица 7
Характеристика основных фиксированных комбинаций БА ДД и ГК
|
Препарат |
Лекарственная форма |
Доза, мкг |
|
Сальметерол флутиказон |
ДАИ ПИ ДАИ |
25 50, 125, 250 50 100, 250, 500 25 50, 125, 250 |
|
Формотерол будесонид |
ПИ |
4,5 80, 160; 9 320 |
Примечание: ДАИ дозированный аэрозольный ингалятор, ПИ – порошковый ингалятор
В Рекомендациях GOLD 2014 определены особенности использования ИГК при ХОБЛ:
- эффект ИГК должен дополнять эффекты постоянной бронходилатационной терапии (то есть ИГК не должны назначаться в монотерапии, отдельно от БАДД или АХП ДД)
- у пациентов с постбронходилатационным ОФВ1 < 50% от должного и частыми обострениями (клиническая группа С, D) ИГК при постоянном использовании уменьшают частоту обострений ХОБЛ и улучшают качество жизни пациентов;
- в большом количестве исследований длительное применение ИГК не сопровождалось уменьшением темпов ежегодного снижения ОФВ1 у пациентов с ХОБЛ; однако в одном из наибольших и длительных исследований эффектов фармакотерапии при ХОБЛ (TORCH study) установлено достоверное снижение темпа прогрессирования нарушений вентиляции при лечении флутиказоном.
- согласно результатам ряда мета-анализов, убедительных доказательств благоприятного влияния системных ГК на бронхиальную проходимость у больных со стабильным ХОБЛ получено не было, а положительное влияние на показатели вентиляционной функции легких отмечено только у 10% больных ХОБЛ. Учитывая это обстоятельство, а также известный риск развития нежелательных побочных эффектов, назначение системных ГК на постоянной основе при стабильной ХОБЛ не рекомендуется.
Использование муколитиков (мукокинетиков, мукорегуляторов) у больных ХОБЛ ограничивается случаями с наличием вязкой трудноотделяемой мокроты.
Базисная медикаментозная терапия стабильной ХОБЛ
Стратегическими направлениями медикаментозной терапии стабилной ХОБЛ являются:
- контроль симптомов бронхообструкции при стабильной ХОБЛ (базисная фармакотерапия),
- профилактика повторных обострений, что позволяет замедлить прогрессирование заболевания.
В рекомендациях GOLD 2014 года предложены подходы к выбору и проведению базисной медикаментозной терапии, предусматривающие терапию первой линии, второй линии и альтернативный лечебный подход у больных клинических групп A, B, C, D (их характеристика показана на рис. 4).
Согласно представленной схеме, для терапии первого шага предлагается следующий алгоритм выбора препаратов:
Группа А (незначительные симптомы, низкий риск осложнений): наибольшее значение имеют немедикаментозные рекомендации (см. выше), можно использовать (по потребности) БАКД или АХП КД, или их фиксированные комбинации.
Группа В (значительные симптомы, низкий риск осложнений): рекомендовано постоянное использование БАДД формотерола 12 мкг или сальметерола 50 мкг 2 раза в день или АХП ДД тиотропиум бромид 18 мкг 1 раз в день, при неэффективности – их комбинация.
Группа С (незначительные симптомы, высокий риск осложнений): ИГК в комбинации с БАДД или АХП ДД. Оптимальным считают использование фиксированных комбинаций (например, сальметерол флутиказон или формотерол будесонид утром и вечером).
|
Базисная терапия стабильного ХОБЛ* |
|||
|
Клини-ческая группа ХОБЛ |
Первая линия |
Вторая линия |
Альтернатива # |
|
A |
«По потребности»: АХП КД или БА КД |
АХП ДД или БА ДД АХП КД БА КД |
Теофиллин ДД |
|
B |
АХП ДД или БА ДД |
АХП ДД БА ДД |
БА КД ± АХП КД
Теофиллин ДД |
|
С |
ИГК БА ДД или АХП ДД |
АХП ДД БА ДД или АХП ДД ИФДЕ-4 или БА ДД ИФДЕ-4 |
ИФДЭ-4
β2агонисты КД ± АХП КД
Теофиллин |
|
D |
ИГК БА ДД и/или АХП ДД |
ИГК БА ДД АХП ДД или ИГК БА ДД ИФДЕ-4 или АХП ДД ИФДЕ-4 или АХП ДД БА ДД или АХП ДД ИФДЕ-4 |
Карбоцистеин
β2агонисты КД ± АХП КД
Теофиллин |
Рисунок 4. Подходы к выбору фармакотерапии при стабильной ХОБЛ
Примечания:
- * – препараты внутри ячеек приведены в алфавитном порядке;
- # – препараты из этой колонки могут использоваться самостоятельно или в сочетании с препаратами первой и второй линий
- ИФДЕ-4 – ингибиторы фосфодиэстаразы-4 (рофлумиласт)
Группа D (значительные симптомы, высокий риск осложнений): больные должны принимать БАДД в сочетании ИГК или АХП ДД. Для наиболее тяжелых пациентов позволительно в качестве стартовой терапии выбирать их сочетание. Различные рекомендуемые варианты терапии второй линии представлены на рис.4.
Определенное место в базисной терапии стабильного ХОБЛ сохраняет теофиллин ДД, который может использоваться в любых группах ХОБЛ как альтернативный подход (например, при невозможности (непереносимости ингаляционной терапии, отказе пациента от использования ингаляторами, финансовых причинах) с учетом побочных эффектов препарата.
ОБОСТРЕНИЯ ХОБЛ
Обострение ХОБЛ представляет острую ситуацию, характеризующуюся существенным ухудшением респираторных симптомов, что требует изменения обычного лечебного режима (увеличение интенсивности обычно используемой терапии или назначение других классов препаратов).
Обострения ХОБЛ не только требуют длительного восстановительного периода и способствуют прогрессирующему снижению показателей легочной функции, но и ассоциируются с высокой смертностью, особенно среди пациентов, потребовавших госпитализации.
Обострения ХОБЛ чаще всего обусловлены инфекциями трахеобронхиального тракта (бактериальными или вирусными), реже – другими факторами, причем у 1/3 больные причины обострений остаются не устанавленными.
Клиническая характеристика обострения ХОБЛ
Ведущими симптомами обострения ХОБЛ являются:
- появление или усиление одышки (частота – до 90%),
- усиление кашля (до 80-85%)
- увеличение количества мокроты и гнойный ее характер (60-70%).
Кроме того, обострения ХОБЛ нередко сопровождаются явлениями катарального воспаления верхних дыхательных путей (насморк, заложенность носа, боль в горле), часто обострение сопровождается чувством «сдавления» в грудной клетке, появлением свистящих хрипов на выдохе и снижением ТФН, наблюдаются также лихорадка, тахикардия, общая слабость, бессонница.
Появление «новых» рентгенологических изменений, как правило, требует дифференциальной диагностики с внегоспитальной пневмонией.
Определение тяжести обострения ХОБЛ базируется на оценке выраженности жалоб и физикальных симптомов, а также данных ФВД, пульсоксиметрии и др. Следует подчеркнуть, что выполнение спирометрии во время обострений обычно затруднено, а результаты недостаточно объективны.
Лечебная тактика при обострении ХОБЛ
Для лечения обострения ХОБЛ применяются бронходилатирующие препараты, глюкокортикоиды, антибиотики. Важным в лечении обострений ХОБЛ также считают контролируемую оксигенотерапию с целевыми уровнями оксигенации SаО2 > 90% (Ра О2 > 60 мм рт.ст.). При необходимости проводится неинвазивная вентиляция легких.
Бронходилатирующая терапия при обострении ХОБЛ требует интенсификации, что достигается увеличением доз и модификацией способов доставки препаратов. Препаратами первого ряда являются БА КД (сальбутамол, фенотерол) и АХП КД (ипратропия бромид), вводимые в максимальных дозах с помощью небулайзера или спейсера. При лечении тяжелых обострений показана комбинация препаратов указанных классов.
Характеристика режимов дозирования ингаляционных препаратов при обострениях ХОБЛ приведен в таблице 5.
Таблиця 5
Режимы дозирования ингаляционных бронходилататоров при обострениях ХОБЛ
|
Препарат |
Лечебный режим в период обострения |
|
|
ДАИ |
Небулайзер |
|
|
БАКД |
||
|
Сальбутамол ДАИ, 100 мкг; Небулы, р-р для ингаляций, 2,5 мл, 1 мг/мл |
2-4 вдоха каждые 20-30 мин в течение первого часа, затем каждые 1-4 час («по потребности»), затем каждые 4-6 час |
2,5-,0 мг каждые 20-30 мин в течение первого часа, затем 2,5−10,0 мг каждые 1-4 час («по потребности»), затем каждые 6-8 часов |
|
Фенотерол ДАИ, 100 мкг |
2-4 вдоха каждые 30 хв в течение первого часа, затем каждые 1-4 час («по потребности») |
0,5-1,0 мг каждые 20-30 хв в течение первого часа, затем 0,5-1,0 мг каждые 1-4 час («по потребности») |
|
АХП КД |
||
|
Ипратропия бромидДАИ, 40 мкг |
2-4 вдоха дополнительно к ингаляциям сальбутамола или фенотерола |
0,5 мг дополнительно к ингаляциям сальбутамола или фенотерола |
|
Фиксированные комбинации β2-агониста КД и АХП КД |
||
|
Фенотерол ипратро- пия бромид ДАИ, р-р для ингаляций |
2-4 вдоха каждые 30 мин, затем каждые 1-4 час («по потребности») |
1-2 мл каждые 30 мин в течение первого часа, (максимальная доза 4 мл), затем 1,5-2 мл каждые 1-4 час («по потребности») |
|
Сальбутамол ипратропия бромидДАИ, 100 20 мкг |
2-4 вдоха каждые 30 мин, затем каждые 1-4 час («по потребности») |
|
Примечание: ДАИ дозированный аэрозольный ингалятор, ПИ – порошковый ингалятор
Наряду с применением БА КД (сальбутамол, фенотерол) и/или АХП КД (ипратропия бромид) в указанных дозировках при обострении ХОБЛ параллельно должны быть назначены системные ГК – 30-40 мг преднизолона или других ГК в эквивалентных дозировках внутрь или парентерально в течение 7-10 дней. Применение системных ГК способствует более быстрому увеличению ОФВ1, уменьшению одышки, улучшению оксигенации артериальной крови, сокращению сроков госпитализации. Эффективность системных ГК проявляется также в снижении на 50% риска неудачного исхода лечения.
Применение внутривенных форм теофиллина при обострениях ХОБЛ большинством экспертов не поддерживается, поскольку в контролированых исследованиях эффективность его при обострениях ХОБЛ оказалась низкой, а его применение сопровождалось высоким риском серьезных токсических эффектов.
Антибактериальная терапия.
Обоснованием к назначению антибактериальной терапии при обострении ХОБЛ является инфекционный его генез (связь с инфекцией респираторного тракта).
Для решения относительно назначения антибиотиков при обострепнии ХОБЛ нередко используют подход N. Anthonisen, который рассматривая в качестве «больших» критериев обострения ХОБЛ 1) усиление одышки, 2) увеличение продукции мокроты и 3) ее гнойный характер, выделяет три типа обострений:
- I тип характеризуется наличием всех 3 “критериев” обострения ХОБЛ (усиление одышки, увеличение объема мокроты, появление или усиление гнойного ее характера). Антибактермальная терапия при этом типе обострения обычно высокоэффективна.
- II тип сопровождается наличием только 2 из вышеуказанных критериев. При этом антибактериальная терапия достаточно эффективна и показана, если один из этих симптомов – увеличение «гнойности» мокроты.
- III тип – может включать только 1 из “критериев” в комбинации с острыми катаральными симптомами инфекции верхних дыхательных путей и/или лихорадкой и/или усилением кашля и/или повышением на 20% и более частоту дыхательных двидений (ЧДД) или частоту сердечных сокращений (ЧСС). При таком типе обстрения антибактериальная терапия обычно малоэффективна и не показана!
В большинстве случаев обострений ХОБЛ антибиотики назначаются внутрь. Продолжительность антибактериальной терапии больных с обострением ХОБЛ составляет, как правило, 5-7, реже 10 дней.
Выбор антибактериальных препаратов при обострениях ХОБЛ базируется на клинической оценке больных. Так, у больных моложе 65 лет, с частотой обострений ХОБЛ менее 4 раз в год, при отсусттвии сопутствующих заболеваний и ОФВ1 более 50 % от должных значений (основные возбудители H. influenzae, S. pneumoniae, M. catarrhalis и атипичные микроорганизмы) в качестве антибиотика выбора рекомендуют аминопенициллин (амоксициллин) или макролид. При неэффективности бета-лактамов и макролидов, или аллергии к ним назначается перорально респираторный фторхинолон.
У пациентов старше 65 лет с наличием сопутствующих заболеваний и ОФВ1 в пределах 30-50% (основные возбудители H. influenzae і S. рneumoniae, несколько увеличивается участие Enterobacteriaceae) препаратами выбора являеются пероральные защищенные аминопенициллины (амоксициллинклавуланат) или цефалоспорины 2-3 поколения (цефуроксим, цефалексин, цефтриаксон). В случае необходимости возможно использование цефалоспоринов парентерально. Препаратом второй линии является респираторный фторхинолон для перорального приема.
При ОФВ1 менее 30 % от должных значений, частых (более 4 раз в год) курсах антибактериальной терапии, наличии бронхоэктазов, постоянном приеме ГК, кахексии высока вероятность в качестве возбудителя P. aeruginosae. В связи с этим рекомендуется парентеральное использование комбинации антибактериальных препаратов: 1) фторхинолон II поколения (ципрофлоксацин или респираторный фторхинолон левофлоксацин в комбинации с β-лактамами с антисинегнойной активностью (преимущество имеют цефоперазон, цефтазидим) или 2) β-лактам с антисинегнойной активностью (цефоперазон, цефтазидим) в комбинации с аминогликозидом.
Таким образом, алгоритм терапии обострения ХОБЛ должен включать назначение:
- ингаляционных бронходилататоров (БА КД или АХП КД или их комбинации) в режиме высоких доз, с использованием спейсера или небулайзера;
- системных ГК в дозах, эквивалентных 30-40 мг преднизолона внутрь или парентерально в течение 7-10 дней без необходимости постепенного уменьшения дозы.
- антибактериальных препаратов при наличии гнойной мокроты.
Тактика и условия наблюдения при обострении ХОБЛ
При легком или умеренно тяжелом обострении ХОБЛ больные могут лечиться амбулаторно.
Показаниями к госпитализации в общетерапевтический стационар служат следующие клинические ситуации:
- пожилой возраст (65 лет и более)
- тяжелые сопутствующие заболевания (сахарный диабет, гипотиреоз, хронические заболевания сердца, почек, печени и т.д.)
- тяжелое течение ХОБЛ
- отчетливое ухудшение состояния (увеличение ЧСС или ЧДД на 20 % от исходных, появление одышки в покое, признаков правожелудочковой недостаточности кровообращения (цианоз, периферические отеки)
- возникшие впервые нарушения сердечного ритма и/или признаки левожелудочковой сердечной недостаточности
- недостаточная эффективность «амбулаторной» терапии
- выраженная лихорадка
- диагностические сложности (подозрение на пневмонию, плеврит, ТЭЛА)
- невозможность адекватного лечения в домашних условиях.
Госпитализации больных ХОБЛ в ОРИТ подлежат больные при наличии следующих критических ситуаций:
- ЧДД ≥ 30 /мин або < 16 / мин с ослабленным («ватным») дыханием или признаками утомления дыхательных мышц (альтернирующее или парадоксальное дыхание);
- тяжелая гипоксемия и респираторныйацидоз
- неэффективная (или недоступная) неинвазивная оксигенотерапия
- нарушения ментальных функций пациента (ажитация, депрессия, снижение критичности оценки собственного состояния, утрата контакта с родными, неспособность к сотрудничеству с медицинским персоналом),
- лицевая травма, ожоги, анатомические нарушения, которые препятствуют наложению маски для оксигенотерапии
- гемодинамическая нестабильность (тенденция к снижению АД) и другие критические состояния (септический шок, массивная пневмония, ТЭЛА, баротравма, гидроторакс, пневмоторакс, нарушения глотания)
- развитие гипоксической /гиперкапнической комы на фоне постоянной оксигенотерапии, приема лекарственных препаратов снотворного, транквилизирующего, диуретического действия, диабета, электролитных нарушений, сниженного питания






