Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "Антибактериальная терапия тонзиллофарингита"
Автор: И.Г. Березняков
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: ЛОР, Семейная медицина/Терапия
Просмотров: 3 494
Дата проведения:
Введение
Тонзиллит (ангина) представляет собой инфекционное поражение паренхимы небных миндалин. Он может встречаться как изолированно, так и быть частью генерализованного фарингита. Ввиду отсутствия четких клинических различий между тонзиллитом и фарингитом в литературе нередко используется термин «тонзиллофарингит».
Оценить истинную распространенность тонзиллофарингита затруднительно. По данным зарубежных исследований (Австралия, Великобритания), примерно 10% населения обращается ежегодно за медицинской помощью по поводу этого заболевания. Острый тонзиллофарингит чаще регистрируется у детей.
Актуальность проблемы тонзиллофарингита объясняется не только распространенностью заболевания и связанными с ним временной утратой трудоспособности и невозможностью посещать учебные заведения, но и нередким развитием инфекционных (перитонзиллярный абсцесс, флегмона шеи и др.) и неинфекционных осложнений (острая ревматическая лихорадка, острый постстрептококковый гломерулонефрит).
Этиология
Заболевание вызывается преимущественно вирусами (табл. 1) [1, 2]. Тем не менее, если возбудитель представлен единственным патогеном, то им чаще всего оказываются β-гемолитические стрептококки группы А (БГСА). Хотя в Международной классификации болезней X пересмотра выделяют стрептококковый фарингит (J02.0) и стрептококковый тонзиллит (J03.0), в данной публикации будет использоваться общий термин тонзиллофарингит (ТФ) – как для вирусных, так и для бактериальных заболеваний.
Таблица 1. Этиология острого фарингита
|
Микроорганизмы |
Клинический (-ие) синдром(-ы) |
|
Бактерии |
|
|
β-гемолитические стрептококки группы А |
Фарингит, тонзиллит, скарлатина |
|
Стрептококки группы C и G |
Фаринготонзиллит |
|
Arcanobacterium haemolyticum |
Скарлатиноформная сыпь, фарингит |
|
Neisseria gonorrhoeae |
Тонзиллофарингит |
|
Corynebacterium diphtheriae |
Дифтерия |
|
Смешанные анаэробы |
Ангина Симановского-Венсана |
|
Fusobacterium necrophorum |
Синдром Лемьера, перитонзиллярный абсцесс |
|
Francisella tularensis |
Туляремия (ротоглоточная) |
|
Yersinia pestis |
Чума |
|
Yersinia enterocolitica |
Энтероколит, фарингит |
|
Атипичные бактерии |
|
|
Mycoplasma pneumoniae |
Пневмонит, бронхит |
|
Chlamydophila pneumoniae |
Бронхит, пневмония |
|
Chlamydia psittaci |
Пситтакоз |
|
Спирохеты: |
|
|
Treponema pallidum |
Вторичный сифилис |
|
Вирусы |
|
|
Аденовирус |
Фарингоконъюнктивальная лихорадка |
|
Вирус простого герпеса 1 и 2 |
Гингивостоматит |
|
Вирус Коксаки |
Герпетическая ангина |
|
Риновирус |
Простуда |
|
Коронавирус |
Простуда |
|
Вирус гриппа А и В |
Грипп |
|
Вирус парагриппа |
Простуда, круп |
|
Вирус Эпштейна-Барра |
Инфекционный мононуклеоз |
|
Цитомегаловирус |
Цитомегаловирусный мононуклеоз |
|
Вирус иммунодефицита человека (ВИЧ) |
Первичная острая ВИЧ-инфекция |
 На долю БГСА приходится 5–15% случаев острого ТФ у взрослых и 20–30% у детей [3]. Заболевание в странах с умеренным климатом чаще возникает зимой и ранней весной.
На долю БГСА приходится 5–15% случаев острого ТФ у взрослых и 20–30% у детей [3]. Заболевание в странах с умеренным климатом чаще возникает зимой и ранней весной.
Из бактерий, помимо БГСА, внимания заслуживают следующие. Arcanobacterium haemolyticum редко вызывает острый ТФ, который может ассоциироваться со скарлатиноподобной сыпью, в особенности у подростков и молодых людей. У молодых сексуально активных людей изредка причинами острого ТФ могут быть гонококки (Neisseria gonorrhoeae). Атипичные бактерии – микоплазмы и хламидии – редко вызывают острый ТФ.
Стрептококки группы С – нередкие возбудители ТФ у студентов и взрослых. Кроме того, эти бактерии могут вызывать эпидемические вспышки острого ТФ при употреблении зараженной пищи, например непастеризованного коровьего молока. Описаны также вспышки ТФ, вызванного стрептококками группы С в семьях и в школьных коллективах. Этиологическая значимость стрептококков группы G остается неясной, несмотря на хорошо документированные вспышки ТФ, вызванного этими бактериями, у детей во внебольничных условиях и при употреблении зараженной пищи. В литературе нет описаний атак острой ревматической лихорадки после фарингитов, вызванных стрептококками групп С и G. Случаи острого гломерулонефрита после инфекций стрептококками группы С встречаются крайне редко, а связь этого заболевания с инфекциями стрептококками группы G остается недоказанной. Целесообразность антибактериальной терапии (АБТ) при ТФ, вызванных двумя этими группами стрептококков, в клинических исследованиях должным образом не изучена.
- F. necroforum – грамотрицательная анаэробная бактерия, которая является частью нормальной микрофлоры полости рта, мочеполовых путей и пищеварительного тракта. Тем не менее, она может быть патогенной и вызывать ТФ, синусит, аппендицит, абсцессы и эндокардит [4]. F. necroforum ассоциируется также с синдромом Лемьера, который представляет собой септический тромбофлебит внутренней яремной вены и сопровождается метастатическими инфекциями. Последние почти всегда поражают легкие, но могут охватывать также суставы, кости, печень, мягкие мозговые оболочки и головной мозг. Синдром чаще всего регистрируется у подростков и взрослых молодого возраста (до 30 лет), преимущественно у лиц мужского пола [5]. Согласно некоторым оценкам, у 1 из 400 пациентов с ТФ, вызванным F. necroforum, развивается синдром Лемьера [6]. В публикациях последних лет приводятся данные о высокой частоте обнаружения F. necroforum у больных с ТФ при исследовании мазков из ротоглотки методом полимеразной цепной реакции (ПЦР) [7].
 Следует ли включать идентификацию F. necroforum вместе со стрептококками группы А в качестве обязательных мер диагностики и лечения ТФ? По-видимому, нет. И дело не только в отсутствии в настоящее время соответствующих лабораторных тестов. Во-первых, данные, полученные с помощью ПЦР, не являются убедительными доказательствами инфекции. Золотым стандартом для подтверждения инфекции ротоглотки (хотя и неприменимым для рутинных клинических нужд) остаются серологические исследования парных сывороток, полученных в острой фазе заболевания и в период выздоровления. Обычный вирусный ТФ может привести к изменению микрофлоры ротоглотки и обусловить повышение частоты выделения F. necroforum. Во-вторых, отсутствует четкая корреляция между ТФ, вызванным F. necroforum, и синдромом Лемьера, который может осложнять также мастоидит, отит, перитонзиллярные абсцессы и инфекции полости рта. Кроме того, хотя F. necroforum и является самым частым возбудителем синдрома Лемьера, его вызывают и другие виды микроорганизмов: Bacteroides, Eikenella, Streptococcus, Peptostreptococcus, Porphyromonas, Prevotella, Proteus и внебольничные штаммы Staphylococcus aureus. Наконец, нет никаких доказательств, что лечение ТФ, вызванного F. necroforum, способно предупредить развитие синдрома Лемьера [5].
Следует ли включать идентификацию F. necroforum вместе со стрептококками группы А в качестве обязательных мер диагностики и лечения ТФ? По-видимому, нет. И дело не только в отсутствии в настоящее время соответствующих лабораторных тестов. Во-первых, данные, полученные с помощью ПЦР, не являются убедительными доказательствами инфекции. Золотым стандартом для подтверждения инфекции ротоглотки (хотя и неприменимым для рутинных клинических нужд) остаются серологические исследования парных сывороток, полученных в острой фазе заболевания и в период выздоровления. Обычный вирусный ТФ может привести к изменению микрофлоры ротоглотки и обусловить повышение частоты выделения F. necroforum. Во-вторых, отсутствует четкая корреляция между ТФ, вызванным F. necroforum, и синдромом Лемьера, который может осложнять также мастоидит, отит, перитонзиллярные абсцессы и инфекции полости рта. Кроме того, хотя F. necroforum и является самым частым возбудителем синдрома Лемьера, его вызывают и другие виды микроорганизмов: Bacteroides, Eikenella, Streptococcus, Peptostreptococcus, Porphyromonas, Prevotella, Proteus и внебольничные штаммы Staphylococcus aureus. Наконец, нет никаких доказательств, что лечение ТФ, вызванного F. necroforum, способно предупредить развитие синдрома Лемьера [5].
Микробиологическая диагностика острого стрептококкового ТФ
В соответствии с современными представлениями, БГСА является единственными распространенным возбудителем ТФ, при выделении которого всегда назначается антибактериальная терапия. Поэтому микробиологическая диагностика ТФ сводится, по существу, к получению ответа на единственный вопрос: возбудители заболевания – пиогенные стрептококки или нет?
В настоящее время для подтверждения стрептококковой этиологии ТФ применяют культуральные исследования материала, полученного из зева пациента, или экспресс-тестирование.
 Для микробиологического исследования пригоден материал, полученный с помощью тампона с поверхности миндалин, из устьев крипт миндалин и с задней стенки глотки. Следует строго придерживаться техники получения образцов: не прикасаться тампоном к другим участкам слизистой оболочки до и после забора материала и не забирать мазок вскоре после приема пищи (во время еды микроорганизмы механически удаляются с поверхности слизистой) [8]. Ограничениями культурального исследования являются ожидание ответа в течение 2-3 дней после забора материала и малая доступность должным образом оснащенных микробиологических лабораторий с квалифицированным персоналом.
Для микробиологического исследования пригоден материал, полученный с помощью тампона с поверхности миндалин, из устьев крипт миндалин и с задней стенки глотки. Следует строго придерживаться техники получения образцов: не прикасаться тампоном к другим участкам слизистой оболочки до и после забора материала и не забирать мазок вскоре после приема пищи (во время еды микроорганизмы механически удаляются с поверхности слизистой) [8]. Ограничениями культурального исследования являются ожидание ответа в течение 2-3 дней после забора материала и малая доступность должным образом оснащенных микробиологических лабораторий с квалифицированным персоналом.
Экспресс-тесты позволяют быстро – в течение нескольких минут – дать заключение о наличии или отсутствии антигенов стрептококков в мазке из горла. Именно они рекомендуются в качестве первого шага на пути этиологической диагностики ТФ. При отрицательных результатах теста у детей и подростков рекомендуется контрольный посев мазка из глотки. У взрослых подтверждать отрицательные результаты экспресс-теста с помощью посевов, как правило, не требуется [2]. Доступность экспресс-диагностики позволит существенно сократить случаи неразумного использования антибиотиков у больных ТФ.
Клиническая картина и показания к назначению антибиотиков
Острый ТФ, вызванный БГСА, отличается от вирусного некоторыми эпидемиологическими и клиническими особенностями (табл. 2), хотя дифференциальная диагностика между ними затруднительна. По мнению экспертов Американского общества инфекционистов (IDSA), ни один из предложенных наборов клинических критериев не позволяет с уверенностью диагностировать стрептококковый ТФ, в особенности у детей. Ни один даже самый опытный врач не способен с определенностью поставить такой диагноз, поэтому необходимо бактериологическое подтверждение [2].
Таблица 2. Эпидемиологические и клинические признаки, характерные для БГСА- и вирусного тонзиллофарингитов
|
БГСА-тонзиллофарингит |
Вирусный ТФ |
|
Внезапное начало ТФ |
Конъюнктивит |
|
Возраст 5–15 лет |
Насморк |
|
Лихорадка |
Кашель |
|
Головная боль |
Диарея |
|
Тошнота, рвота, боли в животе |
Охриплость |
|
Воспаление миндалин и глотки |
Язвенный стоматит |
|
Фрагментарные тонзиллофарингеальные экссудаты |
Экзантема |
|
Лимфаденит передних шейных лимфатических узлов (болезненные лимфоузлы) |
|
|
Возникновение зимой или в начале весны |
|
|
Анамнестические указания на контакт с больными стрептококковым ТФ |
|
|
Скарлатиноформная сыпь |
|
Подобный подход оправдан, когда экспресс-тесты широко доступны и затраты на их использование возмещаются государством, как например во Франции. С другой стороны, разработаны клинические критерии, которые с разной степенью вероятности позволяют предсказывать возможную стрептококковую этиологию ТФ и решать вопрос о назначении антибиотиков. Наибольшей известностью пользуются модифицированные МакАйзеком критерии Сентора (рис. 1) [9, 10]. При наличии каждого из первых четырех критериев больному присваивается 1 балл, затем баллы суммируются. Если пациентом является ребенок в возрасте от 3 до 14 лет, добавляется еще 1 балл, если взрослый 45 лет и старше – 1 балл отнимается, если подросток старше 14 лет или молодой взрослый (до 44 лет включительно), исходная сумма баллов остается неизменной. Тактика ведения пациентов с ТФ в зависимости от результатов использования критериев МакАйзека представлена на рисунке 2 [11].

Рисунок 1. Критерии МакАйзека
Эксперты Европейского общества по клинической микробиологии и инфекционным заболеваниям (ESCMID) высоко оценивают пользу от использования модифицированных критериев Сентора, однако признают, что у детей первых лет жизни она ниже, чем у взрослых – из-за различий в особенностях клинических проявлений ТФ в разные возрастные периоды [12].
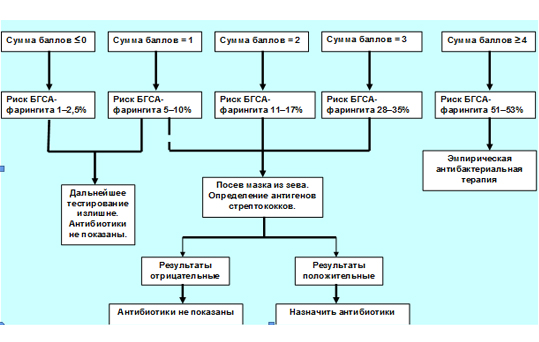
Рисунок 2. Ведение больных ТФ с использованием критериев МакАйзека
Антибактериальная терапия
Среди всех больных с ТФ, которые обращаются за медицинской помощью, на долю стрептококков группы А приходится порядка 10% случаев. Тем не менее, распространенной практикой остается не только чрезмерное назначение антибиотиков для лечения ТФ, но и ошибочный выбор препаратов. Например, в США в 1997–2010 гг. антибиотики назначали в 60% случаев обращений за помощью по поводу ТФ, причем только в 9% обращений выписывали пенициллины. При этом азитромицин назначался в 1,5 раза чаще (в 15% случаев), а еще в 15% обращений врачи выписывали другие нерекомендуемые антибиотики: цефалоспорины II и III поколений, ингибиторозащищенные пенициллины, фторхинолоны [13].
Большинство специалистов сходятся во мнении, что больных с 4 или 5 баллами по критериям МакАйзека следует сразу же лечить антибиотиками (хотя вероятность стрептококкового ТФ лишь ненамного превышает 50%). У пациентов с 3 баллами по критериям МакАйзека вероятность стрептококковой этиологии ТФ еще ниже – в пределах одной трети-одной четверти. Однако и в этом случае назначение антибиотиков многими экспертами рассматривается как оправданное. В остальных случаях (когда количество баллов составляет от 0 до 2) АБТ не рекомендуется [12].
У больных с нетяжелыми и склонными к спонтанному разрешению инфекциями (такими как ТФ) альтернативами срочной антибактериальной терапии (т.е. назначенной сразу после постановки диагноза) может быть отсроченное (отложенное) использование антибиотиков, которое, в частности, рекомендуется экспертами ESCMID [12]. Для обоснования такого подхода приводят данные авторов Кокрановского сотрудничества о том, что примерно у 50% нелеченных больных острым ТФ (ангиной) симптоматика исчезает уже через 3,5 дня, а спустя 1 неделю от начала заболевания симптомы отсутствуют почти у 90% пациентов, как получавших, так и не получавших антибиотики [14].
Эффективность отложенного применения антибиотиков при инфекциях дыхательных путей изучена авторами Кокрановского сотрудничества [15]. В окончательный анализ вошли 10 рандомизированных клинических исследований (РКИ), причем 4 из них выполнены у больных ТФ. Под отложенным (отсроченным) применением антибиотиков понимали использование или совет использовать эти медикаменты не ранее чем через 48 ч после первоначальной консультации, под срочной АБТ – немедленный прием антибиотика, выписанного на исходной консультации.
Хотя авторы обзора подтвердили эффективность и безопасность отложенного приема антибиотиков и высокую удовлетворенность больных лечением (или их родственников/опекунов) при использовании этой технологии при нетяжелых инфекциях дыхательных путей, складывается впечатление, что при ТФ эффективность срочной АБТ может быть выше. Так, у больных фарингитом/ангиной в одних исследованиях срочная АБТ превосходила отложенное применение антибиотиков, в других – различия не были найдены (табл. 3). Характеристика включенных в исследования пациентов, выбор и критерии оценки клинических исходов во многих РКИ различались, поэтому мета-анализ оказался возможным только в отношении лихорадки (рис. 3). Вероятность того, что на 3-й день заболевания лихорадка будет оставаться тяжелой, почти в 2 раза ниже в случае использования срочной АБТ.
Таблица 3. Сравнение клинических исходов у больных ТФ при использовании отложенного применения антибиотиков и срочной АБТ
|
Клинические исходы |
В пользу срочной АБТ |
В пользу отложенного применения антибиотиков |
Обе технологии сопоставимы |
|
Боли на 3-й день |
1 РКИ |
|
|
|
Боли |
|
|
3 РКИ |
|
Недомогание на 3-й день |
1 РКИ |
|
|
|
Недомогание |
|
|
1 РКИ |
|
Число дней с лихорадкой |
1 РКИ |
|
1 РКИ |

Рисунок 3. Тяжесть лихорадки у больных ТФ
Кроме того, в реальной клинической практике, когда у врача просто не хватает времени на подробное разъяснение больному достоинств и недостатков отложенного использования антибиотиков, удовлетворенность лечением может быть выше в том случае, если антибиотики назначены сразу. Поэтому срочная АБТ у пациентов с ТФ при наличии 3 и более баллов по критериям МакАйзека представляется наиболее оправданной.
В сравнительных исследованиях с плацебо продемонстрирована способность антибиотиков сокращать продолжительность симптомов ТФ примерно на 16 ч и предупреждать возникновение инфекционных и постинфекционных осложнений [16]. Через 3 дня лечения симптомы чаще всего исчезают у больных с подтвержденной при микробиологическом исследовании стрептококковой этиологией заболевания: условное число пациентов, которых необходимо пролечить антибиотиками для исчезновения симптомов ТФ у 1 человека, равно 3,7. Пользу от использования антибиотиков получают и больные ТФ с отрицательными результатами микробиологического исследования (соответствующий показатель равен 6,5) и даже те, у кого такие исследования никогда не проводились (показатель равен 14,4).
Лечение больных ТФ антибиотиками позволяет сократить число случаев перитонзиллярного абсцесса примерно в 7 раз, острого среднего отита – в 3,5 раза, острой ревматической лихорадки – также в 3,5 раза [16]. Переоценивать эти данные не следует. Например, частота острого среднего отита как вторичного осложнения острого ТФ сократилась в развитых странах с 3% до 1975 г. до 0,7% в 2013 г. В результате для предупреждения 1 случая острого среднего отита количество больных ТФ, которых необходимо пролечить антибиотиками, возросло с 50 почти до 200 [16].
Препаратами выбора при лечении ТФ являются пенициллины. Несмотря на 75-летнее использование пенициллина в клинической практике, пиогенные стрептококки (БГСА) сохраняют к ним 100%-ную чувствительность. Так, в России за 10-летний период протестировали 860 штаммов БГСА, и все они были чувствительны к пенициллину (рис. 4). Высокая чувствительность сохраняется у БГСА к гликопептидам, оксазолидинонам, респираторным фторхинолонам, ко-тримоксазолу, макролидам (прежде всего, 16-членным, таким как джозамицин) (рис. 5) [17].
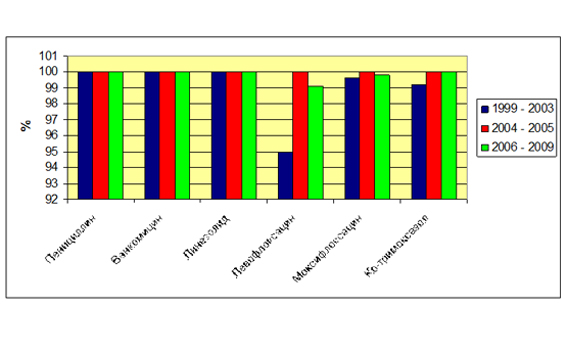
Рисунок 4. Чувствительность S. pyogenes к антибиотикам разных групп (Россия, 1999–2009 гг.)
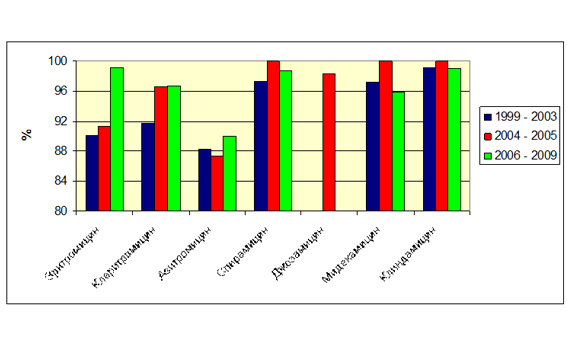
Рисунок 5. Чувствительность S. pyogenes к макролидам (Россия, 1999–
2009 гг.)
Рекомендации по АБТ БГСА-тонзиллофарингита представлены в табл. 4. В ней отсутствует феноксиметилпенициллин, который обычно упоминается в руководствах, изданных в США и Европейском союзе. Этот кислотоустойчивый пенициллин с узким спектром активности для приема внутрь уже много лет как не зарегистрирован в Украине. Вместо него у детей обычно используется амоксициллин – при сопоставимой эффективности растворенная в воде диспергируемая таблетка или суспензия этого антибиотика обладают лучшими вкусовыми качествами. При этом сам процесс растворения диспергируемой таблетки существенно быстрее и проще приготовления суспензии из порошка амоксициллина.
Таблица 4. Антибактериальная терапия БГСА-тонзиллофарингита
|
Препарат, путь введения |
Дозирование |
Длительность или количество |
|
Больные без аллергии на пенициллин |
||
|
Амоксициллин внутрь |
50 мг/кг 1 раз в сутки (максимум 1000 мг); альтернатива: 25 мг/кг (максимум 500 мг) 2 раза в сутки |
10 дн. |
|
Бензатинбензилпенициллин в/м |
< 27 кг: 600.000 ЕД; ³ 27 кг: 1,2 млн. ЕД |
1-кратно |
|
Больные с анамнестическими указаниями на аллергию на пенициллин |
||
|
Цефалексин1 внутрь |
20 мг/кг (максимум 500 мг) 2 раза в сутки |
10 дн. |
|
Цефадроксил1 внутрь |
30 мг/кг 1 раз в сутки (максимум 1,0 г) |
10 дн. |
|
Клиндамицин внутрь |
7 мг/кг (максимум 300 мг) 3 раза в сутки |
10 дн. |
|
Азитромицин внутрь |
12 мг/кг 1 раз в сутки (максимум 500 мг) |
5 дн. |
|
Кларитромицин внутрь |
7,5 мг/кг (максимум 250 мг) 2 раза в сутки |
10 дн. |
Примечания: в/м – внутримышечно; 1 – избегать у больных с аллергическими реакциями немедленного типа на пенициллин.
В сравнительных клинических исследованиях (КИ) доказана эффективность приема амоксициллина в дозе 50 мг/кг (максимум 1000 мг) 1 раз/сутки на протяжении 10 дней, что выгодно с точки зрения удобства дозирования и сравнительно невысокой цены.
Из всех лекарственных форм для приема амоксициллина внутрь (таблетки, капсулы, порошок для приготовления суспензии и др.) наиболее удобными являются диспергируемые таблетки. Их преимущества можно суммировать так:
- антибиотик, заключенный в кислотоустойчивые микрогранулы, не разрушается под действием желудочного сока;
- максимальная биодоступность препарата (93%) и минимальное нарушение микроэкологии кишечника;
- удобство приема (таблетка проглатывается целиком или растворяется в воде);
- возможность визуально проконтролировать процесс растворения (таблетка быстро распадается на гранулы без выделения газа) и убедиться в подлинности препарата;
- приятные органолептические свойства.
Большинство антибиотиков для приема внутрь назначаются сроком на 10 дней для достижения максимальной эрадикации (уничтожения) БГСА. При наличии сомнений в том, что пациент завершит предписанный 10-дневный курс лечения, адекватной альтернативой представляется однократное парентеральное введение бензатинбензилпенициллина. В последние годы FDA (Американская администрация по контролю продуктов питания и лекарственных средств) одобрила 5-дневные курсы цефдинира (в Украине не зарегистрирован), цефподоксима проксетила и азитромицина для лечения БГСА-фарингита. Однако спектр активности пероральных цефалоспоринов шире, а стоимость, даже при 5-дневном курсе, выше, чем соответствующие характеристики амоксициллина, в связи с чем, например, эксперты IDSA в настоящее время воздерживаются от рекомендации их к широкому внедрению в практику.
У большинства больных с анамнестическими указаниями на аллергию на пенициллин используют пероральные цефалоспорины. Цефалоспорины I поколения цефадроксил или цефалексин предпочтительнее пероральных цефалоспоринов с более широким спектром действия (цефуроксим аксетил, цефподоксим проксетил и др.), которые существенно дороже и в большей степени способствуют селекции резистентной флоры. До 10% лиц с повышенной чувствительностью к пенициллину страдают также аллергией на цефалоспорины, поэтому последние не следует применять у больных с повышенной чувствительностью к пенициллину немедленного типа (анафилактическими реакциями на пенициллин).
Резистентность БГСА к клиндамицину невелика, поэтому данный препарат разумно использовать для лечения больных с анамнестическими указаниями на аллергию на пенициллин. В подобных случаях могут применяться и макролиды. Распространение резистентности БГСА к макролидам ассоциируется с возможными клиническими неудачами лечения [2]. Наиболее перспективными из этого класса антибиотиков для лечения ТФ являются 16-членные макролиды (джозамицин и др.). Устойчивость БГСА к макролидам обусловлена либо модификацией мишени, на которую действуют антибиотики, либо активным изгнанием макролидов, проникших внутрь бактерии, наружу с помощью бактериальных насосов. В первом случае клинически неэффективными становятся все макролиды, во втором – только 14- и 15-членные. Поэтому чувствительность БГСА к 16-членным макролидам обычно выше. Джозамицин, кстати, также выпускается в виде диспергируемых таблеток.
Причинами повторных эпизодов ТФ, которые развиваются спустя недели или месяцы после первого, могут быть: 1) некомплаентность по отношению к ранее предписанной АБТ; 2) новая БГСА-инфекция глотки, приобретенная от домочадцев или во внебольничных условиях (включая одноклассников); 3) хроническое носительство БГСА с интеркуррентной вирусной инфекцией. Повторное заболевание ТФ, вызванным первоначальным штаммом БГСА, также возможно, но встречается значительно реже.
Хроническое носительство БГСА в глотке не сопровождается активной реакцией иммунной системы организма, например, повышением титра антистрептококковых антител. В странах с умеренным климатом в холодное время года до 20% бессимптомных школьников становятся хроническими носителями БГСА, причем на протяжении ³ 6 мес., и в это время могут переболеть интеркуррентным вирусным фарингитом. Риск передачи БГСА хроническими носителями лицам, находящимся в тесном контакте с ними, невелик, а риск развития гнойных и негнойных осложнений – минимальный, либо отсутствует. Большинству хронических носителей стрептококков АБТ не показана, за исключением следующих случаев: 1) во время внебольничной вспышки острой ревматической лихорадки, острого гломерулонефрита или инвазивной БГСА-инфекции; 2) во время вспышки БГСА-тонзиллофарингита в замкнутых или полуоткрытых сообществах; 3) в случаях предшествующих атак острой ревматической лихорадки у пациента или членов семьи; 4) в семьях, чрезмерно обеспокоенных по поводу БГСА-инфекции; 5) если рассматривается целесообразность тонзиллэктомии исключительно в связи с носительством БГСА. В подобных случаях могут использоваться 10-дневные курсы пероральной АБТ клиндамицином по 20–30 мг/кг/сут. в 3 приема (максимальная разовая доза – 300 мг) или амоксициллином/клавуланатом по 40 мг/кг/сут. (по амоксициллину) в 3 приема (максимум – 2,0 г амоксициллина в сутки), лучше – в виде диспергируемых таблеток. Добавление клавуланата к амоксициллину не повышает активность антибиотика в отношении БГСА, которые не вырабатывают β-лактамазы, но дает ему возможность проявить антибактериальное действие в отношении анаэробов.
В рутинной клинической практике разграничивать больных с БГСА-тонзиллофарингитом и хронических носителей БГСА с интеркуррентным вирусным фарингитом нелегко. Определенную помощь могут оказать возраст пациента, время года, местная эпидемиологическая ситуация (например, локальная распространенность гриппа и/или энтеровирусных заболеваний), а также клинические особенности заболевания (табл. 2).
Тем не менее, во многих случаях дифференциальная диагностика между БГСА-тонзиллофарингитом и хроническим носительством БГСА невозможна. У больных ТФ с микробиологически подтвержденным повторным эпизодом БГСА-инфекции вскоре после завершения адекватной АБТ по поводу предшествующего эпизода, назначают любой антибиотик из числа представленных в таблице 4. В связи с нередкой сомнительной комплаентностью по отношению к пероральной АБТ можно использовать 1-кратное внутримышечное введение бензатинбензилпенициллина. После завершения терапии таких повторных эпизодов нет необходимости во взятии образцов для культурального исследования, за исключением случаев сохранения или возобновления симптомов.
Еще более сложную проблему представляют пациенты (обычно школьники или подростки) с многократными рецидивами БГСА-тонзиллофарингита, подтвержденного микробиологически или с помощью экспресс-теста. Во многих случаях они оказываются хроническими носителями БГСА, переносящими интеркуррентные вирусные ТФ. В настоящее время нет РКИ, где бы тестировалось лечение больных с повторными культурально-позитивными рецидивами острого ТФ. Однако при использовании 10-дневных курсов клиндамицина или амоксициллина/клавуланата частота бактериологических неудач невелика. Постоянная антибиотикопрофилактика не рекомендуется, за исключением случаев профилактики повторных атак острой ревматической лихорадки у пациентов с анамнестическими указаниями на подобные атаки.
У больных, у которых частота фарингитов, сопровождающихся симптомами, не снижается с течением времени, можно прибегнуть к тонзиллэктомии. Однако эффективность такого вмешательства была продемонстрирована только у сравнительно небольшой группы таких пациентов [2].
Следует ли применять антибиотики после тонзиллэктомии?
От 12% лор-врачей в Великобритании до 79% в США рутинно применяют антибиотики после тонзиллэктомии. В пользу их назначения обычно выдвигаются следующие аргументы:
- у большинства пациентов боли после тонзиллэктомии сохраняются более 7 дней;
- в сроки от нескольких часов до нескольких дней больные не могут вернуться к привычным жизнедеятельности и питанию;
- частота послеоперационных кровотечений составляет 2–40% [18].
По существу, ни один из представленных доводов не доказывает наличие бактериальной инфекции и не обосновывает необходимость применения антибиотиков. Авторы Кокрановского сотрудничества проанализировали данные 10 РКИ применения антибиотиков после тонзиллэктомии у 1025 детей и взрослых. Назначение антибиотиков ассоциировалось с уменьшением лихорадки, но не влияло на частоту вторичных кровотечений. При этом в группе больных, получавших антибиотики, увеличивалась частота побочных эффектов, хотя различия с группой плацебо не достигли статистической значимости (рис. 6) [18].
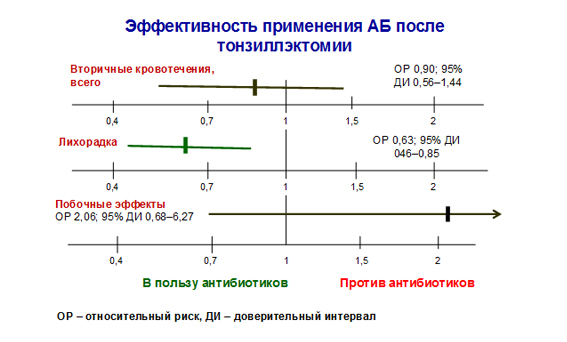
Рисунок 6. Антибиотики после тонзиллэктомии
Таким образом, рутинно применять антибиотики после тонзиллэктомии не следует. Они не являются жаропонижающими средствами (для этого достаточно медикаментов других классов), а иных аргументов в пользу использования антибиотиков нет.
Заключение
Основными возбудителями острых ТФ являются вирусы. На долю тонзиллофарингитов (ангин), вызванных БГСА, приходится примерно 10% случаев. Антибактериальная терапия показана при наличии у пациента 3-х и более критериев МакАйзека. Препаратом выбора является амоксициллин, который назначается внутрь в дозе до 1,0 г/сут. в 1–2 приема сроком на 10 дней, лучше – в виде диспергируемых таблеток.
Литература:
- Bisno A.L. Acute pharyngitis. N. Engl. J. Med. 2001; 344: 205-11.
- Shulman S.T., Bisno A.L., Clegg H.W., et al. Clinical practice guideline for the diagnosis and management of group A streptococcal pharyngitis: 2012 update by the Infectious Diseases Society of America. Clin. Infect. Dis. 2012; 55 (10): e86–102.
- Ebell M.H., Smith M.A., Barry H.C., et al. The rational clinical examination. Does this patient have strep throat? 2000; 284: 2912-8.
- Kuppalli K., Livorsi D., Talati N.J., Osborn M. Lemierre’s syndrome due to Fusobacterium necrophorum. Lancet Infect. Dis. 2012; 12: 808-15.
- Linder J.A. Sore throat: avoid overcomplicating the uncomplicated. Intern. Med. 2015; 162: 311-312.
- Centor R.M. Expand the pharyngitis paradigm for adolescents and young adults. Intern. Med. 2009; 151: 812-5.
- Centor R.M., Atkinson T..P, Ratliff A.E., et al. The clinical presentation of Fusobacterium–positive pharyngitis and streptococcal–positive pharyngitis in a university health clinic. A cross-sectional study. Ann. Intern. Med. 2015; 162: 241-7.
- Отвагин И.В., Соколов Н.С. Современные аспекты диагностики инфекций, вызванных стрептококками группы А. Клин. микробиол. антимикроб. химиотер. 2011; 13 (3): 223-230.
- Centor R.M., Witherspoon J.M., Dalton H.P., et al. The diagnosis of strep throat in adults in the emergency room. Med. Decis. Making 1981; 1: 239–246.
- McIsaac W.J., White D., Tannenbaum D., Low D.E. A clinical score to reduce unnecessary antibiotic use in patients with sore throat. Can. Med. Assoc. J. 1998; 158: 75–83.
- McIsaac W.J., Kellner J.D., Aufricht P., et al. Empirical validation of guidelines for the management of pharyngitis in children and adults. JAMA 2004; 291: 1587–1595.
- Pelucchi C., Grigoryan L., Galeone C., et al. Guideline for the management of acute sore throat. ESCMID Sore Throat Guideline Group. Clin. Microbiol. Infect. 2012; 18 (Suppl. 1): 1–27.
- Barnett M.L., Linder J.A. Antibiotic prescribing to adults with sore throat in the United States, 1997-2010. JAMA Intern. Med. 2014; 174: 138-40.
- Del Mar C.B., Glasziou P.P., Spinks A.B. Antibiotics for sore throat. Cochrane Database Syst. Rev. 2006; (4): CD000023.
- Spurling G.K.P., DelMar C.B., Dooley L., et al. Delayed antibiotics for respiratory infections. Cochrane Database Syst. Rev. 2013; (4): CD004417.
- Spinks A., Glasziou .P.P, Del Mar C.B. Antibiotics for sore throat. Cochrane Database Syst Rev. 2013; (11): CD000023.
- Азовскова О.В., с соавт., исследовательская группа «ПеГАС». Динамика антибиотикорезистентности респираторных штаммов Streptococcus pyogenes в России за период 1999–2009 гг. Клин. микробиол. антимикроб. химиотер. 2012; 14 (4): 309-21.
- Dhiwakar M., Clement W.A., Supriya M., McKerrow W. Antibiotics to reduce post-tonsillectomy morbidity. Cochrane Database Syst. Rev. 2012; (12):






