Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "Диагностика и лечение бронхиальной астмы в свете рекомендации GINA"
Автор: Вишнивецкий И.И., Дядык А.И.
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Пульмонология, Семейная медицина/Терапия
Просмотров: 4 082
Дата проведения: с 17.09.2014 по 17.09.2015
Бронхиальная астма (БА) – высоко распространенное заболевание, сопровождающееся значительной морбидностью, что делает ее серьезной медицинской и социально-экономической проблемой. По данным эпидемиологических исследований в мире около 300 млн. человек болеют БА. Однако истинная ее распространенность, очевидно, существенно превышает эту цифру, так как у значительного числа больных заболевание диагностируется с существенным запозданием. БА болеют лица обоего пола и всех возрастных групп. Она сопровождается значительными прямыми и непрямыми финансовыми затратами, снижением качества жизни, потерей трудоспособности, а при неадекватных лечебных подходах – увеличением летальности. В последние десятилетия в большинстве стран (особенно с низким экономическим уровнем) отмечается нарастание распространенности БА. Вместе с тем, в странах с высоким экономическим уровнем отмечена стабилизация распространенности заболевания и существенное снижение смертности, что объясняется некоторым уменьшением загрязненности окружающей среды, своевременной диагностикой и адекватным применением высокоэффективных лечебных подходов.
Настоящий семинар посвящен обсуждению диагностики, лечения и профилактики БА. Основные положения семинара соответствуют новой редакции рекомендаций Всемирной инициативы по борьбе с бронхиальной астмой (Global Initiative for Asthma, GINA) 2014 года. Основные нововведения данного пересмотра Рекомендаций GINA представлены:
- новой формулировкой определения БА, подчеркивающей ее гетерогенную природу и ключевые проявления в виде вариабельной симптоматики и вариабельной бронхиальной обструкции;
- акцентом на верификации диагноза БА во избежание как избыточной, так и недостаточной терапии;
- практическими инструментами для оценки контроля симптомов БА и факторов риска будущих осложнений;
- исчерпывающим подходом к ведению пациентов с БА, основывающемся на фундаментальной роли применения ингаляционных глюкокортикоидов (ИГК) с возможностями индивидуализации терапии на основе клинических и фенотипических особенностей, модифицируемых факторов риска и предпочтений пациентов;
- усилением роли оценки приверженности лечению и адекватности техники ингаляции перед расширением объема медикаментозной терапии (step-up);
- включением новых глав по ведению БА у детей 5 лет и младше и по сочетанию БА и хронической обструктивной болезни легких.
Определение
БА – гетерогенное заболевание, преимущественно связанное с хроническим воспалением в дыхательных путях, в патогенезе которого задействованы различные клеточные элементы, включающие тучные клетки, эозинофилы, Т-лимфоциты, а также многочисленные медиаторы воспаления. Хроническое воспаление ассоциируется с развитием бронхиальной гиперреактивности, что ведет к повторным эпизодам свистящих хрипов, одышки, удушья, ощущениям сдавления грудной клетки и кашля, особенно в ночное время или ранние утренние часы. Эти эпизоды обычно сопровождаются распространенной обструкцией дыхательных путей, которая в подавляющем большинстве случаев обратима спонтанно или под влиянием лечения.
Сегодня мы располагаем убедительными доказательствами, что клинические проявления БА, включающие симптоматику, нарушения сна, ограничения физической активности, нарушения дыхательной функции, могут успешно контролироваться адекватными лечебными подходами. При этом рецидивы развития симптомов заболевания существенно снижаются, а тяжелые обострения астмы наблюдаются редко.
Распространенность
Данные о распространенности БА существенно разнятся в различных сообщениях, что объясняется неоднозначными подходами к определению заболевания, его запоздалой диагностикой и значимыми различиями частоты заболевания в различных регионах мира. В крупных эпидемиологических исследованиях распространенность БА в различных странах оценивается от 1% до 18%. Очевидно, более реальная распространенность БА среди взрослого населения может базироваться на результатах крупного эпидемиологического исследования World Health Survey, проводимого экспертами Всемирной Организации Здравоохранения (ВОЗ). В общей популяции среди 178 215 человек из 70 стран распространенность БА составила от 4,3 до 8,6% (колебания зависели от используемого определения заболевания). В ряде масштабных эпидемиологических исследований показано увеличение распространенности БА во многих регионах мира (прежде всего, в странах с низким социальным уровнем и загрязненной окружающей средой). В мире около 300 млн. человек страдает БА, и эта цифра увеличивается на 50% каждые 10 лет. Определенный оптимизм внушают данные о прекращении нарастания распространенности БА, а также существенное снижение летальности в странах с высоким социальным уровнем.
Морбидность, смертность, экономический ущерб
В проведённом экспертами ВОЗ исследовании (The Global Burden of Asthma), посвященного изучению Глобального Бремени БА, показано существенное нарастание распространенности, морбидности и экономического ущерба, связанного с этим заболеванием во многих регионах мира (Африка, Азия, Латинская Америка), прежде всего, в странах с низким социальным уровнем и плохими экологическими характеристиками. При этом отмечается высокий уровень запоздалой диагностики заболевания, увеличение частоты госпитализаций по поводу обострений (особенно у детей), а также летальности.
Ежегодно около 250 000 летальных исходов связано с БА. Причем, летальность значительно выше в странах с низким социальным уровнем, где имеют место несвоевременная диагностика заболевания и неадекватная лечебная тактика в стабильном периоде (прежде всего, ограниченное использование ингаляционных глюкокортикоидов – ИГК), а также ограниченные возможности оказания качественной помощи при обострениях.
По оценкам экспертов ВОЗ, ежегодно БА обуславливает потерю 15 млн. так называемых DALY («Disability Adjusted Life Year» – год жизни, потерянный в связи с нетрудоспособностью), что составляет около 1% общего всемирного ущерба от болезней.
Существенные финансовые затраты обусловлены как прямыми медицинскими затратами на лечение БА (стоимость лекарственных препаратов, пребывание в стационарах), так и затратами, обусловленными днями нетрудоспособности и инвалидизации. В глобальном масштабе финансовые расходы на ведение больных с БА превышают таковые у больных туберкулезом и у лиц, инфицированных ВИЧ.
Этиология
БА является многофакторным заболеванием, характеризующимся сложными взаимодействиями многочисленных факторов, включающих генетические, климатические особенности, загрязненность окружающей среды, социально-экономический уровень, расовую принадлежность и др.
Факторы риска БА можно разделить на обуславливающие ее развитие и/или провоцирующие обострения. Выделяют так называемые факторы макроорганизма (внутренние факторы):
- генетические:
- гены, предрасполагающие к атопии;
- гены, предрасполагающие к бронхиальной гиперреактивности;
- ожирение;
- пол (мужской в детском возрасте, женский – у взрослых);
И факторы окружающей среды (внешние факторы):
- аллергены:
- аллергены помещений (домашние клещи), шерсть домашних животных (собак, кошек, мышей), аллергены тараканов, грибы (плесневые, дрожжевые);
- наружные аллергены (пыльца, грибы – плесневые дрожжевые)
- инфекции (преимущественно вирусные);
- профессиональные сенсибилизаторы;
- табакокурение:
- активное;
- пассивное;
- загрязнение воздуха внутри и снаружи помещений;
- особенности питания.
Патогенез
Патогенез БА представляется сложным, многогранным и не до конца изученным. БА является воспалительным заболеванием дыхательных путей, в развитии которого участвует ряд воспалительных клеток и множество медиаторов воспаления, что приводит к характерным патофизиологическим изменениям.
Различные сочетания и сложные взаимоотношения указанных выше этиологических факторов у предрасположенных лиц обусловливают развитие хронического воспаления в дыхательных путях, сопровождающегося бронхиальной гиперреактивностью и астматическими симптомами.
Несмотря на разнообразие клинических проявлений БА и особенностей патофизиологических механизмов, хроническое воспаление дыхательных путей является фундаментальной характеристикой заболевания. При этом воспалительный процесс в дыхательных путях персистирует даже в ситуациях, когда симптомы заболевания эпизодические, а связь между тяжестью астмы и интенсивностью воспаления далеко не всегда отчетливая. Воспалительные процессы наблюдаются во всех отделах респираторного тракта, включая верхние дыхательные пути, нос, но более выражены в бронхах среднего калибра. Воспаление дыхательных путей присутствует при всех клинических формах БА – аллергической, неаллергической и аспириновой.
Воспалительные клетки и медиаторы воспаления
Воспаление при БА имеет ряд особенностей, характерных для аллергических заболеваний. К ним относится наличие активированных тучных клеток, повышенное количество активированных эозинофилов и увеличенное число рецепторов неизмененных естественных киллерных Т-клеток, а также Тлимфоцитов хелперов 2-го типа (Th-2), продуцирующих воспалительные медиаторы, обуславливающие развитие симптомов заболевания.
В таблице №1 представлены функциональные характеристики воспалительных клеток в дыхательных путях больных БА.
Таб. №1 Функциональная характеристика воспалительных клеток.
|
|
|
|
|
|
Роль структурных клеток дыхательных путей в патогенезе БА показана в таблице №2.
Табл. №2 Место структурных клеток дыхательных путей в патогенезе БА.
|
|
|
|
|
Место ключевых медиаторов в патогенезе БА показано в таблице №3
Табл. №3 Ключевые медиаторы в патогенезе БА.
|
|
|
|
|
|
Таким образом, при БА наблюдается воспаление, характерное для аллергических заболеваний, с наличием активированных тучных клеток, увеличенным количеством активированных эозинофилов, повышенным количеством неизмененных естественных Т-киллеров и Th-2 лимфоцитов, которые продуцируют медиаторы, обусловливающие развитие клинических проявлений заболевания. Структурные клетки дыхательных путей также продуцируют воспалительные медиаторы, что способствует персистенции воспаления. Известно, что более 100 различных воспалительных медиаторов вовлечены в развитие комплекса воспалительных процессов в дыхательных путях у больных БА.
Финальным этапом описанных патофизиологических процессов является констрикция дыхательных путей, ведущая к клиническим проявлениям и физиологическим изменениям при астме. Важное место в развитии и персистенции БА отводится гиперчувствительности дыхательных путей, механизмы которой изучены недостаточно. Гиперчувствительность обуславливает функциональные нарушения, приводящие к сужению дыхательных путей в ответ на различные стимулы, не оказывающие негативного влияния на здоровых людей. В свою очередь, сужение дыхательных путей ведет к вариабельному ограничению воздушного потока и развитию интермиттирующих симптомов. Гиперчувствительность дыхательных путей частично обратима под влиянием лечения.
Механизмами развития бронхиальной гиперреактивности являются увеличение объема и/или контрактильности гладкомышечных клеток бронхов, десинхронизация сокращений гладкой мускулатуры дыхательных путей, изменение геометрии бронхов и сенсибилизация афферентных нервов, что ведет к чрезмерному сокращению гладких мышц дыхательных путей и бронхоконстрикции. В патогенезе бронхиальной обструкции важное место также отводится отеку дыхательных путей, утолщению стенки бронхов вследствие их ремоделирования и гиперсекреции слизи.
Структурные изменения дыхательных путей
Наряду с воспалительным ответом и бронхиальной гиперреактивностью у больных БА развиваются характерные структурные изменения, часто обозначаемые как ремоделирование дыхательных путей, обуславливающее плохую обратимость бронхообструкции.
Структурные изменения характеризуются:
- субэпителиальным фиброзом, развивающимся вследствие депозиции коллагеновых фибрилл и протеогликанов под базальной мембраной и наблюдающимся у всех больных БА, включая детей еще до развития симптомов. Фиброз также наблюдается в других слоях стенки бронхов и также обусловлены депозицией коллагена и протеогликанов;
- увеличением толщины гладких мышц дыхательных путей, что обусловлено как их гипертрофией (увеличением размера клеток), так и гиперплазией. Это ведет к увеличению толщины стенки дыхательных путей. Интенсивность этого процесса коррелирует с тяжестью заболевания, а его развитие обусловлено воспалительными медиаторами такими, как факторы роста;
- пролиферацией кровеносных сосудов в стенке дыхательных путей под влиянием таких факторов, как сосудистый эндотелиальный фактор роста. Это способствует увеличению толщины стенки дыхательных путей;
- гиперсекрецией слизи в результате увеличения числа бокаловидных клеток в эпителии дыхательных путей и увеличением размера подслизистых желез.
Патофизиологические особенности БА при ряде специфических ситуаций
- Обострения астмы (ОА). Транзиторные ухудшения течения БА и утрата контроля заболевания могут быть результатом воздействия таких факторов, как чрезмерная физическая нагрузка, загрязнение воздуха и некоторые погодные факторы. Более длительные ухудшения чаще всего обусловлены вирусной инфекцией дыхательных путей (особенно риновирусы и респираторно-синцитиальные вирусы), а также экспозицией аллергенов, усиливающих воспаление в нижних дыхательных путях.
- Ночная астма. Ухудшение астмы в ночное время связывают с циркадными ритмами циркулирующих гормонов, таких как норадреналин, кортизол или мелатонин, а также нейрогенными механизмами (ночное увеличение холинергического тонуса). В ночное время наблюдается усиление воспаления в дыхательных путях, что может быть связано со снижением эндогенных противовоспалительных механизмов.
- Необратимая бронхообструкция. У части больных с тяжелой астмой развивается прогрессирующее нарушение внешнего дыхания, которое не является обратимым под воздействием лечения.
- БА, трудно поддающаяся лечению. Остаются неизвестными причины, почему у некоторых больных снижена чувствительность к глюкокортикоидам и астма плохо контролируется. В части случаев это связано с плохой приверженностью больных к лечению. В ряде случаев такие варианты БА обусловлены генетическими особенностями.
- Курение и астма. Табакокурение существенно затрудняет контроль БА, ассоциируется с более частыми обострениями и госпитализациями и более быстрым развитием нарушения легочной функции и повышением риска летальных исходов. У таких больных воспаление носит нейтрофил-доминирующий характер, а также отмечается плохой ответ на глюкокортикоиды.
Клиника, диагностика, классификация и лечебная тактика.
Одним из ключевых аспектов рекомендаций GINA 2014 является подчеркивание роли строгой верификации диагноза БА до назначения медикаментозной терапии. Постановка диагноза астмы базируется на оценке двух ключевых параметров:
- наличия варьирующих по времени и интенсивности респираторных симптомов, таких как свистящие хрипы, затруднение дыхания, скованности в грудной клетке, кашель
И
- инструментального подтверждения вариабельной бронхиальной обструкции.
В таблице № 4 обобщены важные характеристики, использующиеся при диагностике БА
Таблица № 4. Критерии диагностики БА.
|
|
Типичными симптомами являются свистящие хрипы, затруднение дыхания, скованности в грудной клетке и кашель
|
|
|
Клиническая картина.
Жалобы. Типичные для БА жалобы включают эпизоды одышки, свистящего дыхания, кашля (с мокротой или без таковой) и ощущение стеснения грудной клетки. Эти симптомы не являются специфическими для БА и могут наблюдаться при различных острых и хронических заболеваниях дыхательных путей. Рассматриваемые симптомы также могут наблюдаться у части больных с ХОБЛ, при этом дифференциальная диагностика между БА и ХОБЛ нередко вызывает затруднения.
Некоторым пациентам затруднительно оценить тяжесть собственных симптомов, около 10% больных во время приступа не ощущают удушья и одышки, отмечая лишь свистящее дыхание и кашель.
Для БА является характерным появление симптомов после контакта с аэроаллергенами и ирритантами. Часто развивается сенсибилизация к аллергенам домашних животных, клещей, домашней пыли, тараканов. У ряда больных наблюдаются сезонные обострения БА, связанные с сенсибилизацией к пыли цветущих растений.
Кашлевой вариант БА
При кашлевом варианте БА кашель является ведущим, а в части случаев единственным симптомом заболевания. «Кашлевая» БА чаще наблюдается у лиц молодого возраста и детей. Для постановки диагноза у таких больных важную роль играют исследования вариабельности показателей функции легких, выявление бронхиальной гиперактивности и определение эозинофилов в мокроте.
Кашлевой вариант БА следует отличать от ряда состояний, проявляющихся кашлем и эозинофилией мокроты. Например, при эозинофильном бронхите имеется хронический малопродуктивный кашель, повышение содержание эозинофилов в мокроте или бронхиальных смывах, но показатели функции легких остаются неизменными. Также следует учитывать возможность развития кашля, связанного с приемом ИАПФ, гастроэзофагеальным рефлюксом, хроническим синуситом и дисфункцией голосовых связок.
Бронхоконстрикция, провоцируемая физическими нагрузками.
У многих больных ведущей (а в некоторых случаях единственной) причиной развития симптомов бронхоконстрикции является физическая активность. Постнагрузочный бронхоспазм обычно развивается через 5-10 минут после прекращения физической активности (реже – во время нагрузки), при этом у пациентов наблюдаются типичные симптомы БА или иногда упорный кашель, самостоятельно проходящий через 40-45 минут. Некоторые виды физической активности (например, бег) провоцируют бронхоспазм чаще. Он также значительно чаще наблюдается при вдыхании сухого холодного воздуха. Быстрое устранение симптомов постнагрузочного бронхоспазма после ингаляции β2-агонистов свидетельствует в пользу наличия БА.
При постановке диагноза БА важное место занимает тщательно собранный анамнез, включающий ответы на такие вопросы:
- Был ли у пациента эпизод (эпизоды) свистящего дыхания?
- Бывает ли у пациента мучительный ночной кашель?
- Бывают ли у пациента свистящее дыхание и/или кашель через 5-10 минут после физической нагрузки?
- Бывают ли у пациента развитие свистящего дыхания, сдавления в грудной клетке или кашля после контакта с аэроаллергенами или поллютантами?
- Отмечает ли пациент, что у него часто «простуда опускается в грудную клетку» или продолжается более 10-ти дней?
При расспросе больного и оценке медицинской документации также важно установить у него наличие различных факторов, способных указывать на наличие БА или усугублять ее течение. К ним следует отнести наличие:
- патологии носа или околоносовых пазух;
- атопического дерматита/крапивницы/поллиноза;
- пищевой аллергии;
- гастроэзофагеального рефлюкса;
- непереносимости аспирина.
Физикальное обследование.
Из-за вариабельности проявлений БА симптомы заболевания дыхательной системы при физикальном обследовании часто могут отсутствовать.
Для острого приступа и обострения БА характерно наличие тахипноэ до 25-30 в минуту и тахикардии около 100 в минуту. Примерно в 25-30% случаев частота дыханий может быть более 30 в минуту, а пульса – более 120 в минуту.
Развитие синусовой тахикардии нередко связывают с применением β2-агонистов и теофиллина для купирования обструкции. Тем не менее, ведущей причиной тахикардии во время острого приступа БА является гипоксемия. Тахикардия обычно устраняется при применении β2-агонистов на фоне разрешения бронхообструкции.
Для больных с острым приступом БА характерно ослабление везикулярного дыхания, удлинение выдоха, наличие свистящих хрипов, прослушивающихся на вдохе и выдохе.
У части больных при наличии выраженной обструкции дыхательных путей могут отсутствовать свистящие хрипы или прослушиваться только на форсированном выдохе («немое легкое»). Этот феномен обусловлен тяжелыми нарушениями вентиляции. У таких больных обычно также имеют место цианоз, тихипноэ, тахикардия, сонливость, ступор, «вздутие» грудной клетки, участие в акте дыхания вспомогательных мышц и втяжение межреберных промежутков, парадоксальный пульс и обильное потоотделение.
Дополнительные методы диагностики и мониторирования БА.
Постановка диагноза БА базируется на сочетании характерных клинических симптомов и инструментальных доказательств наличия гиперреактивности бронхов при изучении функции внешнего дыхания (ФВД). Вспомогательную роль в диагностике также имеют методы исследования, подтверждающие связь с сенсибилизацией и эозинофильным характером воспаления в дыхательных путях. Количество дополнительных методов исследования, которые следует использовать при диагностике БА, зависит от исходной, т.н. претестовой вероятности диагноза, основанной на наличии и выраженности характерных клинических проявлений. В общих чертах подходы к диагностике БА показаны на рисунке 1.
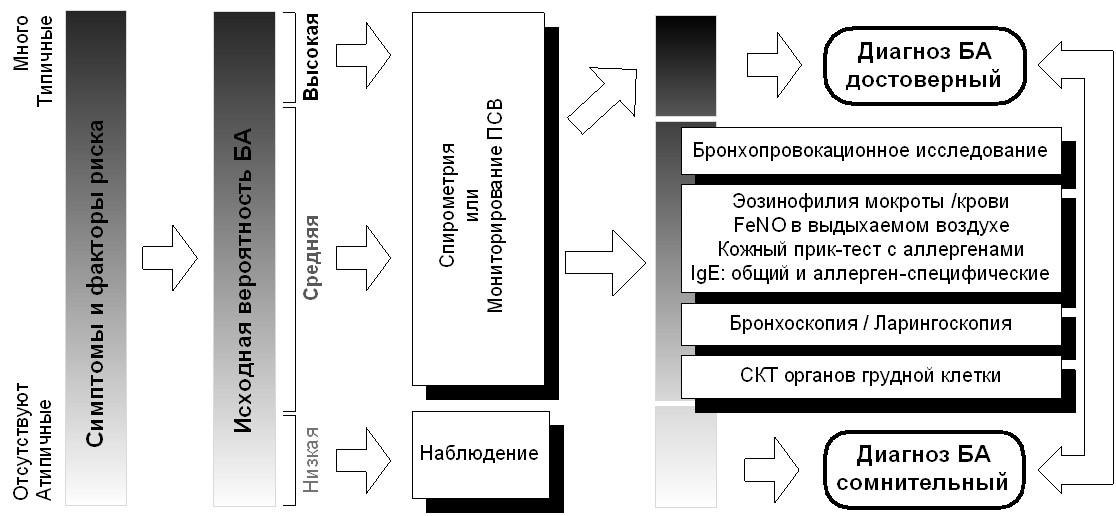
Рисунок 1. Общие подходы к диагностике БА.
У лиц с типичными клиническими проявлениями и высокой претестовой вероятностью БА изучение ФВД является необходимым не столько для подтверждения диагноза, сколько для оценки степени тяжести заболевания. У бессимптомных пациентов или у лиц с недостаточно характерными проявлениями без факторов риска (с низкой претестовой вероятностью БА) изучение ФВД и других инструментальных и лабораторных параметров не имеет существенной диагностической ценности из-за высокой частоты ложноположительных и ложноотрицательных результатов. Наиболее информативны результаты дополнительных исследований у лиц со средней вероятностью наличия БА. При этом наличие признаков обратимой бронхиальной обструкции при спирометрическом исследовании или значительная вариабельность пиковой скорости выдоха (ПСВ) в течение суток является достаточным для постановки точного диагноза БА. В случае их отсутствия при стандартном исследовании ФВД необходимо проведение бронхопровокационного тестирования, которое способно выявить ключевой признак БА – гиперреактивность бронхов.
Наличие лабораторных и инструментальных данных об эозинофильном характере воспаления в дыхательных путях (эозинофилия мокроты и крови, фракция оксида азота (FeNO) в выдыхаемом воздухе) и аллергической сенсибилизации может свидетельствовать в пользу БА. Но их отрицательные результаты не позволяют исключить наличие астмы. Ряд других методов исследования (рентгенологические, эндоскопические) может представить дополнительные данные, позволяющие провести дифференциальную диагностику. Ниже представлено описание методов, используемых для диагностики и мониторирования течения БА.
Спирометрия и бронходилатационный тест. Спирометрия является методом выбора для оценки наличия, выраженности и обратимости бронхиальной обструкции. Объем форсированного выдоха за первую секунду (ОФВ1) и форсированная жизненная емкость легких (ФЖЕЛ) определяют с помощью спирометра при форсированном выдохе.
Спирометрическим критерием, подтверждающим наличие обструкции является отношение ОФВ1/ФЖЕЛ, составляющее менее 0,7. Критерием диагностики БА также в течение длительного времени считалось наличие обратимости бронхиальной обструкции после ингаляции 400 мкг сальбутамола (т.е. после проведения бронходилатационного теста). Критерием обратимой бронхиальной обструкции считают наличие прироста ОФВ1 ≥ 12% и ≥ 200 мл при выполнении бронходилатационного теста. Однако в последние годы в целом ряде масштабных исследований показано, что выраженный ответ на бронходилатацию (т.е. прирост ОФВ1 более 12%, а иногда и до 30-40%) может наблюдаться более чем у 13 больных ХОБЛ. При этом обструкция является лишь частично обратимой, то есть полностью не разрешается после пробы с бронходилататором. Кроме того, около 30% больных с тяжелой или длительно текущей астмой после ингаляции сальбутамола не демонстрируют значительного прироста ОФВ1 и обструкция у них также является не полностью обратимой. Приведенные данные свидетельствуют, что наличие прироста ОФВ1 ≥ 12% и ≥ 200 мл после бронходилатации не может служить надежным спирометрическим признаком БА. Достаточно характерным для БА признаком является полное устранение обструкции после ингаляции 400 мкг сальбутамола (в среднем, у 23 пациентов).
Кроме того, результаты бронходилатационного теста не могут служить основанием для выбора бронходилатационной терапии (β2-агонисты или антихолинергические средства) из-за отсутствия соответствующей доказательной базы.
Пикфлоуметрия. Для оценки степени бронхиальной обструкции и эффективности терапии также используется пикфлоуметрия – измерение пиковой скорости выдоха (ПСВ). Обычно ПСВ измеряют утром, до приема препаратов; при этом чаще всего получают близкое к минимальному значение ПСВ. Вечером ПСВ измеряют перед сном, как правило, получая более высокие значения. Согласно рекомендациям GINA 2014, среднесуточную вариабельность ПСВ следует определять таким образом:
- Проводят измерение ПСВ 2 раза в сутки (при каждом измерении выбирают лучшую из 3 попыток) и рассчитывают среднее значение (ПСВср).
- Вычисляют отношение (ПСВмакс – ПСВмин)/ПСВср, выраженное в процентах.
- Усредняют данный показатель за за 7-14 дней.
Изменение ПСВ в течение суток более чем на 10% указывает на наличие БА.
Другим способом оценки вариабельности ПСВ является определение минимальной ПСВ за 1 нед в процентах от самого лучшего показателя за этот же период (Min%Max). Предполагается, что данный метод имеет ряд преимуществ, поскольку его проще рассчитать и он лучше коррелирует с бронхиальной гиперреактивностью.
Оценка бронхиальной гиперреактивности. У пациентов с характерными симптомами БА, но с нормальными показателями функции легких значительную диагностическую ценность имеет исследование реакции бронхов на метахолин, гистамин, маннитол, аденозин, гипертонический солевой раствор или физическую нагрузку. Бронхиальная реактивность отражает«чувствительность» дыхательных путей к так называемым триггерам, т.е. факторам, способным вызывать появление симптомов БА. Результаты теста обычно приводятся в виде провокационнойконцентрации (или дозы) агента, вызывающего определенное снижение ОФВ1 (как правило, на 20%). Достигнутая концентрация характеризует наличие и степень выраженности бронхиальной гиперреактивности.
Неинвазивное определение маркеров воспаления дыхательных путей. Для оценки наличия и активности воспаления в дыхательных путях при БА проводится специальное цитологическое исследование спонтанно продуцируемой или индуцированной ингаляцией гипертонического солевого раствора мокроты. Стандартная микроскопия мокроты не может быть заменой данному исследованию, так как не позволяет полноценно оценить характер и интенсивность воспалительных явлений.
Кроме того, в качестве неинвазивных маркеров воспаления в дыхательных путях при БА были предложены уровни оксида азота (FeNO) в выдыхаемом воздухе. У больных БА отмечается повышение уровня FeNO по сравнению с лицами без БА.
Оценка аллергического статуса. У части больных выявляется тесная взаимосвязь БА с различными атопическими состояниями, и особенно аллергическим ринитом. Выявление у больных БА аллергии (подтвержденной с помощью кожных проб или определения специфических IgE в сыворотке крови) позволяет установить у них факторы риска и триггеры ухудшения течения заболевания.
Кожные пробы с аллергенами представляют собой основной метод оценки аллергического статуса. Они просты в применении, не требуют больших затрат времени и средств и обладают высокой чувствительностью. Однако неправильное выполнение проб может привести к получению ложноположительных или ложноотрицательных результатов. Определение специфических IgE в сыворотке крови не превосходит кожные пробы по надежности, но является более дорогостоящим методом. Главным недостатком методов оценки аллергического статуса является то, что положительные результаты тестов не обязательно указывают на аллергическую природу заболевания и на связь аллергена с развитием БА, так как у части лиц специфические IgE могут обнаруживаться при отсутствии симптомов заболевания и не играть какой-либо роли в развитии БА.
Дифференциальная диагностика.
Дифференциальную диагностику следует проводить со следующими заболеваниями:
- гипервентиляционный синдром и панические атаки;
- обструкция верхних дыхательных путей и аспирация инородных тел;
- дисфункция голосовых связок;
- гастроэзофагеальная рефлюксная болезнь (ГЭРБ);
- другие обструктивные заболевания легких, в особенности хроническая обструктивная болезнь легких (ХОБЛ);
- необструктивные заболевания легких (например, интерстициальные заболевания легких);
- нереспираторные заболевания (например, левожелудочковая сердечная недостаточность).
БА может сочетаться с любым из перечисленных выше состояний, что нередко затрудняет диагностику, оценку степени тяжести и уровня ее контроля.
Отдельного обсуждения заслуживает проведение дифференциальной диагностки между БА и ХОБЛ, учитывая их высокую распространенность и принципиально разные подходы к лечению. Основные дифференциально-диагностические критерии ХОБЛ и БА приведены в табл. 5.
Таблица 5. Основные критерии дифференциальной диагностики ХОБЛ и БА
|
Признаки |
БА |
ХОБЛ |
|
Возраст начала болезни |
Чаще детский и молодой * |
Как правило, старше 40 лет |
|
Курение в анамнезе |
/ – |
|
|
Внелегочные проявления аллергии ** |
Характерные |
Не характерны |
|
Симптомы (кашель и одышка) |
Симптомы изменчивы, появляются приступообразно: в течение дня, с каждым днем, сезонно |
Постоянные, прогрессируют медленно |
|
Отягощенная наследственность по астме |
Характерна |
Не характерна |
|
Бронхиальная обструкция |
Преимущественно обратимая |
Мало обратимая или необратимая |
|
Суточная вариабельность ПСВ |
<10% |
|
|
Наличие легочного сердца |
Не характерно |
Характерно при тяжелом течении заболевания |
|
Тип воспаления *** |
Преобладают эозинофилы |
Преобладают нейтрофилы |
|
Эффективность глюкокортикоидной терапии |
Высокая |
Умеренная |
Примечания:
* Бронхиальная астма может начинаться в среднем и пожилом возрасте.
** Аллергический ринит, конъюнктивит, атопический дерматит, крапивница.
*** Тип воспаления дыхательных путей наиболее часто определяется путем цитологического исследования мокроты и жидкости бронхоальвеолярного лаважа.
Классификация БА.
В новом пересмотре рекомендаций GINA 2014 отсутствует раздел, посвященный классификации БА. Тем не менее, традиционно при оценке БА используют три параметра, включающие этиологическое происхождение, тяжесть заболевания и степень достижения его контроля.
По этиологии. Возможности классификации БА на основе этиологии с учетом сенсибилизирующих внешних факторов заметно ограничены, так как для некоторых больных не удается выявить внешние факторы риска. Руководство GINA 2014 указывает, что выделение аллергической (атопической, экзогенной) и неаллергической (эндогенной) БА нецелесообразно, так как причиной БА редко является единственный специфический аллерген. Несмотря на это поиск внешних факторов развития БА (например, профессиональной БА, аспириновой БА) должен обязательно проводиться у каждого пациента. Кроме того, указание на этиологию при формулировке диагноза является привычным и в ряде случаев полезным для определения тактики лечения.
По уровню контроля БА и риска осложнений. С целью оценки ответа пациента на назначенную терапию, введено понятие контроля БА. Термин «контроль» обозначает устранение проявлений заболевания. В идеале это должно относиться не только к клиническим проявлениям, но и к лабораторным маркерам воспаления и патофизиологическим признакам заболевания (например, гиперреактивности бронхов). В клинической практике рекомендуется использовать классификацию БА по уровню контроля над заболеванием и риску будущих осложнений течения заболевания и медикаментозной терапии (табл. 6).
Таблица 6. Уровни контроля БА и риска осложнений.
|
А. Оценка текущего клинического контроля (в течение последних 4 нед). |
||||
|
Характеристики |
Контролируемая БА (всё ниже-перечисленное) |
Частично контролируемая БА (любое проявление в течение любой недели) |
Неконтролируемая БА |
|
|
Дневные симптомы |
Отсутствуют (или ≤2 эпизодов в неделю) |
Наличие трех или более признаков частично контролируемой БА
Наличие обострения длительностью более 1 недели * |
||
|
Ограничения активности |
Отсутствуют |
Есть |
||
|
Ночные симптомы/пробуждения |
Отсутствуют |
Есть |
||
|
Потребность в препаратах неотложной помощи |
Отсутствует (или ≤2 эпизодов в неделю) |
|||
|
Б. Оценка будущего риска (риск обострений, дестабилизации, быстрого снижения функции легких, побочных эффектов от лечения) |
||||
|
Необходимо оценить будущий риск при постановке диагноза и периодически оценивать повторно, особенно у лиц с обострениями. Следует измерить ОФВ1 до начала лечения, через 3-6 месяцев базисной терапии и повторно по необходимости. |
||||
|
Признаки, ассоциируемые с высоким риском обострений БА, включают:
|
Наличие данных факторов сопровождается увеличением риска обострений даже в случае хорошего контроля или отсутствия симптомов |
|||
|
Факторы риска развития необратимой обструкции: неприменение ИГК, воздействие табачного дыма и аэрополлютантов, низкий ОФВ1, хроническая гиперсекреция слизи, наличие эозинофилии мокроты или крови. |
||||
|
Факторы риска развития побочных эффектов медикаментозной терапии: Частые курсы оральных глюкокортикоидов; длительное применение, высокие дозы ИГК, сопутствующий прием ингибиторов цитохрома Р450, неадекватная техника ингаляции. |
||||
Полный контроль над БА обычно достигается с помощью базисной терапии, с учетом должного внимания к переносимости лечения, риску развития побочных эффектов и стоимости лекарственных средств, необходимых для достижения этой цели.
По степени тяжести. Классификация БА по степени тяжести также является традиционным подходом, который основывается на результатах анализа комплекса клинических и функциональных признаков бронхиальной обструкции. Прежде считалось, что классификация БА по степени тяжести может оказаться полезной для выбора тактики лечения заболевания. Однако далеко не всегда первоначальная оценка выраженности клинических проявлений у больного может служить надежным критерием выбора оптимальной лечебной тактики и прогноза. Кроме того, тяжесть клинических проявлений у конкретного больного может существенно меняться с течением времени под влиянием адекватной терапии.
Тяжесть БА тесно коррелирует со сложностью достижения медикаментозного контроля над астмой. Эксперты GINA пришли к заключению, что тяжесть БА целесообразно оценивать только ретроспективно по объему терапии, необходимому для достижения контроля заболевания после нескольких месяцев адекватно подобранной базисной терапии. При этом использовавшееся ранее разделение на интермиттирующую и персистирующую астму в настоящей редакции рекомендаций не упоминается.
Легкая степень тяжести констатируется при достижении контроля БА на фоне применения только короткодействующих бета-агонистов (КДБА) по требованию или низких доз ИГК или антилейкотриеновых препаратов (АЛП), что соответствует 1-2 шагам терапии (см. ниже).
Средняя степень тяжести устанавливается при достижении контроля БА на фоне применения низких доз ИГК в сочетании с длительнодействующими бета-агонистами (ДДБА) или средних доз ИГК (соответствует 3 шагу терапии).
Тяжелая БА констатируется, когда для достижения полного контроля необходим большой объем терапии (например, высокие дозы ИГК в сочетании с ДДБА, что соответствует 4-5 шагам терапии астмы) или, несмотря на большой объем терапии, контроль БА достигнуть не удается.
Важно отличать тяжелую БА от недостаточно контролируемой. Прежде чем прийти к заключению о наличии тяжелой БА, следует убедиться, что исключены другие возможные причины отсутствия контроля:
- неадекватная техника ингаляции (до 80% пациентов);
- низкая приверженность лечению;
- некорректная диагностика БА;
- наличие коморбидных состояний (риносинусит, гастроэзофагеальный рефлюкс, ожирение, синдром обструктивного ночного апноэ и др.).
Лечебная тактика при БА
Целью успешного ведения больных БА является:
- устранение и профилактика симптомов заболевания;
- достижение хорошего качества жизни;
- уменьшение потребности в применении β2 – агонистов;
- по возможности сохранение легочной функции, близкой к нормальной;
- профилактика обострений;
- снижение риска побочных эффектов проводимой терапии;
- снижение смертности.
Общие вопросы лечебной тактики
Каждому пациенту назначают лечение, соответствующее одной из пяти ступеней, или шагов, терапии. Традиционно в русскоязычной среде слово «ступень» использовалось для обозначения тяжести БА и объема необходимой терапии. Однако после 2006 года новый подход к ступенчатой терапии БА перестал быть «привязан» к тяжести БА. Поэтому во избежание путаницы часто понятие «ступень» используют применительно к тяжести БА, а термин «шаг терапии» – к интенсивности лечения. В данной публикации эти термины используются взаимозаменяемо. На рис. 2 представлена терапия БА на каждом шаге.
Рис. 2. Подход к лечению БА, ориентированный на контроль над заболеванием (рекомендации GINA 2014)
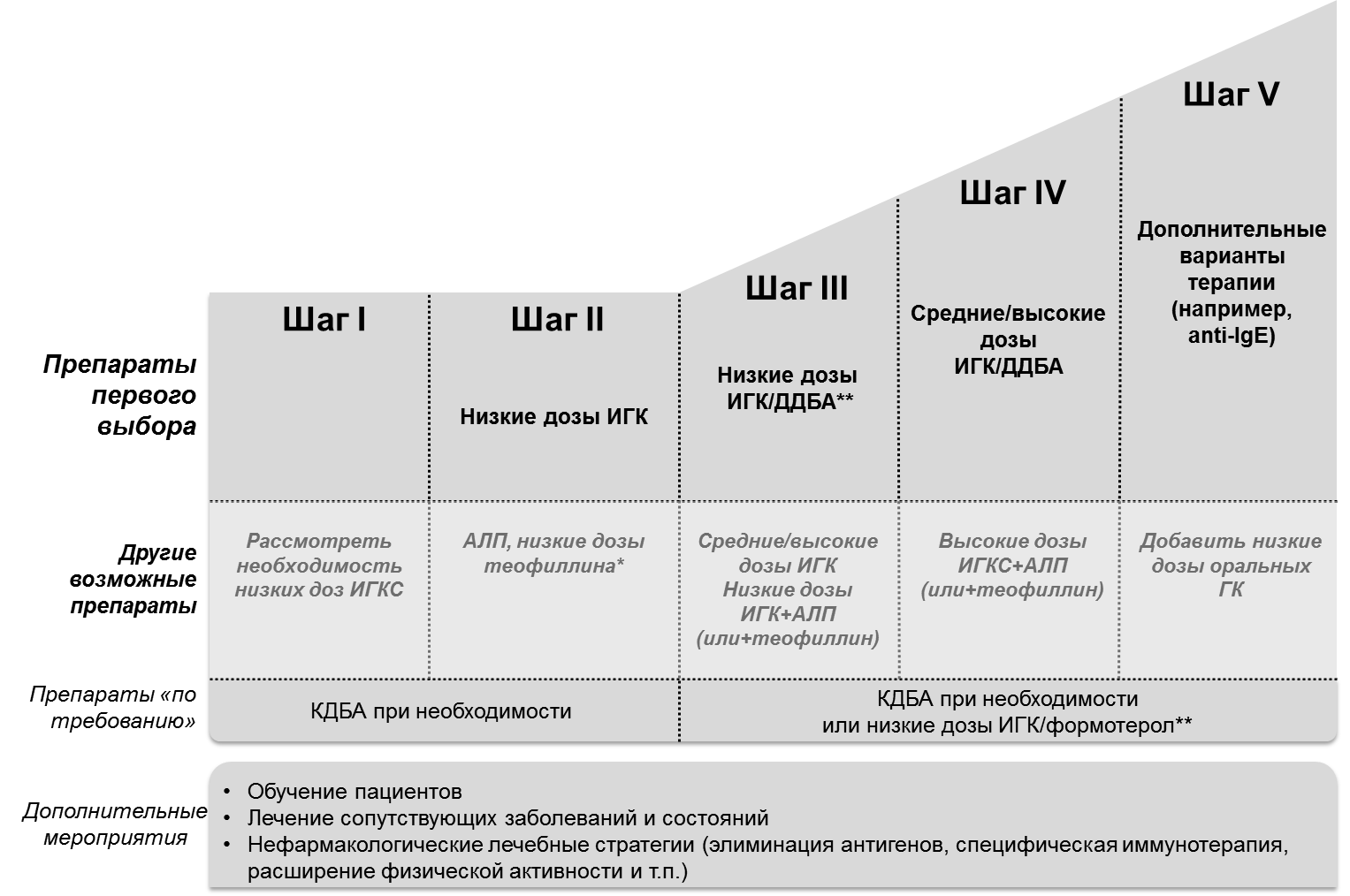
На любом шаге терапии пациенты должны использовать по потребности препараты неотложной помощи для быстрого облегчения симптомов, предпочтительнее, КДБА. В ряде случаев (на 3-5 шагах терапии у пациентов с частыми обострениями) вместо КДБА в качестве скоропомощного препарата предпочтительнее использовать комбинацию ИГК/формотерол (SMART-терапия). К альтернативным (менее предпочтительным) препаратам для облегчения симптомов относятся ингаляционные антихолинергические средства, некоторые β2-агонисты длительного действия и теофиллин короткого действия. На шагах 2–5 пациенты дополнительно нуждаются в применении одного или более базисных препаратов.
Регулярная терапия ИГК рекомендуется, если есть хотя бы один из признаков:
- симптомы БА проявляются более 2 раз в месяц;
- имеет место хотя бы одно ночное пробуждение из-за БА в течение месяца;
- наличие любых симптомов БА в сочетании с любым из факторов риска обострений (наличие за последние 12 мес обострения, потребовавшего применения системных глюкокортикоидов; низкий ОФВ1; интенсивная терапия обострения в прошлом).
У большинства больных с впервые выявленной БА или ранее не получавших препаратов базисной терапии следует начинать лечение со 2 шага терапии (или 3 при наличии тяжелых персистирующих симптомов). Показано, что даже такой малоинтенсивный режим лечения обеспечивает достижение контролируемого состояния заболевания у большинства пациентов. Обычно пациенты посещают врача через 1–3 мес после первичного визита, затем каждые 3-6 мес. После обострения назначают визит последующего наблюдения в срок от 1 до 2 нед.
Если на фоне текущей терапии БА не контролируется, следует увеличить объем терапии (перейти на следующую ступень). Обычно развернутый эффект от увеличения объема терапии и клинически значимое улучшение наступает в течение 1 мес. При частично контролируемой БА также следует рассмотреть возможность расширения объема терапии (увеличение на одну ступень). При этом необходимо взвешивать безопасность и стоимость лечения и удовлетворенность пациента достигнутым уровнем контроля над заболеванием. Однако следует помнить, что перед принятием решения об увеличении шага терапии нужно оценить комплаенс и технику ингаляции, устранить модифицируемые факторы риска (например, курение) и осуществить коррекцию важных сопутствующих заболеваний.
Если пациент не достигает приемлемого уровня контроля над бронхиальной астмой на фоне лечения, соответствующего 4 шагу, можно считать, что пациент страдает БА, трудно поддающейся лечению. У таких пациентов допустимо достижение «достаточного» уровня контроля, который бы обеспечивал наилучший возможный контроль над заболеванием при наименьшем риске побочных эффектов терапии.
Если контроль поддерживается в течение 3 мес и более, следует постепенно уменьшать объем лечения, переходя на более низкий шаг терапии. При этом целью является достижение наименьшего возможного объема лечения, обеспечивающего поддержание контроля над БА. При этом нужно убедиться, что для этого выбран оптимальный момент (не во время вирусной инфекции, беременности, не планируется путешествие пациента).
Даже после достижения контроля необходимо продолжать мониторирование, так как БА представляет собой вариабельное заболевание, при котором периодически требуется коррекция терапии в ответ на утрату контроля, проявляющуюся ухудшением течения заболевания или развитием обострения.
Характеристика медикаментов и других подходов, применяемых при лечении БА
Для достижения целей лечения БА используют как фармакологические, так и нефармакологические лечебные подходы.
Лекарственные препараты, используемые при лечении больных с БА, классифицируются на «базисные», обеспечивающие контроль заболевания (в англоязычной литературе – «controllers»), и «симптоматические» (в англоязычной литературе – «relievers»), устраняющие кратковременные ухудшения симптоматики БА.
Базисная терапия характеризуется ежедневным приемом лекарственных препаратов в течение неопределенно длительного времени с целью клинического контроля БА благодаря преимущественно противовоспалительным эффектам. Симптоматическая терапия – приемом быстродействующих препаратов для устранения бронхоспазма и связанных с ним симптомов.
Пути введения лекарственных препаратов включают ингаляционные, пероральные и парентеральные (внутривенные, подкожные и внутримышечные). Преимущество ингаляционного приема препарата обусловлено его непосредственным поступлением в дыхательные пути, и созданием при этом эффективных местных концентраций, что снижает риск развития или уменьшения выраженности побочных эффектов препарата.
Ингаляционные препараты для лечения БА представлены в виде различных доставочных устройств, различающихся по эффективности доставки лекарственного препарата в нижние дыхательные пути, а также простоте и доступности применения. Основные классы доставочных устройств – дозирующие аэрозольные ингаляторы (ДАИ) и их модификации (например, устройства, активируемые вдохом) и дозирующие порошковые ингаляторы (ДПИ). Представляет интерес также новое устройство типа soft mist, которое без использования пропеллента создает «медленное» мелкодисперсное облачко препарата, значительно улучшающее доставку. Достоинством ДАИ является их невысокая цена, что делает их хорошим выбором для пациента, способного синхронизировать вдох и нажатие на распылитель. В противном случае могут быть использованы вспомогательные средства (спейсер) или другие типы доставочных устройств. Следует помнить, что у некоторых пациентов с тяжелой БА и снижением инспираторного резерва может снижаться эффективность применения ДПИ.
Эффективность доставки препарата в нижние отделы дыхательных путей зависит от таких факторов, как тип ингалятора и форма лекарственного средства, размер частиц, скорость аэрозольного потока или облачка и простоты применения устройства. В связи с этим критически важным является выбор подходящего доставочного устройства, адекватное обучение пациента и регулярная проверка техники ингаляции.
Симптоматическая терапия
Симптоматическая терапия бронходилататорами направлена на быстрое устранение бронхоконстрикции и обусловленных ею симптомов, что достигается за счет релаксации гладкой мускулатуры дыхательных путей. Бронходилататоры действуют преимущественно на гладкую мускулатуру дыхательных путей, что ведет к быстрому устранению симптомов, оказывая в лучшем случае незначительный противовоспалительный эффект.
В современной практике применяются три класса бронходилататоров: β2-адренергические агонисты, антихолинергические препараты и теофиллин, среди которых наиболее эффективныβ2-агонисты.
Короткодействующие β2-агонисты короткого действия (КДБА).
КДБА являются средством выбора для устранения бронхоспазма при остром приступе астмы или в некоторых случаях для его профилактики. К ним относятся сальбутамол, тербуталин, фенотерол. Продолжительность их действия составляет 3 – 6 часов.
β2-агонисты активируют β2-адренергические рецепторы, широко представленные в дыхательных путях. При их стимуляции увеличивается внутриклеточный циклический АМФ, релаксирующий гладкомышечные клетки и ингибирующий некоторые клетки воспалительного каскада.
Ведущим механизмом действия β2-агонистов является релаксация гладкомышечных клеток всех дыхательных путей, где они действуют в качестве функциональных антагонистов, устраняя и превентируя бронхоконстрикцию. Такой эффект обусловливает их высокую эффективность в качестве бронходилататоров при астме. Кроме того, β2-агонистам присущ ряд небронходилатирующих эффектов, включающих ингибирование освобождения медиаторов тучных клеток, снижение экссудации плазмы и ингибирование активации сенсорных нервов. В отличие от глюкокортикоидов, β2-агонисты не оказывают эффект на воспалительные клетки в дыхательных путях и не снижают их гиперчувствительность.
В таблице № 7 представлены механизмы действия β2-агонистов.
Таблица 7. Эффекты β-адренергических агонистов на дыхательные пути
|
|
|
|
|
|
|
Ингаляции КДБА обычно используются для быстрого устранения симптомов БА. Необходимость в их частом применении свидетельствует о недостаточном контроле БА, требующем коррекции базисной терапии.
Развитие побочных эффектов при использовании ингаляционных β2-агонистов в большинстве случаев не является проблемой. Иногда (более характерно для пожилых) развивается тремор, тахикардия и аритмии. У части больных наблюдается незначительное снижение плазменного калия. Этот эффект не представляет серьезной клинической проблемы и не требует назначения препаратов калия.
У больных, которые не способны принимать ингаляционные препараты, допустимо применение пероральных КДБА. Однако при этом наблюдается существенное увеличение частоты и тяжести побочных эффектов.
Антихолинергические препараты. Короткодействующие антихолинергические препараты, используемые при БА, включают ипратропиум бромид и окситропиум бромид. Их способность устранять бронхоконстрикцию уступает таковой КДБА. В метаанализе исследований, где ингаляционный ипратропиум бромид применялся в комбинации с КДБА у больных с обострением БА, было показано, что дополнительное назначение ипратропиума ассоциировалось со статистически значимым, хотя и умеренным улучшением легочной функции и существенным снижением риска повторных госпитализаций. Преимущества ипратропиума над КДБА при длительном применении не установлены. При тяжелом обострении БА антихолинергические препараты следует применять только после КДБА, так как они характеризуются медленным началом бронходилатации. Вместе с тем, ипратропиум может служить альтернативным бронходилататором для больных со значительными побочными эффектами от КДБА, включающими тремор, тахикардии и аритмии.
Побочные эффекты ингаляционных ипратропиума и окситропиума включают сухость и горький вкус во рту. У пожилых больных иногда наблюдаются задержка мочи и развитие или усугубление глаукомы.
Теофиллин. В течение длительного времени пероральный теофиллин широко использовался в качестве бронходилататора. В настоящее время ведущую позицию в лечении БА заняли ингаляционные β2-агонисты благодаря своему мощному бронходилатирующему эффекту и меньшей частоте побочных эффектов.
Непролонгированные формы теофиллина у некоторых больных могут быть использован для устранения симптомов. У лиц, получающих β2-агонисты они не оказывают никакого дополнительного бронходилатирующего эффекта.
Эуфиллин (растворимая соль теофиллина) ранее широко использовался внутривенно для устранения симптомов у больных с тяжелой БА. Сегодня его применение ограничивается случаями тяжелого обострения астмы, рефрактерного к высоким дозировкам КДБА.
Вопросы дозирования, безопасности и побочных эффектов теофиллина более детально раскрыты ниже в разделе, посвященном базисной терапии.
Системные глюкокортикоиды (ГК). Системные ГК не рассматриваются как симптоматические препараты. Они находят применение при тяжелых обострениях БА, что рассматривается в главе, посвященной лечебной тактике при обострениях заболевания.
Базисная терапия БА
Ингаляционные глюкокортикоиды
ИГК сегодня рассматриваются как наиболее эффективные противовоспалительные средства в лечении БА. В многочисленных исследованиях продемонстрирована их способность уменьшать частоту и интенсивность симптомов астмы, улучшать качество жизни и показатели легочной функции, снижать гиперчувствительность дыхательных путей, контролировать воспалительные процессы в них, снижать частоту и тяжесть обострений и летальность.
Однако важно отметить, что ИГК не излечивают астму и после прекращения их использования у многих больных наблюдается возвращение симптомов и ухудшение течения заболевания (ухудшение качества жизни и показателей легочной функции, увеличение риска обострений и связанных с ними осложнений).
Различные ИГК отличаются по их активности и биодоступности. Однако эти различия не ассоциируются с заметными различиями в клинической эффективности.
В табл. №7 показаны приблизительно эквивалентные дозы различных ИГК, базирующиеся на данных исследований.
Таблица 7. Эквивалентные суточные дозы ИГК у взрослых
|
Препарат |
Низкая суточная доза (мг) |
Умеренная суточная доза (мг) |
Высокая суточная доза (мг) |
|
Беклометазон дипропионат |
200- 500 |
||
|
Будесонид |
200 – 400 |
||
|
Флютиказон пропионат |
100 – 250 |
– 1000 |
|
|
Мометазон фуроат |
200 |
≥400 |
≥800 |
Примечание: Наиболее важной детерминантой адекватной дозы ИГК является оценка эффективности терапии. Врач должен мониторировать динамику заболевания и регулировать дозировку препарата. После достижения контроля БА доза препарата должна тщательно титроваться до минимальной, сохраняющей контроль заболевания, что позволяет снизить риск побочных эффектов. Эффективность некоторых ИГК варьирует при использовании различных доставочных устройств.
В большинстве случаев желаемый эффект ИГК у взрослых больных достигается при использовании низких дозировок – эквивалентных 400 мг будесонида в сутки. Увеличение дозировок не всегда улучшает контроль БА, но ассоциируется с увеличением риска побочных эффектов. Следует подчеркнуть довольно широкую вариабельность эффекта ИГК у различных больных, что требует индивидуального подхода к выбору оптимальной дозировки. Часть больных с тяжелой БА нуждается в длительном применении высоких дозировок ИГК, что обеспечивает хороший контроль заболевания.
У курящих больных снижается эффект ИГК, что обычно требует увеличения их дозировок.
При недостаточном контроле БА под влиянием низких или умеренных дозировок обычно не следует увеличивать их дозировку, а назначить дополнительно другой класс базисных препаратов.
Побочные эффекты ИГК. Локальные побочные эффекты ИГК включают орофарингеальный кандидоз, дисфонию и реже кашель, обусловленный раздражением верхних дыхательных путей. Новые доставочные устройства снижают риск этих побочных эффектов. Риск развития орального кандидоза снижается при полоскании рта водой после ингаляции.
Поступающие в легкие ИГК в определенной мере проявляют системную биодоступность. Развитие системных побочных эффектов, их характер и выраженность при лечении ИГК зависят от многих факторов, включающих дозу и активность препаратов, системную биодоступность, конверсию в неактивные метаболиты в печени и периода полувыведения системно абсорбированных глюкокортикоидов. Следовательно, системные побочные эффекты неоднозначны для различных ИГК. В ряде исследований продемонстрированы менее выраженные системные эффекты у будесонида, циклесонида и флютиказона пропионата. Представлены убедительные доказательства, что у взрослых, получающих будесонид в дозе 400 мг и менее в сутки, системные побочные эффекты препарата не являются клинически значимыми.
Системные побочные эффекты, риск развития которых увеличивается у больных, длительно принимающих максимальные дозы ИГК, включают надпочечниковую недостаточность, снижение минеральной костной плотности, остеопороз, повышенный риск переломов, кушингоид и др. Имеются неоднозначные доказательства относительно риска развития катаракты, глаукомы и развития легочных инфекций, включая туберкулез. Тем не менее, считается общепризнанным, что они не противопоказаны больным с активным туберкулезом.
Антилейкотриеновые препараты (АЛП)
АЛП включают антагонисты CysLT1 – рецепторов цистеиниловых лейкотриенов (монтелукаст, пранлукаст и зафирлукаст), а также ингибитор 5-липооксигеназы (зилеутон).
АЛП обладают слабым и вариабельным бронходилатирующим эффектом, уменьшают тяжесть симптомов, включая кашель, улучшают показатели лёгочной функции, снижают воспаление в дыхательных путях и риск обострений БА. Они могут быть альтернативой ИГК для лечения пожилых больных с легкой персистирующей БА, а также для лиц с аспириновой астмой. АЛП менее эффективны в достижении контроля БА, чем низкие дозы ИГК. Не рекомендуется назначать АЛП вместо ИГК, так как это может привести к утрате контроля БА.
У больных с умеренной или тяжелой БА АЛП могут использоваться в качестве дополнительной базисной терапии к ИГК, позволяя при этом снижать высокие дозировки последних. Однако в качестве дополнения к терапии ИГК они уступают в эффективности ингаляционным β2-агонистам продленного действия (ДДБА).
Побочные эффекты. АЛП характеризуются хорошей переносимостью, побочные эффекты характеризуются как несущественные.
Длительнодействущие β2-агонисты (ДДБА)
ДДБА, включая формотерол и сальметерол, не рекомендуется использовать в качестве монотерапии при БА, так как они не оказывают противовоспалительный эффект в дыхательных путях. ДДБА применяются в комбинации с ИГК. Такая комбинация особенно предпочтительна в случаях, когда умеренные дозы ИГК не способны обеспечить достаточный контроль БА.
Комбинация ИГК с ДДБА снижает или устраняет клинические проявления астмы, улучшает показатели легочной функции, снижает необходимость в применении КДБА, уменьшает риск обострений и частоту госпитализаций, а также позволяет достигать контроля БА у большего числа больных в более короткие сроки при более низких дозах ИГК, чем при их самостоятельном применении.
Представленные выше преимущества комбинированного применения ИГК с ДДБА послужили основанием для создания ингаляторов, содержащих фиксированные комбинации ИГК с ДДБА (например, флютиказона пропионат с сальметеролом; будесонид с формотеролом; беклометазон с формотеролом). Такие фиксированные комбинации характеризуются более существенным преимуществом по сравнению с самостоятельным применением ИГК и ДДБА, повышают приверженность больных к лечению. Кроме того, ингаляторы, содержащие фиксированную комбинацию формотерола и будесонида, могут использоваться одновременно как для купирования симптомов (reliever), так и для регулярной базисной терапии (controller). Такой режим применения одного и того же ингаляционного средства получил название SMART-терапии (Single Inhaler Maintenance and Reliever Therapy).
ДДБА, применяемые в комбинации с ИГК, способны эффективно превентировать бронхоспазм, индуцированный физической нагрузкой.
Сальметерол и формотерол обеспечивают примерно равную по продолжительности бронходилатацию. Однако формотерол проявляет бронходилатирующий эффект более быстро, чем сальметерол, что позволяет использовать его как для устранения симптомов БА, так и для их профилактики.
Побочные эффекты. Применение ДДБА может быть связано с риском развития ряда побочных эффектов, включающих тахикардию, аритмии, тремор и гипокалиемию. Регулярное использование β2-агонистов (короткого и продленного действия) может привести к снижению чувствительности к ним. В ряде метаанализов показано незначительное увеличение риска смертности у больных БА, получавших ДДБА в комбинации с ИГК по сравнению с лицами, получавшими монотерапию ИГК. Однако способность комбинации ИГК с ДДБА надежно контролировать течение БА, снижать частоту обострений и улучшать показатели легочной функции служит важным аргументом в необходимости дополнительного назначения ДДБА к ИГК у большинства больных БА.
Тиотропий
Тиотропий – ингаляционный антихолинергический препарат продленного действия, ингибирует констрикцию гладкомышечных клеток и секрецию слизистой бронхов. Кроме того, представлены доказательства о способности тиотропия оказывать противовоспалительный эффект в дыхательных путях.
В течение десятилетий антихолинергические агенты широко используются для лечения больных с ХОБЛ. Многие клиницисты относят антихолинергические средства к бронходилататорам первой линии при ХОБЛ. В лечении БА антихолинергические препараты менее популярны, что, очевидно, связано с медленным началом их действия и менее выраженным бронходилатирующим эффектом по сравнению с ДДБА.
Дополнительное применение тиотропия у больных с тяжелым течением БА, где комбинация ИГК с ДДБА не способна обеспечить оптимальный контроль БА, изучено в нескольких небольших исследованиях, результаты которых неоднозначны. Определенный оптимизм о благоприятном влиянии дополнительного назначения ингаляционного тиотропия продемонстрирован в крупном (912 больных с неконтролируемой БА на фоне применения комбинации ИГК с ДДБА). В группе пациентов, получавших в дополнение к ИГКДДБА тиотропий, имела место существенная пролонгация времени до обострения БА и более выраженная бронходилатация, чем в группе лиц, получавших плацебо.
Теофиллин
Теофиллин имеет слабую бронходилатирующую эффективность. При применении в низких дозировках оказывает также небольшое противовоспалительное действие в дыхательных путях. Данные о способности таблетированного теофиллина продленного действия длительно и успешно контролировать БА отсутствуют. Он может применяться дополнительно к терапии ИГК, если не достигается достаточный контроль заболевания. Отмена теофиллина в такой комбинации может сопровождаться с ухудшением контроля БА. При комбинации с ИГК теофиллин менее эффективен, чем ДДБА.
Побочные эффекты. Применение теофиллина в дозе 10 мкг/кг/сут и более может сопровождаться довольно существенными побочными эффектами. В связи с этим необходим тщательный подбор дозы препарата. Побочные эффекты включают гастроинтестинальные симптомы, тахикардию, различные аритмии. Увеличение плазменных уровней теофиллина особенно сопровождается увеличением риска развития побочных при заболеваниях печени, застойной сердечной недостаточности, одновременном приеме ряда лекарственных препаратов (циметидин, хинолоны, макролиды).
Кромоны: кромогликат натрия и недокромил натрия
Роль кромогликата натрия и недокромила натрия в лечении БА очень ограничена. Имеются сообщения об их эффективности у больных с легкой астмой и при постнагрузочном бронхоспазме. Их противовоспалительный эффект слабый и значительно уступает ИГК.
Побочные эффекты не существенны и включают кашель, проявляющийся во время ингаляции и раздражение слизистой оболочки глотки.
Антитела к IgE.
Применение анти-IgE-антител (омализумаб) ограничивается больными с тяжелой БА и высокими сывороточными уровнями IgE, где использование ИГК не способно обеспечить достаточный контроль заболевания. Применение омализумаба в комбинации с ИГК безопасно.
Системные глюкокортикоиды (СГК).
Длительное применения (более 2-х недель) пероральных СГК ограничивается редкими случаями тяжелой БА, не контролируемой общепринятыми лечебными подходами. Длительное применение СГК ограничено развитием тяжелых побочных эффектов, включающих развитие остеопороза, спонтанных переломов, сахарного диабета, АГ, ожирения, мышечной слабости, гипокалиемии, истончение кожи, угнетением гипоталамо-гипофизарно-надпочечниковой системы. Пациентам, вынужденным длительно принимать СГК, следует также принимать препараты для профилактики остеопороза.
Другие лечебные подходы, предлагаемые для контроля БА.
С целью уменьшения побочных эффектов глюкокортикоидов делаются попытки их комбинации с препаратами цитотоксического действия (например, метотрексатом). Однако существенные побочные эффекты метотраксата и не подтвержденный в крупных контролируемых исследованиях эффект не позволяют сегодня рекомендовать его в широкой клиническойю практике.
Эффективность длительного применения макролидов при БА активно изучается. Сделать вывод об обоснованности их применения можно будет только после окончания крупных исследований.
Аллергенспецифическая иммунотерапия (АСИТ).
Роль АСИТ в лечении БА у взрослых ограничена. Для проведения адекватной иммунотерапии необходимо знать клинически значимые антигены у конкретного пациента. С целью формирования толерантности вводятся специфические аллергены в нарастающих дозах. По данным крупного Кокрановского метаанализа (75 контролируемых рандомизированных исследований), у больных с БА специфическая иммунотерапия показала благоприятный эффект по сравнению с плацебо, включающий снижение количества и тяжести симптомов, потребности в медикаментах для базисной терапии, а также гиперреактивности дыхательных путей. Однако представленный благоприятный эффект заметно уступает традиционным медикаментозным подходам при лечении БА. Кроме того, применение АСИТ сопряжено с рядом побочных эффектов (местных и системных). Системные побочные эффекты включают анафилактические реакции, тяжелое обострение БА. Описаны летальные исходы у больных с БА при применении АСИТ.
Возможность применения АСИТ может быть рассмотрена у пациентов, у которых тщательная элиминация аллергенов и традиционная базисная терапия с применением ИГК не позволили достигнуть контроля БА.
Ведение обострений БА.
Современное определение обострений БА приведено в Рекомендациях Американского торакального общества и Европейского респираторного общества по определению контроля и обострений астмы (2009 г.) и Рекомендациях GINA (2014 г.): Обострения БА – острые или подострые эпизоды прогрессирования ее симптомов БА (одышки, кашля, свистящего дыхания, скованности грудной клетки или их сочетания) относительно привычного для пациента уровня. Эти эпизоды принципиально отличаются от неудовлетворительного контроля астмы: при обострении БА обычно отсутствует значительная суточная вариабельность показателей скорости воздушного потока (ключевой маркер неудовлетворительного контроля БА), но наблюдается их снижение по сравнению с состоянием до обострения.
Можно отметить, что в современных клинических рекомендациях подчеркнута практическая невозможность отличить легкие ОА от транзиторной утраты контроля БА.
Алгоритм лечебной тактики при ОА представлен на рисунке 3.
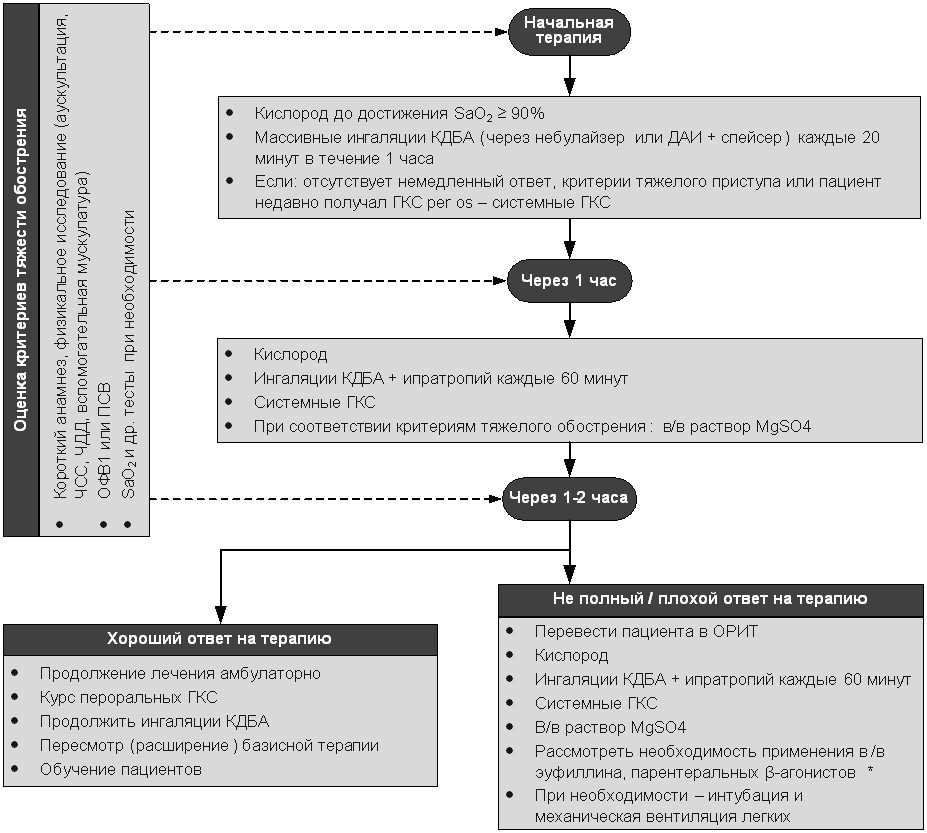
Рисунок 3. Алгоритм лечения обострения БА. КДБА – короткодействующие бета-агонисты; ДАИ – дозированный аэрозольный ингалятор; ГКС – глюкокортикостероиды; ОРИТ –отделение реанимации и интенсивной терапии; * – присутствует только Рекомендациях GINA.
Лечение обострений БА преследует следующие цели: 1) поддержание адекватной сатурации кислорода, 2) улучшение функции внешнего дыхания и 3) уменьшение воспаления в бронхах для ускорения разрешения бронхиальной обструкции и предотвращения рецидива обострения. Для достижения этих целей применяют ряд обсуждаемых ниже лечебных подходов.
КДБА занимают ведущее место в терапии ОА. Сальбутамол, применяемый как в виде ДАИ, так и виде раствора для небулизации, благодаря своей высокой бронходилатирующей эффективности, быстрому началу действия и хорошей переносимости является самым часто используемым КДБА во всем мире. Во всех современных рекомендациях подчеркивается, что ингаляционные КДБА должны получать все пациенты с обострениями БА, ввиду того что «… это самый эффективный способ устранения бронхиальной обструкции. Примерно у 60-70% пациентов наблюдается достаточная бронходилатирующая эффективность и хорошая переносимость повторных доз КДБА уже на начальном этапе оказания помощи при ОА» (GINA 2014). При купировании ОА используются высокие дозы КДБА. В случае использования небулайзерных ингаляций обычно применяют сначала 5 мг сальбутамола (2 небулы), затем через каждые 20 минут дополнительно по 2,5 мг (по 1 небуле). При использовании сальбутамола в виде ДАИ со спейсером также используют высокие дозы. На начальном этапе терапии обычно применяют до 1200 мкг в течение первого часа. Обученный использованию ДАИ со спейсером медперсонал отмеряет по 1 дозе сальбутамола в спейсер, контролирует правильность вдоха пациентом и повторяет это еще 3 раза до достижения общей дозы 400 мкг. В дальнейшем такая последовательность повторяется каждые 20 минут. На следующих этапах доза сальбутамола может быть увеличена (в зависимости от тяжести обструкции) до 6-10 вдохов через спейсер каждый час.
Использование высоких доз β2-агонистов при тяжелой обструкции объясняется необходимостью в преодолении существенных анатомических препятствий (отек слизистой, спазм, скопления слизи в просвете бронхов), а также дозозависимым характером эффективности КДБА. Безопасность таких доз подтверждена длительной клинической практикой и обширной доказательной базой. Убедительно доказано, что даже удвоение рекомендуемой дозы сальбутамола (до 2,4 мг в час, по 4 последовательные дозы через через ДАИ спейсер каждые 10 минут или по 2,5-5 мг каждые 20 минут через небулайзер), обеспечивает низкую сывороточную концентрацию и минимальное количество побочных эффектов.
У пациентов, у которых после начальной терапии сохраняется выраженная бронхиальная обструкция (ОФВ1 и ПСВ < 40-50%) к лечению добавляются ингаляции ипратропия бромида. Установлено, что при тяжелом обострении БА он совместно с сальбутамолом заметно улучшает функцию внешнего дыхания. Применяется в виде ДАИ спейсер последовательно до 8 доз или по 0,5 мг через небулайзер каждые 60 минут.
Обсуждая ингаляционную терапию короткодействующими бронходилататорами, уместно напомнить, что отсутствие небулайзеров не является существенным препятствием для качественного лечения ОА. В ряде систематических обзоров показано, что корректное использование спейсеров (которые значительно более доступны и шире распространены) по эффективности ничем не уступает небулизации лекарственных веществ при любой степени тяжести ОА. Более того, есть данные, что использование ДАИ со спейсерами большого объема при адекватных дозах КДБА позволяет получить даже более быструю и выраженную бронходилатацию с меньшим количеством побочных эффектов, по сравнению с небулайзерными ингаляциями. Это особенно ценно для пациентов с очень тяжелой обструкцией, которым необходимо наиболее быстро обеспечить доставку большой дозы КДБА (на ингаляцию необходимой дозы через ДАИ со спейсером затрачивается 1-2 минуты, тогда как на небулайзерную ингаляцию в среднем 15-20 минут). Разумеется, использование обычного ДАИ без спейсера не имеет смысла, так как пациент с острой тяжелой бронхообструкцией обычно не в состоянии синхронизировать вдох с нажатием на клапан.
Глюкокортикоиды. Системные ГК являются основой противовоспалительной терапии при обострении БА, и должны применяться у большей части пациентов, за исключением случаев очень легких ОА. Они не обладают непосредственным бронходилатирующим эффектом, но очень эффективно уменьшают выраженность воспаления в дыхательных путях, за счет чего способствуют ликвидации обструкции и ускоряют купирование обострения. При применении рекомендуемых доз системных ГК требуется не менее 6-8 ч до появления эффекта на показатели скорости воздушного потока. Такая временная задержка наступления эффекта связана с геномным механизмом действия системных ГК. Этим же обусловлено то, что пероральное и внутривенное применение системных ГК эквивалентны по скорости наступления и выраженности эффекта у большинства пациентов, из-за чего во всех Рекомендациях по лечению обострений БА в/в введение системных ГК резервируется исключительно для пациентов с очень тяжелой обструкцией, у которых затруднено глотание. Рекомендуемые дозы системных ГК составляют 0,5-1 мг/кг/сутки (не более 50 мг/сутки).
Не менее важна роль системных ГК для профилактики рецидивов обострения после восстановления бронхиальной проводимости. Поэтому их курс в дозе около 60 мг/сутки необходимо продолжить в течение 5-7 дней после нормализации состояния, что является обязательным компонентом лечебной программы при ОА. В рекомендациях GINA 2014 отмечено, что при курсе системных ГК такой продолжительности, они могут быть отменены одномоментно, без постепенного снижения дозы.
Современные согласительные документы отводят следующее место ИГК в лечении обострений БА:
- в очень высоких дозах (будесонид до 3200 мкг/сутки, флютиказон до 1500 мкг/сутки) – в качестве альтернативы курсу пероральных ГКС после стабилизации/выписки у пациентов: 1) с нетяжелым обострением БА; 2) способных корректно использовать ИГК, и/или 3) плохо переносящих пероральные формы СГК;
- в обычных дозах (с учетом «step-up», расширения объема базисной терапии из-за обострения) – в качестве обязательного лечения, сопутствующего курсу пероральных ГКС.
Прочие медикаментозные подходы. Сульфат магнезии для в/в применения в дозе 2 г каждые 20 минут у взрослых и 25-75 мг/кг у детей (суммарно не более 2 г) улучшает вентиляционную функцию у пациентов с тяжелыми и жизнеугрожающими ОА, но не показан при нетяжелых ОА.
Применение внутривенного теофиллина (эуфиллина) для купирования бронхиальной обструкции при обострении БА в течение длительного времени являлось одним из ведущих подходов к лечению ОА. В то же время представлены убедительные доказательства, что эффективность метилксантинов в данной ситуации является менее чем скромной. Установлено, что применение эуфиллина значительно уступает ингаляционным КДБА по броходилатирующей активности. Добавление его к сальбутамолу дает дополнительный бронхолитический эффект только у 10% пациентов, но в большинстве случаев вызывает увеличение частоты таких побочных эффектов, как тремор, тахиаритмии, тошнота, возбуждение и тревожность. В ряде случаев позиция международных экспертов относительно эуфиллина достаточно строга, в частности, четко указывается, что рутинное применение эуфиллина при ОА является недопустимым.
Не менее категоричны эксперты в отношении парентерального применения β2-агонистов (адреналина, раствора сальбутамола для инъекций), отмечая, что внутривенное применение β2-агонистов не имеет преимуществ перед ингаляционным путем введения, не обосновано доказательной базой и не должно применяться при ОА.
Агрессивная гидратационная терапия у взрослых и детей старшего возраста также не имеет под собой никаких доказательных обоснований, и может применяться только у детей младшего возраста, у которых возможна дегидратация из-за тахипноэ и снижения потребления жидкости. У пациентов с ОА также не рекомендуется рутинное применение муколитиков, антибиотиков (в том числе макролидов), физиотерапии и седативных препаратов.






