Семинары
Уважаемые коллеги!
На свидетельстве участника семинара, который будет сгенерирован в случае успешного выполнения Вами тестового задания, будет указана календарная дата Вашего он-лайн участия в семинаре.
Семинар "ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА И ЛЕЧЕНИЕ СУСТАВНОГО СИНДРОМА"
Автор: Поворознюк В.В., Григорьева Н.В.
Проводит: Республиканский Медицинский Университет
Рекомендован по специальностям: Кардиология, Неврология, Ревматология, Семейная медицина/Терапия
Просмотров: 22 239
Дата проведения: с 01.06.2015 по 01.06.2016
 Суставным синдромом (СС) принято обозначать клинический симптомокомплекс, обусловленный поражением анатомических структур суставов при разнообразных заболеваниях и патологических процессах. Суставной синдром проявляется болями в суставах, их дефигурацией и деформацией, ограничением движений в суставах, изменениями сухожильно-связочного аппарата суставов и окружающих мышц. В основе патогенеза суставного синдрома лежат воспалительные или дистрофические изменения в суставах и околосвязочном аппарате, в легких случаях синдром проявляется только артралгиями.
Суставным синдромом (СС) принято обозначать клинический симптомокомплекс, обусловленный поражением анатомических структур суставов при разнообразных заболеваниях и патологических процессах. Суставной синдром проявляется болями в суставах, их дефигурацией и деформацией, ограничением движений в суставах, изменениями сухожильно-связочного аппарата суставов и окружающих мышц. В основе патогенеза суставного синдрома лежат воспалительные или дистрофические изменения в суставах и околосвязочном аппарате, в легких случаях синдром проявляется только артралгиями.
Суставной синдром может быть проявлением преимущественного поражения самих суставов или отражением системных поражений организма при различных заболеваниях, в том числе и диффузных заболеваниях соединительной ткани. В одних случаях поражение суставов является ведущим в клинической картине заболевания и определяет медико-социальный прогноз (ревматоидный артрит (РА), остеоартроз (ОА)). В других ситуациях СС является одним из проявлений некоторых заболеваний, маскируя их и затрудняя диагностику (острый вирусный гепатит в дебюте, неспецифический язвенный колит и др.). В каждом конкретном случае врач должен уметь оценить характер СС (локализация, число пораженных суставов, течение, внесуставные проявления и др.) для определения направления диагностического поиска с целью установления причины поражения суставов и верификации нозологического диагноза. Диагностический поиск при суставном синдроме условно может быть представлен в виде нескольких, последовательно проводимых этапов (табл. 1).
Таблица 1. Этапы дифференциальной диагностики суставного синдрома
|
1. |
Сбор анамнеза (анализ факторов риска, сопутствующих заболеваний, аутоиммунных заболеваний у родственников, связь с травмой, инфекцией) |
|
2. |
Клиническое обследование больного |
|
3. |
Дополнительные методы исследований: инструментальные, лабораторные и др. |
|
4. |
Консультации смежных специалистов (при необходимости) |
 Причины возникновения болей с вовлечением суставов чрезвычайно разнообразны, что существенно затрудняет проведение дифференциальной диагностики и верификацию диагноза. С целью ее проведения необходимо осуществить максимально полное обследование пациента с анализом возможных факторов риска и наличия сопутствующих заболеваний, использованием инструментальных и лабораторных методов обследования, а также, при необходимости, привлечения смежных специалистов (табл. 1).
Причины возникновения болей с вовлечением суставов чрезвычайно разнообразны, что существенно затрудняет проведение дифференциальной диагностики и верификацию диагноза. С целью ее проведения необходимо осуществить максимально полное обследование пациента с анализом возможных факторов риска и наличия сопутствующих заболеваний, использованием инструментальных и лабораторных методов обследования, а также, при необходимости, привлечения смежных специалистов (табл. 1).
Сбор анамнеза. На начальном этапе диагностического поиска необходимо убедиться в том, что имеющаяся симптоматика связана именно с суставной патологией, т.е. верифицировать поражение сустава (табл. 2). С этой целью следует исключить целый ряд синдромно-сходных заболеваний (синдромов), первично не связанных с артропатией. Например, боли внесуставного происхождения могут быть обусловлены первичным поражением периартикулярных тканей (мышечный, сухожильно-связочный аппарат), кожи, сосудов, периферических нервов, костных структур и другими факторами. К таким заболеваниям относят: бурситы; тендовагиниты (теносиновит) и лигаментиты, фиброзиты, миозиты (миалгии), синдром карпального канала, фасциит, ревматическая полимиалгия, поражения кожи и подкожной клетчатки (целлюлит, рожистое воспаление, узловая эритема, флегмона мягких тканей); тромбофлебит, поражение костей (остеопороз, остеомаляция).
Таблица 2. Варианты боли при поражении суставов, околосуставных тканей и внесуставных структур
|
Результаты исследования |
Боль |
||
|
периартикулярная |
суставная |
отраженная |
|
|
Опрос |
Только определенные движения болезненны |
Все движения в суставе болезненны |
Боль не связана с движением. Не четкой локализации боли, она может быть усилена путем трения |
|
Боль при движении |
Боль возникает при активных, и в меньшей степени, пассивных движениях в определенных направлениях (активные – ограничиваются избирательно) |
Одинаково при пассивных и активных движениях. Возникает при движении в различных направлениях |
Норма |
|
Диапазон движения |
Активные движения могут быть ограничены из-за боли. Пассивные движения в полном объеме |
Могут быть одинаково ограничены и активные, и пассивные движения |
Норма |
|
Сопротивление активным движениям |
Боль при определенных движениях |
Нет |
Нет |
|
Пальпация |
Болезненность в области проекции периартикуляр-ного образования (в отдалении от линии сустава). Точечная или локальная болезненность при пальпации. Ограниченная припухлость. Отсутствие местных признаков воспаления |
Болезненность над линией сустава. Местные признаки воспаления (припухлость, гипертермия, гиперемия). Деформации. Блокада сустава, крепитация |
Норма |
 Необходимо иметь в виду, что симптоматика поражения сухожильно-связочного аппарата может наблюдаться и при некоторых истинно «суставных» ревматических заболеваниях (тендиниты и бурситы при синдроме Рейтера, миалгии при системной красной волчанке (СКВ) и др.). Однако в большинстве случаев поражения околосуставных тканей представляют собой самостоятельные заболевания дегенеративного или воспалительного характера, требующие соответствующего лечения.
Необходимо иметь в виду, что симптоматика поражения сухожильно-связочного аппарата может наблюдаться и при некоторых истинно «суставных» ревматических заболеваниях (тендиниты и бурситы при синдроме Рейтера, миалгии при системной красной волчанке (СКВ) и др.). Однако в большинстве случаев поражения околосуставных тканей представляют собой самостоятельные заболевания дегенеративного или воспалительного характера, требующие соответствующего лечения.
Опрос пациента с СС должен быть направлен на выявление особенностей его возникновения и течения. Необходимо уточнить предполагаемую причину и время возникновения СС, а также возможную связь СС с предшествующим стрессом, тяжелыми нагрузками, длительными заболеваниями, отъездом в другие страны. Уточняющие вопросы необходимы для выявления связи возникновения СС с фактами, которым сам пациент может не придавать значения и, соответственно, не указывать в жалобах и при сборе анамнеза. Например, травма сустава является основанием для консультации ортопеда-травматолога, а наличие псориаза – консультации дерматолога. Больной может не связывать перенесенный месяц назад уретрит или энтероколит с фактом возникновения в настоящее время СС, и только прицельный вопрос о наличии «триггерных» факторов в анамнезе может позволить вовремя заподозрить реактивный артрит (РеА). Если пациент отмечает частое возникновение простудных заболеваний, ОРВИ, гриппа, а также наличие очагов хронической инфекции (хронический тонзиллит, пиелонефрит, синуситы, воспалительные заболевания полости рта и мочеполовой сферы) необходимо заподозрить наличие артрита, ассоциированного с инфекцией. Данные о наличии у больного онкологического заболевания позволяют подозревать развитие паранеопластического артрита, а ранее диагностированные аутоиммунные заболевания и развитие острого СС могут свидетельствовать о возможном обострении воспалительного процесса.
При обследовании больного с СС, прежде всего, необходимо дифференцировать воспалительное поражение суставов от других причин возникновения СС невоспалительного характера (табл. 3), которые также могут сопровождаться жалобами пациентов на боли в суставах.
При обследовании больного с СС необходимо обязательно уточнять наличие у пациента «типичных» жалоб и признаков, позволяющих заподозрить конкретное заболевание. Наличие «утренней скованности» более 1 часа типично для РА, моноартрита с поражением первого плюснефалангового сустава характерно для подагрического артрита. Мигрирующий характер болевого синдрома, его начало с суставов нижних конечностей в сочетании с энтезитом встречается чаще при РеА, а наличие «хруста» и щелчков при движении является достоверным признаком ОА.
Таблица 3. Заболевания, сопровождающиеся суставным синдромом
|
Воспалительные поражения суставов |
Невоспалительные заболевания |
|
· Инфекционные артриты (инфекционные неспецифические артриты: гепатиты, мононуклеоз, токсоплазмоз, боррелиоз, ВИЧ, сифилис). · Кристаллические артриты: подагра, псевдоподагра. · Артриты аутоимунной этиологии: ревматоидный артрит (РА), системная красная волчанка (СКВ), болезнь Шегрена, полимиозит, серонегативные спондилоартриты и др. · Реактивные артриты: ревматическая полимиалгия, синдром Рейтера |
· Травмы (острый посттравматический артрит, посттравматический артроз, ушибы суставов, растяжения сухожилий, внутрисуставной перелом). · Дегенеративные заболевания суставов (остеоартроз): коксартроз, гонартроз, артрозы мелких суставов кистей и стоп, артрозы других локализаций. · Гиперпластические процессы (доброкачественная гигантоклеточная синовиома). · Метастазы в кости, параканкрозный артрит |
Основными субъективными проявлениями суставного синдрома являются боли и нарушение (ограничение) подвижности (табл. 4). Боль в суставе является самым ранним, а иногда единственным субъективным симптомом их поражения, однако механизм возникновения боли при поражении суставов различного характера неодинаков.
Таблица 4. Симптомы суставного синдрома
|
Субъективные симптомы |
Объективные симптомы |
|
|
В возникновении болей в суставе важную роль играют механические факторы – механическая перегрузка сустава, растяжение сухожильно-связочного аппарата, раздражение синовиальной оболочки, микроциркуляторные расстройства, обменные нарушения в костной ткани, развитие в суставе воспалительных и дегенеративных изменений. Вследствие этих процессов в тканях суставов накапливаются вещества-алгетики (тканевые протеазы, кинины, простагландины, гистамин, серотонин), которые раздражают болевые рецепторы и дают начало дуге болевого рефлекса. Боль при СС преимущественно ноцицептивная и возникает тогда, когда повреждающий ткань раздражитель действует на периферические болевые рецепторы (ноцицепторы). Последние находятся в синовиальной оболочке, фиброзной капсуле суставов, периосте костей, адвентиции микрососудов, связках и сухожилиях. Их нет в хряще и менисках. Возникновение боли связывают с раздражением окончаний чувствительных нервов синовиальной оболочки суставной капсулы продуктами воспаления, иммунных реакций, токсинами, кристаллами солей (например, уратами), остеофитами и др.
По своему физиологическому назначению ноцицептивная боль – предупреждающий сигнал о возникновении в организме нарушений или повреждений, следовательно, она выполняет важнейшую защитную функцию в организме. Но если боль сохраняется после окончания действия повреждающего фактора и периода заживления, она утрачивает свое сигнальное значение. Хроническая боль практически не несет позитивной направленности, превращаясь из сигнального симптома в самостоятельное заболевание. Меняется также клиническая картина: боль не контролируется анальгетиками, появляются другие симптомы, снижается работоспособность и нарушается качество жизни пациента.
Ноцицептивная боль – это чаще всего острая боль со всеми присущими ей характеристиками. Характерным для этого типа боли является их быстрый регресс после прекращения действия повреждающего фактора и проведения короткого курса лечения анальгетическими средствами.
Боли в суставах являются постоянным симптомом при ревматических заболеваниях. У больных артритом боль в пораженных суставах связывают с диффузными воспалительными изменениями в суставной капсуле и околосуставных мягких тканях из-за активации ферментативных систем, растяжения капсулы и смежных с ней связок внутрисуставным выпотом при его быстром и значительном накоплении, а также из-за рефлекторного спазма околосуставных мышц (с целью защитного ограничения движений, вызывающих боль).
При хроническом артрите возникновение боли связано с растяжением при движениях, фиксированных вследствие фиброза участков капсулы и связок. Фиброз также приводит к сдавлению нервных окончаний, формируя предпосылки для возникновения другого вида боли – нейропатической.
При ОА боль возникает из-за разрушения суставного хряща с изменениями в субхондральной кости и снижением способности суставных поверхностей переносить нагрузку, это приводит к повышению давления на кость и микропереломам.
При опросе пациента обязательно выясняются параметры суставных болей – точная локализация, характер, длительность, интенсивность, время появления в течение суток.
Второй субъективный симптом СС – ограничение движений в суставах. Степень выраженности этого признака обычно прямо пропорциональна тяжести органических и функциональных изменений в суставах.
Клиническое обследование. При объективном обследовании больного с СС принципиально важным является соблюдение классической методики обследования пациента по органам и системам, что позволяет выявить те признаки и симптомы, которые в дальнейшем помогут сформировать предварительный диагноз.
Осмотр больного позволяет выявить изменения кожного покрова. Наличие гиперемии, припухлости и гипертермии в области суставов указывают на воспалительный характер суставного процесса и позволяют в большинстве случаев исключить ОА (за исключением ОА с вторичным синовитом). Изменения на коже, наличие эритемы, проявлений геморрагического синдрома, феномена Рейно, выявление тофусов, увеличение лимфатических узлов – далеко не полный перечень признаков, наличие которых позволяет заподозрить определенные заболевания и, в дальнейшем, обследовать больного с «прицелом» на подтверждение или исключение данного предварительно диагноза.
Пальпация необходима для установления характера суставного синдрома. При этом оценивают наличие или отсутствие синовиита исследуемого сустава, а также степень выраженности болевого синдрома.
Количественная оценка болевого синдрома чаще всего проводится клинически, а также с помощью визуально-аналоговых или вербально-аналоговых шкал (ВАШ). Для этого используют 4- или 11-составную ВАШ, Мак-Гилловский болевой опросник, опросник WOMAC. Оценка выраженности болевого синдрома важна с учетом подбора адекватного анальгетического средства для его купирования.
К объективным признакам поражения суставов относят дефигурацию и деформацию суставов, припухлость, покраснение кожи над суставами, нарушение их функции. Дефигурация сустава (или суставов) – это изменение формы сустава за счет воспалительного отека синовиальной оболочки и периартикулярных тканей, выпота в полость сустава, гипертрофии синовиальной оболочки и фиброзно-склеротических изменений околосуставных тканей. Деформация суставов – это стойкое изменение формы суставов за счет костных изменений, развития анкилозов, подвывихов. Припухлость в области сустава может быть при обоих указанных состояниях. Покраснение кожи над пораженными суставами обусловлено локальным повышением кожной температуры и свидетельствует об активном воспалительном процессе в суставе.
При осмотре и пальпации пораженных суставов ориентировочно устанавливают ограничение объема движений, свойственных данному суставу. Оценивают ограничение активных и пассивных движений в суставах.
При подозрении на наличие у пациента ревматического заболевания необходимо первоначально выделять две большие группы заболеваний. На основании жалоб, данных анамнеза и обследования всех пациентов можно разделить на имеющих признаки артрита или признаки обменно-дистрофических заболеваний (табл. 5). Разделение пациентов на данные группы позволяет упростить проведение дифференциально-диагностических мероприятий, а также влияет на проведение адекватной терапии на этапе верификации диагноза. Наличие классических признаков воспаления в области суставов позволяет заподозрить наличие у больного одного из воспалительных ревматических заболеваний.
Таблица 5. Дифференциальный диагноз воспалительного и невоспалительного поражения суставов
|
Признак |
Воспалительное поражение суставов |
Невоспалительное поражение суставов |
|
Утренняя скованность |
Длительная (больше 1 часа), провоцируемая продолжительным отдыхом |
Появляется после короткого отдыха, длится меньше часа (20 минут) |
|
Боль |
Проходит после двигательной активности и приема противо-воспалительных препаратов |
Усиливается при физической активности |
|
Признаки воспаления |
Общие признаки воспаления (утомляемость, лихорадка, похудение). Увеличение CОЭ и СРБ и других воспалительных маркеров |
Боль не сопровождается местными, общими и лабораторными признаками воспаления |
|
Гипертермия |
Есть |
Отсутствует |
|
Боль при активных движениях |
Есть |
Отсутствует |
|
Припухлость мягких тканей |
Есть |
Отсутствует |
|
Синовиит |
Выражен |
Возможна |
|
Костная крепитация, образование остеофитов |
Отсутствуют |
Выражены |
|
Ослабление связочного аппарата |
Отсутствует |
Возможна |
|
Нестабильность |
Отсутствует |
Возможна |
При дифференциальной диагностике СС важным является оценка течения и темпов развития СС, который условно может быть квалифицирован как острый и хронический (табл. 6). Для одних заболеваний типично острое воспаление суставов (острый подагрический артрит, псевдоподагра) с полным обратным развитием симптомов, в то время как при других заболеваниях СС характеризуется длительно текущим, прогрессирующим артритом (РА, ОА).
Таблица 6. Характеристики острого и хронического воспаления суставов
|
Острое воспаление суставов |
Хроническое воспаление суставов |
|
|
При дифференциальной диагностике СС важным также является оценка локализации суставного процесса (рис. 1), симметричности и числа пораженных суставов. Суставной синдром может характеризоваться поражением одного сустава (моноартрит), двух или трех суставов (олигоартрит) и вовлекать более трех суставов (полиартрит). Кроме того, чрезвычайно важным является не только количество вовлеченных в патологический процесс суставов, но и их локализация (табл. 7).
Таблица 7. Особенности локализации пор ажения суставов при различных заболеваниях
|
Острый моноартрит первого плюсне-фалангового сустава |
Требует исключения подагры |
|
Артрит крестцово-подвздошного сочленения |
Анкилозирующий спондилоартрит или другие серонегативные артриты |
|
Хронический моноартрит коленного сустава |
Требует исключения туберкулезного поражения |
Важным диагностическим признаком у больных СС является наличие внесуставных проявлений, спектр которых достаточно обширен и разнообразен по своим клиническим проявлениям. Характер внесуставных проявлений определяется основным заболеванием и в ряде случаев может быть ключом к расшифровке СС (тофусы при подагре, ревматоидные узелки при ревматоидном артрите, ириты и иридоциклиты при анкилозирующем спондилоартрите и т.д.) (табл. 8).
Таблица 8 . Характер внесуставных поражений
|
Заболевание |
Признаки |
|
Подагра |
Тофусы |
|
РА |
Ревматоидные узелки. Поражение периартикулярных тканей кисти с формированием стойких деформаций в виде «бутоньерки» или «лебединой шеи» |
|
Анкилозирующий спондилоартрит |
Ириты и иридоциклиты |
|
Болезнь Рейтера |
Конъюнктивит, уретрит |
|
Артрит при болезни Крона и неспецифическом язвенном колите |
Узловатая эритема. Иридоциклит, увеит. Язвы полости рта |
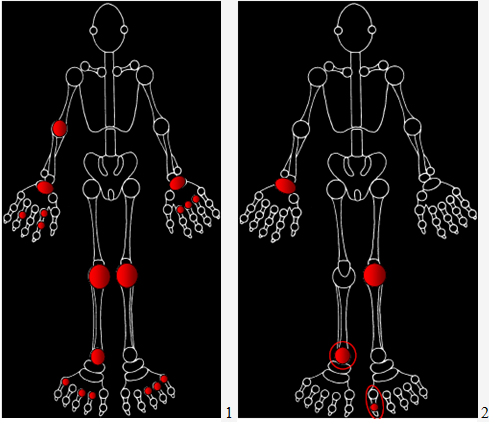
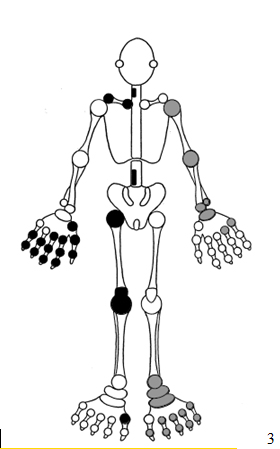
Рисунок 1. Локализация суставного синдрома при различных заболеваниях:
1. Ревматоидный артрит. 2. Серонегативные спондилоартропатии. 3. Остеоартроз (целевые суставы окрашены слева черным; суставы, относительно не вовлекаемые в заболевание окрашены справа серым цветом)
При обследовании необходимо уточнить, в какое время суток артрит больше всего беспокоит больного, возможное вовлечение позвоночника и наличие сакроилеита (в том числе, боли в области ягодиц).
Дифференциальная диагностика артритов в зависимости от локализации, количества вовлеченных суставов и длительности заболевания представлена в табл. 9.
Таблица 9. Дифференциальная диагностика артритов в зависимости от количества вовлеченных суставов, их локализации и длительности заболевания
|
Острый моноартрит |
· Основные причины: септический артрит (рис. 2) и кристаллические синовииты (подагра и псевдоподагра). · Кристаллические артриты (рис. 3) характеризуются очень быстрым началом (боль и отек – максимальное развитие в течение 6-24 часов), очень сильной болью (часто описывается как нетерпимая), повышенной кожной чувствительностью (больной часто не в состоянии соприкасаться пораженным суставом с одеждой или бельем), выраженным синовиитом с напряженным выпотом, отеком мягких тканей и эритемой (особенно подагра), купируется самостоятельно, даже без лечения, в течение нескольких дней или недель. · Следует дифференцировать с посттравматическим синовиитом, палиндромным ревматизмом, реактивным артритом, псориатическим артритом и бактериальным эндокардитом |
|
Хронический воспалительный моноартрит |
· Основные возможные причины: инфекции (бруцелла, микобактерии туберкулеза, болезнь Лайма и др.), моно- или олигоартикулярный дебют полиартрита (ювенильный идиопатический артрит, реактивный артрит, серонегативные спондилоартропатии), и инородное тело (напр., повреждение шипами растений). · Дифференциальная диагностика должна проводиться с заболеваниями невоспалительного характера (остеоартрит/остеоартроз (рис. 4), рецидивирующий гидрартроз, остеонекроз, хронический региональный болевой синдром (рис. 5), нейропатическая болезнь суставов (суставы Шарко)) и опухолями, включая пигментный виллонодулярный синовиит |
|
Хронический симметрич ный периферический полиартрит |
· Подобная картина является общей для многих ревматических заболеваний, особенно заболеваний соединительной ткани, таких какРА (рис. 6), СКВ (рис. 7) , первичный синдром Шегрена, полимиозит и смешанные заболевания соединительной ткани. · Псориатический артрит может также манифистировать периферическим полиартритом, хотя наблюдается тенденция к асимметричному поражению и связь с поражением либо дистальных межфаланговых или крестцово-подвздошных суставов. · ОА с отложением пирофосфата кальция чаще встречается у пожилых пациентов. Наличие в анамнезе генерализованного ОА с рецидивирующими воспалительными эпизодами подтверждает это предположение. · Хронический полиартрит при подагре также может иметь сходную клиническую картину, однако ему почти всегда предшествует факт моноартрита в анамнезе. · Вирусные артриты, связанные с парвовирусом В19, ВИЧ и гепатитами, могут иметь сходную клиническую картину, однако имеют более острое начало, чем РА или другие заболевания соединительной ткани. · Дифференциальный диагноз данного вида полиартрита основывается на тщательной оценке внесуставных проявлений |
|
Хронический асимметричный олиго/полиартрит |
· Псориатический артрит (рис. 8) является наиболее частой причиной данной формы артрита. Для его подтверждения чрезвычайно важен анамнез, в том числе и семейный, наличия псориаза. · При поражении проксимальных и дистальных межфаланговых суставов альтернативным диагнозом может быть остеоартроз суставов кисти (узелки Гебердена и Бушара), хотя он, как правило, имеет более медленное развитие, однако может сопровождаться и эпизодами синовиитов. · Хроническая артропатия при саркоидозе может манифистировать данным видом артрита, для нее характерно асимметричное поражение суставов. · Другие серонегативные спондилоартропатии, в частности анкилозирующий спондилоартрит (рис. 9) также могут манифестировать данной формой артрита, однако сопровождаются наличием боли в спине воспалительного характера, а также наличием боли в ягодицах (из-за наличия сакроилеита). · Реактивные артриты или артриты, связанные с воспалительным заболеванием кишечника сопровождаются развитием данного вида артрита, однако, в большей степени поражаются дистальные суставы с симметричным их поражением. · Другие причины хронического асимметричного олиго/полиартрита включают дебют ревматоидного артрита, ювенильный идиопатический артрит, подагрический полиартрит, ОА, кальций-пирофосфатную артропатию, болезнь Бехчета. · Дифференциальный диагноз данного вида полиартрита основывается на тщательной оценке внесуставных проявлений, включая наличие энтезопатий, увеита и др. |
|
Проксимальные олигоартриты |
· Наиболее распространенной причиной данного вида артрита являются серонегативные спондилоартропатии. Наличие боли воспалительного характера в пояснице, личный или семейный анамнез псориаза, воспалительные заболевания кишечника, анкилозирующий спондилит, увеит и возникновение любого инфекционного заболевания (инфекционной диареи, инфекции мочевыводящих путей) в течение нескольких недель, предшествующих артриту, должны быть учтены при обследовании больного. Другие причины проксимального олигоартрита включают болезнь Бехчета, ювенильный идиопатический артрит и ранний ревматоидный артрит. · Нередко данный вид артрита не соответствует определенным классификационным критериям и часто описывается как идиопатический олигоартрит. |
|
Артрит суставов плечевого и поясничного пояса |
· Артрит данной локализации характеризуется болью воспалительного характера с выраженной скованностью в области плечевого и поясничного пояса. · Физикальное обследование выявляет признаки артрита плечевых и/или тазобедренных суставов, иногда с незначительным вовлечением периферических суставов. · Ревматическая полимиалгия является наиболее частым вариантом данного вида артрита. Пациент, как правило, пожилой человек, с болью и скованностью в шее, плечевой и бедренной области. Также могут быть вовлечены и периферические суставы. · Важно также подтверждение наличия и внесуставных проявлений – недомогания, лихорадки, усталости, потери аппетита и веса |
Дифференциальная диагностика СС при различных заболеваниях представлена в табл. 10.
Таблица 10. Дифференциальная диагностика суставного синдрома при различных заболеваниях
|
Ревматоид-ный артрит |
Симметричный полиартрит с поражением суставов кистей (II и III пястно-фаланговые и проксимальные межфаланговые), плюсне-фаланговых, коленных, лучезапястных, голеностопных суставов. Моно- или олигоартрит (чаще коленного сустава), имеющий стойкое, подострое и доброкачественное течение. · артрит 3 суставов и более длительностью более 3 мес; · артрит суставов кисти; · симметричный артрит мелких суставов; · утренняя скованность (не менее 1 ч); · ревматоидные узелки; · ревматоидный фактор в сыворотке крови (титр 1/4 и выше); · рентгенологические признаки (эрозивный артрит, околосуставной остеопороз) |
|
СКВ |
· Острый или подострый мигрирующий полиартрит, подобный ревматическому. · Возникают резкие, иногда «морфинные» боли в первом плюснефаланговом суставе подобно подагре. · Поражение мелких суставов кисти, как при ревматоидном артрите |
|
Подагра |
· Приступ развивается внезапно (обычно ночью). · Характерны сильные боли, чаще всего в I-ом плюснефаланговом суставе, его припухлость, яркая гиперемия кожи с последующим шелушением. · Лихорадка (иногда до 40 градусов), озноб, лейкоцитоз, увеличение СОЭ. · Через 5-6 дней признаки воспаления полностью исчезают. · Продолжительность приступов от 3 дней до 1,5 месяцев. · Острые приступы повторяются с различными интервалами, захватывая все большее количество суставов, развивается хронический подагрический артрит со стойкой припухлостью и деформацией. · Раньше всего вовлекаются мелкие суставы стоп |
|
Псориати-ческий артрит |
Хроническое воспалительное заболевание суставов, ассоциированное с псориазом. Асимметричный олигоартрит (70 %). Асимметричность – наиболее характерная черта. Артрит дистальных межфаланговых суставов. Симметричный ревматоидоподобный артрит. Мутилирующий артрит. Псориатический спондилит |
|
Мутилирую-щий артрит |
· Тяжелый деструктивный артрит дистальных отделов пальцев кистей и стоп, их остеолиз. · Наблюдается укорочение фаланг с их деформацией по типу «пера в чернильнице». · Возникает патологическая подвижность фаланг. · Часто сочетается с поражением позвоночника |
|
Болезнь Рейтера |
Триада: артрит, конъюнктивит, уретрит. При присоединении к ним поражений кожи и других слизистых оболочек, говорят о тетраде Рейтера. Суставной синдром при болезни Рейтера: · Чаще полиартрит – 3 и более суставов (65%). · Олигоартрит (29%). · Моноартрит (6%). · Острое или подострое начало. · Чаще поражаются суставы нижних конечностей · Артрит всегда асимметричный с частым вовлечением суставов большого пальца стоп, имитирующим псевдоподагрический приступ. · Часто артрит межфаланговых суставов стоп с диффузным их припуханием в виде сосисок. · Односторонний сакроилеит. Очень характерны тендиты и бурситы (ахиллобурситы, подпяточные бурситы, периоститы пяточных бугров – «рыхлые пяточные шпоры»). Их выявление всегда позволяет заподозрить у молодых мужчин болезнь Рейтера, даже при отсутствии других клинических проявлений |
|
Артрит при болезни Крона и неспецифи-ческом язвенном колите |
· Асимметричный моно- или олигоартрит крупных суставов (чаще нижних конечностей). · Односторонний сакроилеит, редко анкилозирующий спондилоартрит по типу болезни Бехтерева (обычно предшествует кишечным проявлениям). · Узловатая эритема. · Иридоциклит, увеит. · Язвы полости рта |
|
Инфекцион-ные артриты |
· СС наблюдается наряду с другими проявлениями инфекционно-воспалительного процесса (пневмония, сепсис, менингит и др.) в разгар заболевания. · Протекают по типу острого моно- или олигоартрита, не прогрессируют, проходят бесследно, как правило, не приводят к деформации. · Возможно рецидивирующее течение, а в ряде случаев заболевание протекает по типу хронического артрита (хламидийные артриты). · Острые септические (гнойные) артриты возникают обычно при бактериемии у больных пневмонией, инфекционным эндокардитом, менингитом, некоторыми другими инфекциями, а также при проведении внутрисуставных диагностических и лечебных манипуляций |
|
Туберкулезный артрит |
· Возникает при гематогенном проникновении микобактерий из первичного туберкулезного очага (обычно в легком). · Чаще всего поражаются крупные суставы (коленный, тазобедренный, голеностопные). · Протекает по типу хронического моноартрита (синовита). · СС может носить параспецифический характер (туберкулезный ревматизм Понсе), проявляться артралгиями, полиартритом (реже моноартритом) и свидетельствует о наличии активного туберкулезного процесса (легкие, лимфоузлы, гениталии) |
|
Гонококковый артрит |
· Чаще возникает у женщин в связи с более поздней диагностикой и отсутствием лечения гонококковой инфекции из-за стертости клинической картины. · Характерен моно- или олигоартрит, в дебюте СС возможно развитие полиартрита. · Обычно сопровождается высокой лихорадкой, ознобами, лейкоцитозом. · Важным подтверждением диагноза является наличие кожных поражений в виде периартикулярных пустул |
|
Лайм-артрит |
· Вызывается боррелией (из рода спирохет), переносимой при укусе иксодовыми клещами. · Клиническая картина характеризуется острым, нередко рецидивирующим моно- или олигоартритом в сочетании с мигрирующей эритемой в виде пятна или папулы, неврологической симптоматикой (менингоэнцефалит), миоперикардитом. · Диагноз верифицируется при выделении культуры спирохеты или IgG-антител к ней. |
|
Параканкроз-ный полиартрит |
· Асимметричный артрит преимущественно суставов нижних конечностей у лиц старше 65 лет. · Чаще у женщин, в 80 % случаев диагностируют рак молочной железы. · Клиническая картина может соответствовать клинике серонегативного ревматоидного артрита |
|
Гипертрофи-ческая остео-артропатия ( первичная и вторичная) |
· Первичная форма не ассоциирована с системными заболеваниями. · Среди вторичных причин ведущее место принадлежит злокачественным опухолям. Наиболее часто развивается при опухолях легких, особенно при аденокарциноме (в 12 % случаев), а также при болезнях легких, осложненных дыхательной недостаточностью. Кроме того, развивается при мезотелиоме, метастазах почек, лимфогранулематозе, тимоме, лейомиоме пищевода, остеогенной саркоме, фибросаркоме, недифференцированной назофарингеальной опухоли. · Клинически проявляется утолщением концевых фаланг пальцев кистей и стоп за счет локальной пролиферации кожи и костной ткани, что приводит к формированию так называемых «барабанных палочек», периоститу трубчатых костей, олиго- или полисиновиитам |
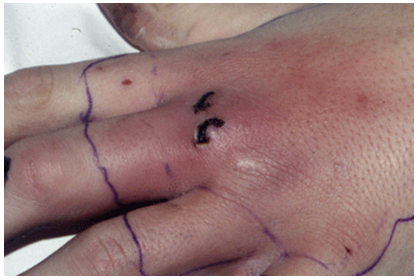
Рисунок 2. С ептический артрит
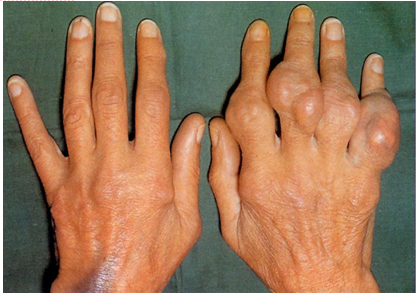
Рисунок 3. Подагрический артрит
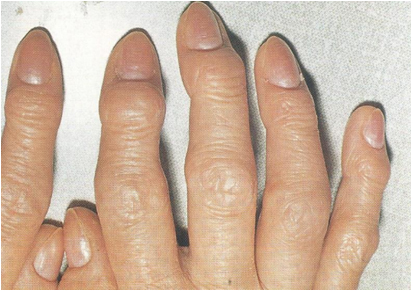
Рисунок 4. Остеоартроз (Узелки Гебердена и Бушара)
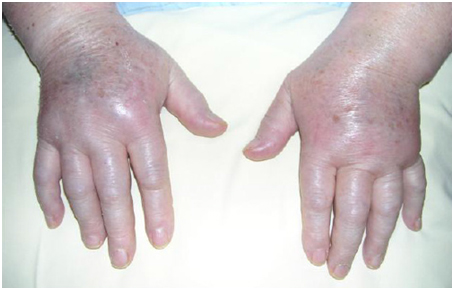
Рисунок 5. Комплексный региональный болевой синдром.
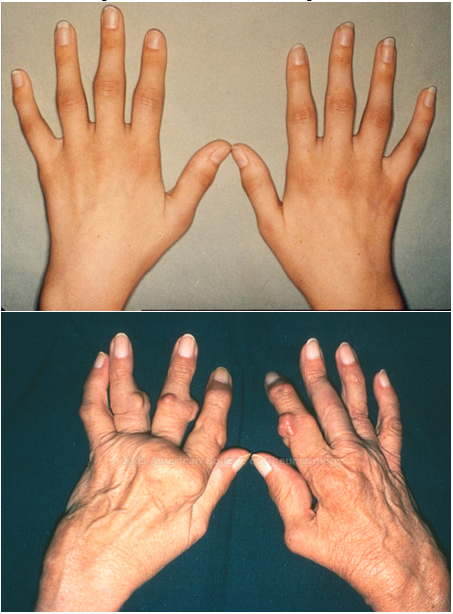
Рисунок 6. Ревматоидный артрит
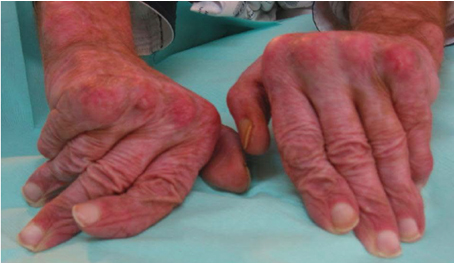
Рисунок 7. Артропатия при СКВ
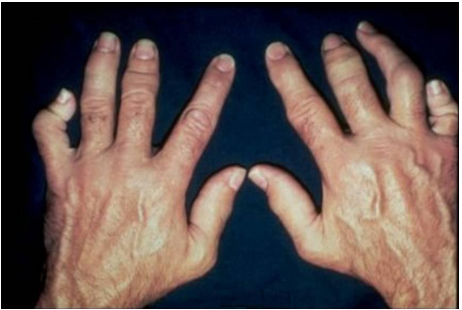
Рисунок 8. Артрит при анкилозирующем спондилите
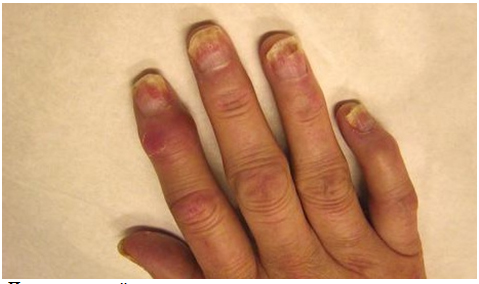
Рисунок 9. Псориатический артрит
Дополнительные методы исследования при СС включают функциональные (гониометрию), лабораторные и дополнительные инструментальные методики.
Гониометрия – это объективная оценка двигательной функции суставов, которая производится с помощью измерения углов тех или иных направлений движений в данном суставе специальными приборами – гониометрами, которые устанавливают по проекции осей конечностей, и при движении бранш синхронно с движениями в суставах образуются углы, величину которых измеряют в градусах.
К лабораторным методам исследования относят методы исследования активности воспалительного процесса, нарушений иммунного статуса и исследование синовиальной жидкости.
Рутинный комплекс исследований активности воспалительного процесса предполагает определение лейкоцитоза, лейкоцитарной формулы и СОЭ в клиническом анализе крови. При активном воспалении отмечают умеренный лейкоцитоз, нейтрофилез, сдвиг лейкоцитарной формулы влево, ускорение СОЭ. Оценивают «показатели острой фазы» или «острофазовые показатели» – С-реактивный белок, фибриноген, сиаловые кислоты, протеинограмма.
У больных с активным воспалительным процессом в крови повышается содержание С-реактивного белка (свыше 0,4 г/л), фибриногена (свыше 200 усл. ед.), содержание сиаловых кислот, серомукоида, отмечается диспротеинемия, гипер-1- и 2-глобулинемия.
Для клинической оценки иммунитета при ревматических заболеваниях необходимо исследование четырех главных компонентов иммунной системы, принимающих участие в защите организма и патогенезе аутоиммунных заболеваний: гуморальный иммунитет (В-клетки), клеточно-опосредованный иммунитет (Т-клетки, моноциты), фагоцитарные клетки ретикуло-эндотелиальной системы (нейтрофилы, макрофаги) и комплемент.
Исследование синовиальной жидкости позволяет дифференцировать дистрофические и воспалительные заболевания суставов, выделять в ряде случаев определенные нозологические формы. Синовиальную жидкость получают путем пункции сустава и оценивают по ряду параметров: цвет, вязкость, прозрачность, характер муцинового сгустка и цитологический состав.
Рентгенологическое исследование суставов – один из важных методов визуализирующего исследования у больных суставной патологией. При этом необходимо учитывать стадии развития процесса. Наиболее типичные рентгенологические изменения при суставных синдромах представлены в табл. 11.
Таблица 11. Рентгенологические признаки при различных заболеваниях суставов
|
Заболевание |
Рентгенологические признаки |
|
Ревматоидный артрит |
Краевые костные эрозии эпифизов |
|
Псориатическая артропатия |
Остеолиз дистальных фаланг пальцев |
|
Остеоартроз |
Подхрящевой остеосклероз, остеофиты |
|
Подагра |
Деструктивный артроз, «пробойники» |
|
Болезнь Бехтерева |
Сакроилеит, кальцификация, связок позвоночника |
Ультразвуковое исследование является неинвазивным, объективным, достаточно недорогим и простым по технике выполнения методом обследования суставов и мягких тканей, которое позволяет диагностировать их патологию, визуализировать травматические, воспалительные и дегенеративные явления суставно-мышечно-связочного аппарата человека, а также выбирать тактику локальной терапии и контролировать ее результаты.
На сегодняшний день в диагностике патологии суставов высоко значение и магнитно-резонансной томографии (МРТ), для проведения которой используют радиоволны и магнитное излучение, которые позволяют получить четкое изображение изучаемых органов и тканей. Поскольку МРТ позволяет получить очень четкую картину преимущественно мягких тканей, расположенных вокруг костей, поэтому часто используется при исследовании крупных суставов (коленных, плечевых и др.), позвоночника и межпозвонковых дисков. С помощью МРТ можно диагностировать даже небольшие разрывы сухожилий, связок и мышц, а также переломы, невидимые на обычных рентгенограммах.
Термография – метод исследования интенсивности инфракрасного излучения тканями. С помощью данного метода дистанционно измеряется температура кожи в области суставов, которая записывается на фотобумаге в виде контурной тени сустава. Метод может считаться визуализирующим и в то же время индикаторным, поскольку позволяет судить об активности воспалительного поражения суставов.
Радиоизотопная сцинтиграфия суставов проводится с помощью остеотропных препаратов (пирофосфат, фосфон), меченных 99mTc. Указанные препараты активно накапливаются в местах активного костного и коллагенового метаболизма. Особенно интенсивно они накапливаются в воспаленных тканях суставов, что отражается в виде сцинтиграммы суставов. Методику радионуклидной сцинтиграфии используют для ранней диагностики артритов, выявления субклинических фаз поражения суставов, дифференциальной диагностики воспалительных и дистрофических поражений суставов.
Артроскопия – визуальное исследование полости сустава. Оно позволяет устанавливать воспалительные, травматические или дегенеративные поражения менисков, связочного аппарата, поражений хряща, синовиальной оболочки. При этом есть возможность прицельной биопсии пораженных участков суставов.
Биопсия синовиальной оболочки проводится двумя способами – с помощью пункции сустава или во время артроскопии. При диффузных заболеваниях соединительной ткани производится также биопсия кожи и внутренних органов.
Основными задачами лечения больного с острым СС являются максимально полное его купирование с учетом этиологии, а также обеспечение условий для проведения полноценного курса реабилитационных мероприятий. Наиболее распространенным методом лечения пациентов с СС является применение нестероидных противовоспалительных препаратов (НПВП), эффективность которых подтверждена многочисленными клиническими исследованиями.
В основе фармакологического действия препаратов этой группы лежит способность ингибировать активность циклооксигеназы (ЦОГ) – ключевого фермента метаболизма арахидоновой кислоты – предшественника простагландинов. Уменьшение синтеза простагландинов сопровождается угнетением образования медиаторов отека и воспаления, снижением чувствительности нервных структур к брадикинину, гистамину, оксиду азота, образующимся в тканях при воспалении. Вместе с тем обезболивающий эффект НПВП может быть обусловлен не только торможением активности ЦОГ, но и другими механизмами.
Центральный механизм действия НПВП связан с угнетением синтеза простагландинов, которые образуются в центральной нервной системе и способствуют передаче болевого сигнала. НПВП снижают чувствительность болевых рецепторов, уменьшают отечность тканей в очаге воспаления, ослабляя механическое давление на ноцицепторы. Обсуждаются дополнительные механизмы противовоспалительной активности НПВП, не связанные с ингибированием ЦОГ: угнетение функции нейтрофилов и взаимодействие лейкоцитов с эндотелием сосудов, активации фактора транскрипции NF-kВ, регулирующего синтез провоспалительных медиаторов или, даже, опиоидоподобные эффекты.
Применение традиционных неселективных НПВП ассоциируются с более высокой частотой развития серьезных гастроинтестинальных эффектов. Согласно литературным данным, распространенность язв желудка и 12-перстной кишки у больных с долгосрочным приемом НПВП составляет около 20%, а ежегодная частота серьезных осложнений от этих язв – 1–4% [Laporte J., Ibáñez L., Vidal X. et al., 2004; Lanas A., Perez-Aisa M., Feu F. et al., 2005; Lanas A., García-Rodríguez L., Polo-Tomás M. et al., 2009].
У ЦОГ-2 селективных НПВП гастроинтестинальный профиль более благоприятный, что доказано серией клинических исследований, проведенных за последние 15 лет, но существуют данные о большем количестве неблагоприятных сердечно-сосудистых и почечных побочных эффектов. Поэтому, тщательное изучение сопутствующих заболеваний у пациента позволит врачу выбрать препарат, который будет эффективным и безопасным. Основным критерием в выборе препарата является соотношение пользы и риска развития побочных эффектов, а основные требования к современным НПВП включают не только вопросы эффективности, но и безопасности, а также возможности их комбинированного применения с другими препаратами (табл. 12).
Таблица 12. Основные требования к выбору НПВП у больных с суставным синдромом
|
Противовоспалительный эффект>обезболивающее действие • |
|
Возможность длительного приема лекарственного средства (несколько месяцев) |
|
Безопасность препарата (гастроэнтерологические побочные эффекты, АД, возможность назначать при поражении почек и печени) |
|
Возможность сочетать с другими препаратами (гипотензивные, сахароснижающие, антикоагулянты) |
|
Влияние на хрящ (синтез протеогликанов) – положительное или нейтральное |
Особенности действия нимесулида. Среди ЦОГ-2 селективных препаратов наиболее исследованным остается нимесулид (4-нитро-2-феноксиметансульфонамид) – уникальный противовоспалительный препарат, положительно отличающийся от большинства НПВП. Нимесулид – первый представитель нового класса селективных ингибиторов ЦОГ-2, представленных на мировом рынке. Он используется в клинической практике с 1985 г., когда впервые появился на фармацевтическом рынке Италии, в настоящее время это лекарственное средство зарегистрировано более чем в 50 странах мира. Нимесулид наиболее часто назначают среди НПВП в Италии, Португалии, Франции [Mathew S., Devi G., Prasanth V., 2011]. Препарат имеет высокую биодоступность, быстро и полностью всасывается из ЖКТ [Барскова В.Г., 2011].
Механизмы действия нимесулида . Влияние нимесулида обусловлено класс-специфическими механизмами, характерными для большинства НПВП и эффектами именно нимесулида. Как и все представители класса, нимесулид обладает противовоспалительным, обезболивающим и жаропонижающим действием. Препарат снижает концентрацию короткоживущего ПГН2, из которого под действием ПГ-изомеразы образуется ПГЕ2. Уменьшение концентрации ПГЕ2 ведет к снижению степени активации простаноидных рецепторов ЕР-типа, что реализуется в анальгетический и противовоспалительный эффекты. Препарат обратимо подавляет образование ПГЕ2 не только в очаге воспаления, но и в восходящих путях ноцицептивной системы, включая пути проведения болевых импульсов в спинном мозге. На ЦОГ-1 нимесулид действует незначительно и, практически, не препятствует образованию ПГЕ2 из арахидоновой кислоты в физиологических условиях, благодаря чему снижается количество побочных эффектов препарата (рис. 10).
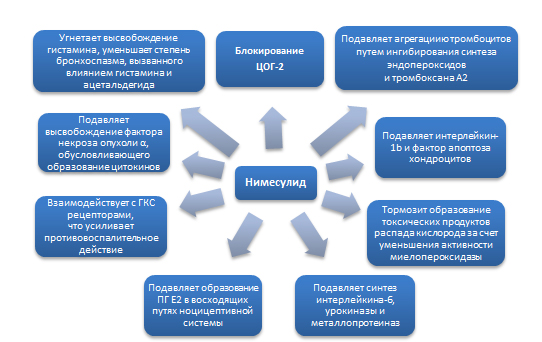
Рисунок 10. Механизмы действия нимесулида
Нимесулид подавляет агрегацию тромбоцитов путем ингибирования синтеза эндопероксидов и тромбоксана А2, подавляет синтез фактора агрегации тромбоцитов, подавляет высвобождение гистамина, а также уменьшает степень бронхоспазма, вызванного воздействием гистамина и ацетальдегида. Нимесулид ингибирует высвобождение фактора некроза опухоли α, который обусловливает образование цитокинов. Показано, что нимесулид способен подавлять синтез интерлейкина-6 и урокиназы, металлопротеиназ (эластазы, коллагеназы), замедляя разрушение протеогликанов и коллагена хрящевой ткани. Кроме того, нимесулид подавляет действие интерлейкина-1β и фактора апоптоза хондроцитов [Воробьева О.В., 2010].
Нимесулид обладает антиоксидантными свойствами, тормозит образование токсических продуктов распада кислорода за счет уменьшения активности миелопероксидазы, влияет на продукцию и действие окислительных радикалов, а также других компонентов нейтрофильной активации, что усиливает противовоспалительный и анальгетический эффекты и снижает вероятность гастроинтестинальной ульцерогенности. Взаимодействие нимесулида с ГКС рецепторами и активация их путем фосфорилирования усиливает противовоспалительное действие препарата.
Безопасность нимесулида. Нимесулид хорошо переносится, что выгодно отличает его от многих других представителей группы НПВП. Большинство побочных эффектов нимесулида являются класс-специфичными и зависят, в определенной степени, от фармакокинетики препарата.
Наиболее частым осложнением для всего класса НПВП является влияние на слизистую оболочку желудочно-кишечного тракта (ЖКТ). Изучению этого явления посвящено большое количество исследований. В исследовании F. Bradbury, где проведена оценка частоты осложнений со стороны ЖКТ при применении диклофенака (n=3553), нимесулида (n=3807) и ибупрофена (n= 470) в реальной клинической практике, суммарная частота этой патологии при использовании нимесулида была существенно меньше в сравнении при использованиис диклофенака (12,1 %) и не отличалась от таковой при использовании ибупрофена (8,1 и 8,6 %) [Bradbury F., 2004]. Итальянские исследователи A. Conforti et al. провели анализ 10608 сообщений о серьезных побочных явлениях, связанных с приемом различных НПВП с 1988 по 2000 г. Оказалось, что нимесулид был причиной развития тех или иных осложнений со стороны ЖКТ в 2 раза реже, чем другие НПВП. Таким образом, количество нежелательных явлений при применении нимесулида составило 10,4%, диклофенака – 21,2%, кетопрофена – 21,7%, пироксикама – 18,6% [Conforti A., Leone R., Moretti U. et al., 2001]. Риск развития желудочно-кишечного кровотечения при использовании нимесулида в реальной клинической практике оценивался в масштабном эпидемиологическом исследовании J. Laporte et al. Согласно полученным результатам, относительный риск кровотечения для нимесулида составил 3,2, для диклофенака – 3,7, мелоксикама – 5,7, а рофекоксиба – 7,2.
Гастроинтестинальная безопасность нимесулида обусловлена отсутствием влияния на ЦОГ-1 и химическими свойствами препарата. Большинство традиционных НПВП по химической структуре – кислоты, которые оказывают повреждающее влияние на слизистую верхних отделов ЖКТ. Это является дополнительным, не связанным с угнетением синтеза ПГ, механизмом развития гастропатии. Нимесулид, напротив, имеет слабые кислотные свойства и не накапливается в слизистой оболочке желудка и кишечника. Кроме того, нимесулид снижает продукцию окислительных радикалов и лейкотриенов, а также выброс гистамина из тучных клеток, чем создает дополнительную протекцию слизистой оболочки ЖКТ. В многочисленных клинических исследованиях при различных заболеваниях костно-мышечной системы доказано, что подавляющее большинство побочных реакций для нимесулида со стороны ЖКТ транзиторные, слабо выраженные и слабо коррелируют с ульцерогенным эффектом. Двойное слепое исследование с использованием гастродуоденоскопии показало, что применение нимесулида в дозе 100 или 200 мг в течение 7 дней не приводило к изменениям слизистой оболочки по сравнению с плацебо. Таким образом, можно констатировать, что нимесулид крайне редко вызывает тяжелые гастроинтестинальные осложнения, что особенно важно для лиц старших возрастных групп.
Принципиальное значение для оценки безопасности нимесулида имеет опыт его длительного применения. Так, в работе P. Locker et al. 199 больных с ОА получали нимесулид (200 мг) или этодолак (600 мг) в течение 3 мес. Терапевтический потенциал нимесулида оказался выше: его действие оценили как «хорошо» или «отлично» 80% больных, в то время как препарату сравнения аналогичную оценку дали только 68% больных. При этом, хотя этодолак относится к селективным НПВП и считается препаратом с очень хорошей переносимостью, количество побочных эффектов в обеих группах лечения не отличалось. В масштабном исследовании Huskisson et al. нимесулид (200 мг/сут) или диклофенак (150 мг/сут) были назначены 279 пациентам с ОА, причем продолжительность терапии составила 6 мес. Эффективность препаратов, которую оценивали по динамике самочувствия больных и функциональному индексу Лекена, оказалась фактически одинаковой. Однако нимесулид существенно превосходил диклофенак по переносимости: появление побочных эффектов со стороны ЖКТ регистрировалось в 36 и 47 % больных соответственно (p<0,05). В настоящее время наиболее длительным и большим рандомизированным двойным слепым исследованием нимесулида остается работа W. Kriegel et al. В этом исследовании определялись эффективность и безопасность нимесулида (200 мг) и напроксена (750 мг) у 370 больных с ОА в течение 12 мес. Как и в работе Huskisson, эффективность обоих препаратов оказалась сопоставимой. Количество осложнений при использовании нимесулида также оказалось меньшим: суммарно 47,5% (54,5 % – у пациентов, получавших напроксен). Очень важно, что ни в одной из трех представленных работ не зафиксировано значимого повышения частоты кардиоваскулярных осложнений на фоне длительного приема нимесулида.
Применение нимесулида связано с низкой частотой аллергических реакций, поскольку он обладает также дополнительными эффектами, которые реализуют его гипоаллергенность, в частности, подавляет фосфодиэстеразу IV, редуцирует выброс гистамина из базофилов и тучных клеток. Эти дополнительные свойства позволяют рассматривать нимесулид как альтернативный противовоспалительный препарат для пациентов с реакциями гиперчувствительности на традиционные НПВП [Воробьева О.В., 2010].
Таким образом, нимесулид – уникальный представитель класса НПВП, который быстро и эффективно уменьшает выраженность болевого синдрома. На сегодняшний день применение нимесулида удачно решает проблему легкой и умеренной боли в амбулаторной практике, однако в последнее время при длительном лечении болевого синдрома у больных все большее предпочтение отдают другому неселективному представителю НПВП – амтолметина гуацилу, который обладает выраженным противовоспалительным, анальгезирующим, жаропонижающим, десенсибилизирующим действием. Кроме того, отличительной особенностью этого препарата является то, что он – единственный представитель группы НПВП, обладающий и гастропротекторным эффектом.
Амтолметина гуацил (АМГ) получен путем добавления к молекуле толметина аминокислоты ванилина, что привело к существенному изменению его фармакологических свойств. В отличие от своего предшественника он приобрел гастропротективные свойства, связанные в первую очередь с подавлением активности ингибиторов iNOS, что приводит к существенному повышению концентрации NO в слизистой оболочке ЖКТ. В экспериментальных работах было показано многократное нарастание активности iNOS в слизистой оболочке ЖКТ лабораторных животных, получавших АМГ; ни плацебо, ни толметин такого эффекта не оказывали [Yuan-Hai Li, Jun Li, Yan Huang et al., 2004; Coruzzi G ., Coppelli G, Spaggiari S. еt al., 2004].
В исследовании Tubaro E. и соавт. продемонстрировано дозозависимое подавление стимулированной желудочной секреции АМГ, таким образом, установлены его антисекреторные свойства. Помимо этого, АМГ отчетливо усиливал секрецию бикарбоната, являющегося основой щелочного буфера слизистой оболочки желудка. Кроме того, АМГ уменьшал повреждающее действие других НПВП. Так, по сравнению с плацебо или толметином, на фоне введения АМГ у лабораторных животных выявлено достоверное дозозависимое уменьшение выраженности ульцерации, вызванной приемом индометацина [Tubaro E., Belogi L., Mezzadri C.M., 2000].
После всасывания амтолметин гуацил сразу подвергается гидролизу эстеразами плазмы крови с образованием трех метаболитов: MED5, толметин и гвиакол, трансформирующихся до активного метаболита толметина, который проникает в ткани, оказывая фармакологическое действие.
Защитное действие АМГ на слизистую оболочку желудка реализуется путем стимуляции рецепторов капсаицина (также их называют ваниллоидными рецепторами), присутствующих в стенках ЖКТ. Вследствие того что в составе АМГ присутствует ванилиновая группа, он может стимулировать капсаициновые рецепторы, что в свою очередь вызывает высвобождение пептида, кодируемого геном кальцитонина, и последующее увеличение продукции оксида азота (NO). Оба этих действия создают противовес отрицательному эффекту, вызываемому снижением количества ПГ из-за ингибирования ЦОГ (рис. 11).
Во многочисленных исследованиях показано, что амтолметина гуацил эффективно подавляет провоспалительные факторы, снижает агрегацию тромбоцитов; угнетает ЦОГ-1 и ЦОГ-2, нарушает метаболизм арахидоновой кислоты, уменьшает образование ПГ (в т.ч. в очаге воспаления), подавляет экссудативную и пролиферативную фазы воспаления. Он уменьшает проницаемость капилляров, стабилизирует лизосомальные мембраны, тормозит синтез или инактивирует медиаторы воспаления (ПГ, гистамин, брадикинины, цитокины, факторы комплемента). Он также блокирует взаимодействие брадикинина с тканевыми рецепторами, восстанавливает нарушенную микроциркуляцию и снижает болевую чувствительность в очаге воспаления. Амтолметина гуацил влияет на таламические центры болевой чувствительности, снижает концентрацию биогенных аминов, обладающих альгогенными свойствами, увеличивает порог болевой чувствительности рецепторного аппарата. Он устраняет или уменьшает интенсивность болевого синдрома, уменьшает утреннюю скованность и отечность, увеличивает объем движений в пораженных суставах через 4 дня применения.
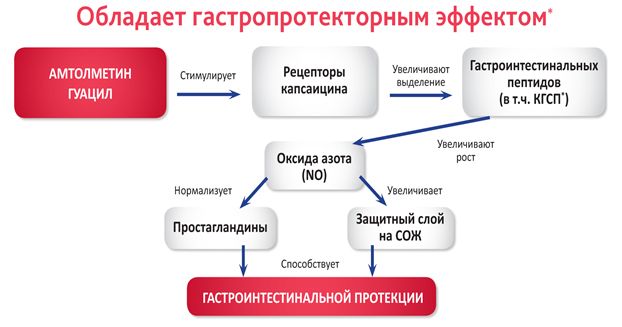
Рисунок 11. Механизм гастропротекторного эффекта амтолметина гуацила
В 1999 г. был опубликован мета-анализ серии 18 РКИ (n=780) продолжительностью от 4 нед. до 6 мес., в которых изучена частота развития побочных эффектов при использовании АМГ и традиционных НПВП (диклофенак, толметин, пироксикам, индометацин). Какие-либо осложнения на фоне АМГ возникали гораздо реже, чем в контрольных группах – (ОШ=0,2, 95% ДИ: 0,1-0,3; риск появления осложнений со стороны ЖКТ был меньше более чем в 3 раза – ОШ=0,3, 95% ДИ: 0,1-0,7). В трех РКИ (суммарно 92 больных) безопасность АМГ оценивали по результатам оценки эндоскопической картины верхних отделов ЖКТ. Препаратами сравнения были индометацин, толметин и диклофенак. Только у нескольких больных, получавших АМГ, развились единичные геморрагии или эрозии слизистой оболочки, в то время как прием обычных НПВП вызвал появление эрозий и язв почти у половины участников исследований.
Амтолметин гуацил хорошо переносится пациентами при длительном применении (в течение 6 мес). Его всасывание после перорального приема является быстрым и полным. Препарат, в основном, концентрируется в стенках желудка и кишечника, где в течение 2 ч после приема поддерживается его очень высокая концентрация.
Таким образом, с учетом многообразия суставного синдрома при различных заболеваниях, атипичности его проявлений в ряде случаев и неоднозначности трактовки некоторых признаков в настоящее время дифференциальная диагностика суставного синдрома является сложной клинической задачей и требует учета ряда анамнестических, клинических и других данных. Купирование болевого синдрома, особенно воспалительного характера требует применения НПВП, обладающих выраженным анальгетическим и противовоспалительным эффектом.
Немаловажными при длительном использовании препаратов являются вопросы их безопасности. В связи с этим применение умеренно селективных препаратов позволяет уменьшить риск возникновения побочных эффектов со стороны сердечно-сосудистой системы и ЖКТ. При решении вопроса о длительной терапии использование амтолметина гуацила является методом выбора, в связи с доказанной эффективностью в лечении данной группы пациентов и выраженным гастропротекторным эффектом.






